解题方法
1 . 将摩尔盐[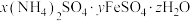 ]溶于水配成溶液,下列说法正确的是
]溶于水配成溶液,下列说法正确的是
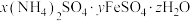 ]溶于水配成溶液,下列说法正确的是
]溶于水配成溶液,下列说法正确的是A.该溶液中还可大量共存 、 、 、 、 |
B.常温下该溶液中水电离出的 可能为 可能为 |
C.加入少量 后再滴入KSCN溶液,溶液变为红色,则证明溶液中含 后再滴入KSCN溶液,溶液变为红色,则证明溶液中含 |
D.向溶液中滴入 溶液使 溶液使 恰好沉淀时, 恰好沉淀时, 和 和 都会参与反应 都会参与反应 |
您最近一年使用:0次
解题方法
2 . 部分含铜物质的价类关系如图所示。下列说法正确的是

A.a能与FeCl3溶液反应: |
| B.b在酸性环境中可以转化为a和e |
| C.c经一步反应可转化为d |
D.若e为Cu(NO3)2,则其水溶液中可能大量存在H+、 、Fe2+ 、Fe2+ |
您最近一年使用:0次
2023-01-12更新
|
237次组卷
|
2卷引用:山东省滕州市2022-2023学年高三上学期期末质量检测化学试题
名校
解题方法
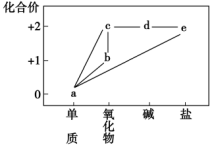
3 . 常温时,将0.1mol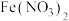 和2mol HC1溶于水得2L混合溶液,然后向该溶液投入mg铁粉使其充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是
和2mol HC1溶于水得2L混合溶液,然后向该溶液投入mg铁粉使其充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是
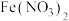 和2mol HC1溶于水得2L混合溶液,然后向该溶液投入mg铁粉使其充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是
和2mol HC1溶于水得2L混合溶液,然后向该溶液投入mg铁粉使其充分反应后,滴加KSCN溶液不变红色。下列有关说法正确的是A.由于氧化性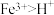 ,首先发生的反应是 ,首先发生的反应是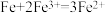 |
| B.当加入16.8g铁粉时,可生成标准状况下6.72L气体 |
C.在铁粉充分反应后的溶液中,铁元素以 和 和 的形式存在 的形式存在 |
| D.m至少等于28,反应过程中溶液的质量由于生成气体原因在减小 |
您最近一年使用:0次
名校
4 . 常温下,下列各离子组在指定溶液中能大量存在的是
A.pH=13的溶液中:Na+、ClO-、CO 、SO 、SO |
B.c(Fe3+)=0.1mol/L的溶液中:H+、I-、Br-、SO |
C.使石蕊变红的溶液中:Na+、NH 、NO 、NO 、SO 、SO |
| D.小苏打溶液中:Ba2+、Cl-、K+、OH- |
您最近一年使用:0次
2022-10-08更新
|
382次组卷
|
4卷引用:山东省枣庄滕州市2022-2023学年高三上学期期中考试化学试题
5 . 从古至今,铁及其化合物在人类生产生活中的作用发生了巨大改变。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是___________ (填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
若将该成分溶于足量的稀硫酸中,再滴加KSCN溶液,溶液变红,继续滴加双氧水至过量,溶液红色褪去,同时有气泡产生。
猜想一:气泡可能是 的反应产物
的反应产物 、
、 、
、 或
或 、
、 ;
;
猜想二:气泡还可能是___________ ,理由是___________ 。(用化学方程式表示)
(2)硫酸渣的主要化学成分为: 约45%,
约45%, 约40%,
约40%, 约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
①在步骤ⅰ中产生的有毒气体可能有___________ 。
②步骤ⅳ中,生成FeCO3的离子方程式是___________ 。
(3)古老而神奇的蓝色染料普鲁士蓝的合成方法如下:___________ 。
(1)古代中国四大发明之一的指南针是由天然磁石制成的,其主要成分是
a.Fe b.FeO c.Fe3O4 d.Fe2O3
若将该成分溶于足量的稀硫酸中,再滴加KSCN溶液,溶液变红,继续滴加双氧水至过量,溶液红色褪去,同时有气泡产生。
猜想一:气泡可能是
 的反应产物
的反应产物 、
、 、
、 或
或 、
、 ;
;猜想二:气泡还可能是
(2)硫酸渣的主要化学成分为:
 约45%,
约45%, 约40%,
约40%, 约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):
约10%,MgO约5%。用该废渣制取药用辅料——红氧化铁的工艺流程如下(部分操作和条件略):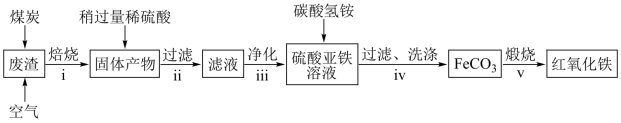
①在步骤ⅰ中产生的有毒气体可能有
②步骤ⅳ中,生成FeCO3的离子方程式是
(3)古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

您最近一年使用:0次
2022-09-14更新
|
475次组卷
|
3卷引用:山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题
山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题江苏省苏州市2022-2023学年高一下学期期末应考化学试题(已下线)重难点05 铁及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
2022高三·全国·专题练习
6 . 依据下列实验,预测的实验现象正确的是
| 选项 | 实验内容 | 预测的实验现象 |
| A |  溶液中滴加NaOH溶液至过量 溶液中滴加NaOH溶液至过量 | 产生白色沉淀后沉淀消失 |
| B |  溶液中滴加KSCN溶液 溶液中滴加KSCN溶液 | 溶液变血红色 |
| C | AgI悬浊液中滴加NaCl溶液至过量 | 黄色沉淀全部转化为白色沉淀 |
| D | 酸性 溶液中滴加乙醇至过量 溶液中滴加乙醇至过量 | 溶液紫红色褪去 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-04更新
|
8155次组卷
|
17卷引用:山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题
山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题(已下线)专题11 化学实验基础-2022年高考真题模拟题分项汇编2022年海南省高考真题化学试题(已下线)第08讲 铝、镁及其重要化合物(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)2022年海南省高考真题变式题1-14(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题浙江省东阳市横店高级中学2022-2023学年高三上学期10月份检测化学试题(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价新疆乌鲁木齐市高级中学2022-2023学年高三第一次模拟考试化学试题(已下线)回归教材重难点10 再现常考化学实验基础知识-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题05 元素化合物性质(已下线)专题05 元素化合物性质(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点2 物质的分离、提纯、检验与鉴别 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)第3讲 物质制备实验的设计与评价河南省项城市第三高级中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
7 . 某化学小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应,实验记录如下表所示:已知:Cu2++Cu+4Cl-=2[CuCl2]-,[CuCl2]- CuCl↓(白色)+Cl-
CuCl↓(白色)+Cl-
下列说法错误的是
 CuCl↓(白色)+Cl-
CuCl↓(白色)+Cl-| 序号 | Ⅰ | Ⅱ | Ⅲ |
| 实验步骤 | 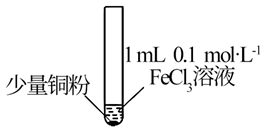 充分振荡,加入2 mL蒸馏水 | 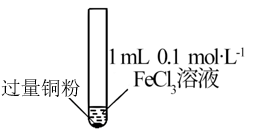 充分振荡,加入2 mL蒸馏水 | 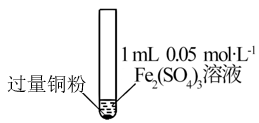 充分振荡,加入2mL蒸馏水 |
| 实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
| A.实验Ⅰ、Ⅱ、Ⅲ中,Fe3+均被还原 |
| B.实验Ⅰ中加入铜粉充分反应后,溶液中铜以[CuCl2]-的形式存在 |
| C.实验Ⅱ中所得白色沉淀能溶于饱和NaCl溶液 |
| D.向实验Ⅲ反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀 |
您最近一年使用:0次
2021-11-17更新
|
732次组卷
|
7卷引用:山东省枣庄市第三中学2021-2022学年高三上学期期中考试化学试题
山东省枣庄市第三中学2021-2022学年高三上学期期中考试化学试题山东省潍坊市2021-2022学年高三上学期期中考试化学试题山东省威海乳山市2021-2022学年高三上学期期中考试化学试题山东省潍坊市临朐中学2021-2022学年高三上学期期中统考化学试题山东省菏泽第一中学2022-2023学年高三上学期期中考试化学试题(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)吉林省长春外国语学校2021-2022学年高一上学期第二次月考化学试题
解题方法
8 . 化学与生产、生活密切相关,下列叙述错误的是
| A.电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法 |
| B.煤经过气化和液化两个化学变化,可变为清洁能源 |
| C.工业生产玻璃、水泥和陶瓷,均需用石灰石作原料 |
D.聚合硫酸铁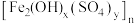 是新型絮凝剂,可用来处理水中的悬浮物 是新型絮凝剂,可用来处理水中的悬浮物 |
您最近一年使用:0次
名校
解题方法
9 . 从宏观现象探究微观本质是重要的化学学科素养。以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性,实验如下:
(1)①中反应的离子方程式是___________ 。
(2)②中逸出的无色气体是___________ ;从物质类别角度分析,Na2CO3与Na2SO3在化学方面的共性是__________ (写一条);从化合价角度分析,Na2CO3与Na2SO3在化学方面的差异是__________ (写一条)。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
I.甲取③中红棕色溶液少许,滴入盐酸酸化的BaCl2溶液,产生白色沉淀。甲得出结论:FeCl3与Na2SO3发生氧化还原反应,离子方程式是___________ 。
II.乙认为甲的实验不严谨,重新设计并进行实验,证实了甲的结论是正确的。其实验方案是____________ 。
(4)根据实验,FeCl3溶液与碱性物质之间的反应多样性与__________ 有关。
| 2mL0.2mol/LFeCl3溶液(pH=1) | 加入试剂 | 现象 |
| ①2mLMg(OH)2浊液(pH=11) | 产生红褐色胶体 | |
| ②滴加2mL0.2mol/LNa2CO3溶液(pH=12) | 逸出无色气体,产生红褐色沉淀 | |
| ③滴加2mL0.2mol/LNa2SO3溶液(pH=10) | 无色气体产生,黄色溶液变为红棕色 |
(1)①中反应的离子方程式是
(2)②中逸出的无色气体是
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
I.甲取③中红棕色溶液少许,滴入盐酸酸化的BaCl2溶液,产生白色沉淀。甲得出结论:FeCl3与Na2SO3发生氧化还原反应,离子方程式是
II.乙认为甲的实验不严谨,重新设计并进行实验,证实了甲的结论是正确的。其实验方案是
(4)根据实验,FeCl3溶液与碱性物质之间的反应多样性与
您最近一年使用:0次
2020-09-28更新
|
248次组卷
|
2卷引用:山东省枣庄市第三中学2021届高三上学期9月阶段性检测化学试题
名校
10 . 下列正确的是
| A.CO2、NH3的水溶液能导电,所以CO2、NH3均是电解质 |
| B.升温可以加快Na与空气中O2反应制取Na2O的反应速率 |
| C.将废铁屑加入FeCl3溶液中,可用于除去工业废气中的Cl2 |
| D.FeCl3腐蚀Cu刻制印刷电路板可说明铁比铜金属性强 |
您最近一年使用:0次



