名校
解题方法
1 . 铁元素在地壳中的含量仅次于氧、硅和铝居第四位。铁及其化合物应用广泛。高铁酸钾( )是种新型、高效、多功能水处理剂,其制备原理如下:
)是种新型、高效、多功能水处理剂,其制备原理如下: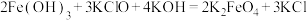
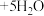 。下列铁及其化合物的性质与用途具有对应关系的是
。下列铁及其化合物的性质与用途具有对应关系的是
 )是种新型、高效、多功能水处理剂,其制备原理如下:
)是种新型、高效、多功能水处理剂,其制备原理如下: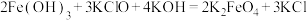
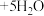 。下列铁及其化合物的性质与用途具有对应关系的是
。下列铁及其化合物的性质与用途具有对应关系的是A. 中铁的化合价为+6,有还原性,可用于净水 中铁的化合价为+6,有还原性,可用于净水 |
B. 受热易分解,可用于吸附杂质 受热易分解,可用于吸附杂质 |
C. 有氧化性,可用于制作印刷铜电路板 有氧化性,可用于制作印刷铜电路板 |
D. 能与盐酸反应,可用于制作油漆涂料 能与盐酸反应,可用于制作油漆涂料 |
您最近一年使用:0次
2022-11-15更新
|
245次组卷
|
2卷引用:宁夏六盘山高级中学 2022-2023学年高一上学期期中联考化学试题
解题方法
2 . 铁是应用最广泛的金属,铁的卤化物、氧化物等均为重要化合物。回答下列问题。
(1)FeCl3溶液吸可以吸收烟气中的SO2,该反应的离子方程式是___________ 。
(2)已知反应:3Br2 + 6FeCl2 = 4FeCl3 + 2FeBr3,向1L 0.4mol/L的FeBr2溶液中通入6.72LCl2(标准状况),写出该反应的离子方程式(用总方程式表示)___________
(3)已知铁的某种氧化物化学式为FexO(x<1),铁元素的质量分数为76.3%,则FexO中x值(精确至0.01)为___________ ,该氧化物中的Fe分别为Fe2+、Fe3+,计算n(Fe2+):n(Fe3+)= ___________
(4)用一定量的铁与足量的稀H2SO4及足量的CuO制单质铜,有人设计以下两种方案:
①Fe H2
H2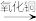 Cu,②CuO
Cu,②CuO  CuSO4
CuSO4 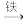 Cu。
Cu。
若实验过程中,根据规范的实验方法和实验操作规则进行操作,则两者制得单质铜的量作比较正确的是___________
A.相等 B.①多 C.②多 D.无法判断
(5)在铁与铜的混合物中,加入不足量的稀硝酸,反应后剩余金属m1 g;再向其中加入一定量稀硫酸,充分振荡后,剩余金属m2 g,则m1___________ (填“大于”、“可能大于”、“等于”或“可能等于”)m2
(6)以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到4molFe(OH)3沉淀,此间共消耗的水的物质的量为___________ mol
(1)FeCl3溶液吸可以吸收烟气中的SO2,该反应的离子方程式是
(2)已知反应:3Br2 + 6FeCl2 = 4FeCl3 + 2FeBr3,向1L 0.4mol/L的FeBr2溶液中通入6.72LCl2(标准状况),写出该反应的离子方程式(用总方程式表示)
(3)已知铁的某种氧化物化学式为FexO(x<1),铁元素的质量分数为76.3%,则FexO中x值(精确至0.01)为
(4)用一定量的铁与足量的稀H2SO4及足量的CuO制单质铜,有人设计以下两种方案:
①Fe
 H2
H2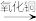 Cu,②CuO
Cu,②CuO  CuSO4
CuSO4 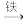 Cu。
Cu。若实验过程中,根据规范的实验方法和实验操作规则进行操作,则两者制得单质铜的量作比较正确的是
A.相等 B.①多 C.②多 D.无法判断
(5)在铁与铜的混合物中,加入不足量的稀硝酸,反应后剩余金属m1 g;再向其中加入一定量稀硫酸,充分振荡后,剩余金属m2 g,则m1
(6)以铁为阳极,铜为阴极,对足量的NaOH溶液进行电解。一段时间后得到4molFe(OH)3沉淀,此间共消耗的水的物质的量为
您最近一年使用:0次
名校
3 . 回答下列问题
(1)请写出一定条件下 Cu 与浓硫酸反应制取二氧化硫的化学方程式:___________ 。该反应中发生氧化反应的物质是__________ ,1mol氧化剂得到__________ mol电子。
(2)PH<______ 的雨称为酸雨。向煤中加入适量的______ 可大大减少燃烧产物中二氧化硫的含量。
(3)一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比为__________ 。
(1)请写出一定条件下 Cu 与浓硫酸反应制取二氧化硫的化学方程式:
(2)PH<
(3)一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的浓度恰好相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比为
您最近一年使用:0次



