名校
解题方法
1 . 常温下,下列各组离子在给定条件下一定能大量共存的是
A.滴加KSCN溶液显红色的溶液中:NH 、K+、Cl-、I- 、K+、Cl-、I- |
B.能使蓝色石蕊试纸显红色的溶液:Na+、NO 、SO 、SO 、Fe2+ 、Fe2+ |
C.无色透明的溶液:Na+、Ca2+、Cl-、MnO |
D.遇酚酞变红的溶液:Ba2+、K+、NO 、Cl- 、Cl- |
您最近一年使用:0次
名校
解题方法
2 . 制作电路板的废液中含有大量CuCl2、FeCl2和FeCl3,某化学兴趣小组想要从中回收铜,并将铁的化合物全部转化为FeCl3溶液作为腐蚀液原料循环使用,流程如图所示。
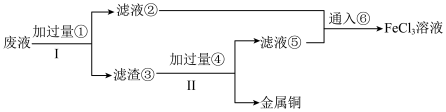
| A.步骤Ⅰ中所加的试剂①是铁粉 |
| B.步骤Ⅱ的操作为过滤 |
| C.滤渣③成分为Cu、Fe,物质④为CuCl2溶液 |
| D.检验废液中是否含有Fe3+可用KSCN溶液 |
您最近一年使用:0次
3 . 检验某补铁剂(主要含 )是否变质,将其溶于蒸馏水配成溶液后,再加入的检验试剂是
)是否变质,将其溶于蒸馏水配成溶液后,再加入的检验试剂是
 )是否变质,将其溶于蒸馏水配成溶液后,再加入的检验试剂是
)是否变质,将其溶于蒸馏水配成溶液后,再加入的检验试剂是| A.氨水溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D.KSCN溶液 |
您最近一年使用:0次
名校
解题方法
4 . 一种利用磁铁矿( )制备铁红的流程如下:
)制备铁红的流程如下:
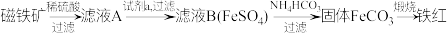
下列说法正确的是
 )制备铁红的流程如下:
)制备铁红的流程如下: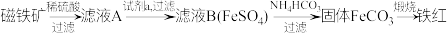
下列说法正确的是
A.往滤液A中滴加少量酸性 溶液,可观察到紫红色褪去 溶液,可观察到紫红色褪去 |
B.可以用KSCN溶液和氯水检验滤液A中是否有 |
C. 在空气中煅烧的反应方程式为 在空气中煅烧的反应方程式为 |
| D.最终得到铁红中的Fe元素的质量小于原磁铁矿中的Fe元素的质量 |
您最近一年使用:0次
5 . 化学来源于生活,且应用于生活。请根据题意填空:
(1)补铁剂(铁以 形式表示)需密封保存以防变质,为检验某补铁剂是否变质,可选用的试剂为
形式表示)需密封保存以防变质,为检验某补铁剂是否变质,可选用的试剂为___________ (填“KSCN溶液”或“氯水”)。
(2)铝制品表面有一层氧化铝薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:_________ 。

(3)稀土元素被称为“冶金工业的维生素”,包括镧系元素以及钪和钇,共___________ (填“10”或“17”)种元素。
(1)补铁剂(铁以
 形式表示)需密封保存以防变质,为检验某补铁剂是否变质,可选用的试剂为
形式表示)需密封保存以防变质,为检验某补铁剂是否变质,可选用的试剂为(2)铝制品表面有一层氧化铝薄膜,有较好的耐腐蚀性,但盛装酸性或碱性物质时,铝制品腐蚀较快。请完成化学方程式:

(3)稀土元素被称为“冶金工业的维生素”,包括镧系元素以及钪和钇,共
您最近一年使用:0次
6 . 下列实验方案及现象、结论均正确的是
选项 | 实验方案及现象 | 结论 |
A | 取少量样品溶液于试管中,加入足量浓NaOH溶液,加热,再用湿润红色石蕊试纸于试管口检验,试纸变蓝 | 该样品中含 |
B | 取少量样品溶液于试管中,加入几滴BaCl2溶液,产生白色沉淀,再加入盐酸酸化,沉淀不完全溶解 | 该样品中含有 |
C | 用玻璃棒蘸取某样品进行焰色试验时观察到黄色火焰 | 该样品中含钠元素 |
D | 取少量样品溶液于试管中,加入几滴KSCN溶液,无明显现象 | 该样品中不含铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 下列离子在指定溶液中一定能大量共存的是
A.酸性溶液中: 、 、 、 、 、 、 |
B.pH=2的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D.使紫色石蕊变红的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
8 . 下列化学实验事实及其解释或结论都正确的是
A.取少量溶液X,向其中加入适量新制氯水,再加几滴 溶液,溶液变红,说明X溶液中一定含有 溶液,溶液变红,说明X溶液中一定含有 |
B.将某固体试样完全溶于盐酸,再滴加 溶液,出现白色沉淀,则该固体试样中存在 溶液,出现白色沉淀,则该固体试样中存在 |
C.某待测溶液可能含有等浓度的下列离子中几种: 、 、 、 、 、 、 、 、 、 、 、 、 。取少量待测溶液于试管,加入足量 。取少量待测溶液于试管,加入足量 溶液得到白色沉淀,加热产生无色气体,则原溶液中可能有 溶液得到白色沉淀,加热产生无色气体,则原溶液中可能有 |
D.向 溶液中加入 溶液中加入 溶液,有白色沉淀生成;再加入四氯化碳振荡,四氯化碳层呈紫色,白色沉淀可能为 溶液,有白色沉淀生成;再加入四氯化碳振荡,四氯化碳层呈紫色,白色沉淀可能为 |
您最近一年使用:0次
名校
9 . 某废旧金属材料中主要含 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: 。
。
回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去_______ 。
(2) 的电子式为
的电子式为_________ ,“碱浸”时发生反应的离子方程式为______ 。
(3)“操作Ⅰ”的名称为________ 。
(4)试剂a为_______ (填化学式),加入试剂a后可能发生的反应为______ (写出其中1个反应的离子方程式即可)。
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量______ (填离子符号),检验该离子的操作是______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物:
和可燃性有机物,现利用下列工艺流程回收部分金属及金属化合物: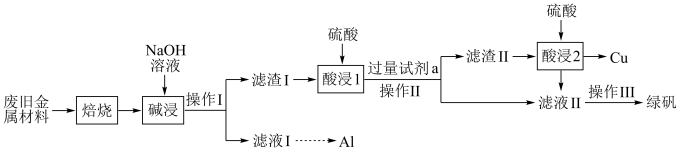
 。
。回答下列问题:
(1)“焙烧”的目的是将金属单质转化为氧化物,并除去
(2)
 的电子式为
的电子式为(3)“操作Ⅰ”的名称为
(4)试剂a为
(5)滤液Ⅱ中可能含有因氧气的作用而产生的少量
您最近一年使用:0次
10 . 由硫铁矿“烧渣”(主要成分: 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图: (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。
(1)①中加入的酸为___________ 。①中 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为___________ 。
(2)关于制备流程中含铁微粒的描述,错误的是___________。
(3)反应②需在高温高压下进行,且随着反应温度的升高,硫铁矿烧渣酸浸液中 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式___________ 。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、___________ 过滤、洗涤、干燥。
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀 酸化,用
酸化,用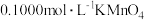 溶液滴定,消耗
溶液滴定,消耗 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为___________ %(保留一位小数)。
(6)长期放置的 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾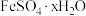 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入___________ ,其原因是___________ (用离子方程式表示)。
(7) 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知
在空气中加热反应可制得铁系氧化物材料。已知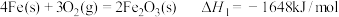
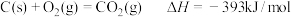

则:4FeCO3(s)+O2(g) 2Fe2O3(s)+4CO2(g) ΔH=
2Fe2O3(s)+4CO2(g) ΔH=___________ 。
(8)用一氧化碳还原氮氧化物,可防止氮氧化物污染。已知:
①2C(s)+O2(g)=2CO(g) ΔH1=-221kJ•mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+181kJ•mol-1
③2CO(g)+2NO(g)=2CO2(g)+N2(g) ΔH3=-747kJ•mol-1
则C(s)的燃烧热为___________ 。
 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图: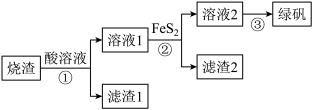
 (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。(1)①中加入的酸为
 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为(2)关于制备流程中含铁微粒的描述,错误的是___________。
A.步骤①,硫酸酸溶后溶液中主要有 、 、 等正离子 等正离子 |
B.步骤①后可依次用KSCN溶液和酸性 溶液来检测溶液中铁元素的价态 溶液来检测溶液中铁元素的价态 |
| C.Fe元素位于周期表的第ⅥB族 |
D.步骤②中加入硫铁矿的目的是将 还原为 还原为 |
(3)反应②需在高温高压下进行,且随着反应温度的升高,硫铁矿烧渣酸浸液中
 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式(4)通过③得到绿矾晶体的实验操作:加热浓缩、
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀
 酸化,用
酸化,用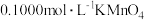 溶液滴定,消耗
溶液滴定,消耗 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为(6)长期放置的
 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾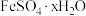 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入(7)
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知
在空气中加热反应可制得铁系氧化物材料。已知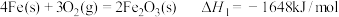
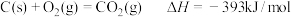

则:4FeCO3(s)+O2(g)
 2Fe2O3(s)+4CO2(g) ΔH=
2Fe2O3(s)+4CO2(g) ΔH=(8)用一氧化碳还原氮氧化物,可防止氮氧化物污染。已知:
①2C(s)+O2(g)=2CO(g) ΔH1=-221kJ•mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+181kJ•mol-1
③2CO(g)+2NO(g)=2CO2(g)+N2(g) ΔH3=-747kJ•mol-1
则C(s)的燃烧热为
您最近一年使用:0次



