名校
1 . 某磁黄铁矿的主要成分是FeXS(S为-2价), 磁黄铁矿中既含有二价铁又含有三价铁。将一定量的该磁黄铁矿与盐酸完全反应(注:矿石中其他成分不与盐酸反应,生成2.4g硫单质、 0.5molFeCl2和一定量H2S气体,且溶液中滴加KSCN溶液不变血红色。
回答下列问题:
(1)该磁黄铁矿FexS中,Fe2+ (二价铁) 与Fe3+ (三价铁)的物质的量之比为__________ 。
(2)该磁黄铁矿FeXS中,x=_________ (保留 2位有效数字)
回答下列问题:
(1)该磁黄铁矿FexS中,Fe2+ (二价铁) 与Fe3+ (三价铁)的物质的量之比为
(2)该磁黄铁矿FeXS中,x=
您最近一年使用:0次
2022-01-18更新
|
488次组卷
|
2卷引用:浙江省杭州西湖区学军中学紫金港校区2020--2021学年高一上学期期末化学试题
解题方法
2 . 由铜和三氧化二铁组成的混合粉末共 ,加入到浓度为
,加入到浓度为 的硫酸中,使之充分反应。
的硫酸中,使之充分反应。
(1)若硫酸溶液过量,且测得反应后溶液中 和
和 的物质的量相等,则原混合物中铜的质量为
的物质的量相等,则原混合物中铜的质量为___________ g;
(2)若固体混合物恰好能全部溶解在硫酸中,且消耗的硫酸体积为 ,求V的最小值,并简要写出推理及计算过程。
,求V的最小值,并简要写出推理及计算过程。___________
 ,加入到浓度为
,加入到浓度为 的硫酸中,使之充分反应。
的硫酸中,使之充分反应。(1)若硫酸溶液过量,且测得反应后溶液中
 和
和 的物质的量相等,则原混合物中铜的质量为
的物质的量相等,则原混合物中铜的质量为(2)若固体混合物恰好能全部溶解在硫酸中,且消耗的硫酸体积为
 ,求V的最小值,并简要写出推理及计算过程。
,求V的最小值,并简要写出推理及计算过程。
您最近一年使用:0次
3 . 确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别加入30.0 mL某浓度的稀硫酸中,充分反应后, 每组样品剩余固体的质量与原样品质量的关系如图所示。

(1)该混合物中,n(Fe2O3):n(Cu)=___________ 。
(2)稀硫酸的物质的量浓度为___________ 。

(1)该混合物中,n(Fe2O3):n(Cu)=
(2)稀硫酸的物质的量浓度为
您最近一年使用:0次
2021-05-29更新
|
964次组卷
|
5卷引用:【浙江新东方】【2021.5.19】【SX】【高三下】【高中化学】【SX00147】
(已下线)【浙江新东方】【2021.5.19】【SX】【高三下】【高中化学】【SX00147】【省级联考】浙江省2020届普通高校招生选考科目化学模拟试题(六)(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题浙江省宁波市九校2021-2022学年高一上学期期末联考化学试题浙江省舟山市舟山中学2022-2023学年高一上学期12月质量检测化学试题
名校
4 . 市售铁强化盐中铁含量测定。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为___________ 。
(2)样品中铁元素的质量分数为___________ (列出式子即可)。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O
 =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为
(2)样品中铁元素的质量分数为
您最近一年使用:0次
21-22高一上·浙江·阶段练习
5 . Ⅰ.2.7gAl与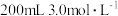 的稀盐酸充分反应,试计算:
的稀盐酸充分反应,试计算:
(1)在标准状况下生成氢气的体积为___________ L。
(2)用6.0mol/L盐酸配制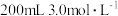 盐酸,需要量取6.0mol/L盐酸的体积
盐酸,需要量取6.0mol/L盐酸的体积___________ mL。
Ⅱ.现有 和
和 的混合溶液,将其分为两等份,向其中一份中加入
的混合溶液,将其分为两等份,向其中一份中加入 溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为mg;向另一份溶液加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。试计算:
溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为mg;向另一份溶液加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。试计算:
(1)m=___________ 。
(2)则原溶液中K+的物质的量浓度为___________ mol/L(写出计算过程)。
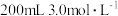 的稀盐酸充分反应,试计算:
的稀盐酸充分反应,试计算:(1)在标准状况下生成氢气的体积为
(2)用6.0mol/L盐酸配制
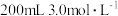 盐酸,需要量取6.0mol/L盐酸的体积
盐酸,需要量取6.0mol/L盐酸的体积Ⅱ.现有
 和
和 的混合溶液,将其分为两等份,向其中一份中加入
的混合溶液,将其分为两等份,向其中一份中加入 溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为mg;向另一份溶液加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。试计算:
溶液,至恰好不再产生沉淀,消耗50mL,将沉淀过滤、洗涤、干燥,称其质量为mg;向另一份溶液加入铁片,充分反应后,取出铁片,洗涤、烘干,称其质量比原来减轻了0.56g。试计算:(1)m=
(2)则原溶液中K+的物质的量浓度为
您最近一年使用:0次
21-22高一上·浙江·期末
解题方法
6 . 称取6.00g氧化铜和氧化铁固体混合物,加50.0mL3.00mol•L-1的硫酸充分溶解,再往所得溶液中加入5.60g铁粉,恰好完全溶解,得到单一溶质的溶液,所得溶液加KSCN,无明显现象。请计算:
(1)加入铁粉反应后,所得溶液中溶质的物质的量___ mol。
(2)固体混合物中氧化铜的质量___ g。
(1)加入铁粉反应后,所得溶液中溶质的物质的量
(2)固体混合物中氧化铜的质量
您最近一年使用:0次
名校
解题方法
7 . 向100 mL FeCl3和CuCl2的混合溶液中加入铁粉,其固体质量的变化如图所示,假设溶液体积不变,求:

(1)原混合溶液中FeCl3的物质的量___________
(2)c点溶液中FeCl2的物质的量浓度___________

(1)原混合溶液中FeCl3的物质的量
(2)c点溶液中FeCl2的物质的量浓度
您最近一年使用:0次
20-21高一上·浙江绍兴·阶段练习
8 . 铁粉和氧化铁粉末的混合物共32.8g,加入到200mL的盐酸中,固体完全溶解,得到标准状况下4.48L氢气。经测定,反应后的溶液中c(H+)为0.5mol/L,反应后的溶液中加入KSCN不变红(忽略反应前后溶液体积变化)。请计算:
(1)反应中放出氢气的质量为__ 。
(2)原混合物中铁和氧化铁的物质的量之比为__ 。
(3)原盐酸的物质的量浓度为_ mol/L。
(1)反应中放出氢气的质量为
(2)原混合物中铁和氧化铁的物质的量之比为
(3)原盐酸的物质的量浓度为
您最近一年使用:0次
名校
9 . 称取一定量Fe2O3与Cu2O的混合粉末,用足量CO还原后,质量减轻8g。若原混合粉末用1L1mol∙L-1的稀H2SO4充分反应后,剩余固体质量为6.4g。已知:Cu2O+2H+=Cu+Cu2++H2O
(1)反应后硫酸的物质的量浓度为___ (设溶液体积不变)。
(2)原红色固体粉末中Fe2O3的物质的量为___ 。
(1)反应后硫酸的物质的量浓度为
(2)原红色固体粉末中Fe2O3的物质的量为
您最近一年使用:0次
2020-12-27更新
|
442次组卷
|
3卷引用:浙江省瑞安中学2020-2021学年高一下学期期初考试化学试题
10 . 有一包铁粉和铜粉混合均匀的粉末样品,为确定其组成,某同学将不同质量的该样品分别与20mL1mol/L的FeCl3溶液反应,实验结果如表所示(忽略反应前后溶液体积的微小变化):
(1)样品中铁和铜的物质的量之比n(Fe):n(Cu)=___________ 。
(2)实验②的滤液中Fe*的浓度为___________ (写出简要计算过程)。
| 实验序号 | ① | ② | ③ | ④ |
| m(粉末质量)/g | 0.45 | 0.90 | 1.80 | 3.60 |
| m(反应后剩余固体)/g | 0 | 0.32 | 1.24 | 3.04 |
(1)样品中铁和铜的物质的量之比n(Fe):n(Cu)=
(2)实验②的滤液中Fe*的浓度为
您最近一年使用:0次



