1 . 以铁屑(表面含少量 )为原料先制备
)为原料先制备 ,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:
,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:

(1)酸溶。将铁屑溶于足量的稀 中过滤所得溶液经检验不含
中过滤所得溶液经检验不含 。
。
①检验酸溶后的溶液是否含 的实验操作是
的实验操作是_______ 。
②滤液中不存在 的原因是
的原因是_______ 。
(2)沉淀、过滤。向酸溶后的溶液中滴加稍过量的 ,过滤得
,过滤得 。
。
①沉淀反应的离子方程式为_______ 。
②沉淀中 含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
 溶液,完全反应时,消耗
溶液,完全反应时,消耗 溶液20.00mL。
溶液20.00mL。
过程中发生的反应为: (未配平,假设杂质不参与反应)。计算沉淀中
(未配平,假设杂质不参与反应)。计算沉淀中 (相对分子质量为180)的质量分数
(相对分子质量为180)的质量分数_______ (写出计算过程)。
(3)灼烧。在氧气流中灼烧 得
得 、
、 。
。
①灼烧时发生反应的化学方程式为_______ 。
②研究发现, 也可以灼烧得到
也可以灼烧得到 ,但灼烧
,但灼烧 得到的
得到的 比灼烧
比灼烧 得到的
得到的 更容易被还原,可能的原因是
更容易被还原,可能的原因是_______ 。
(4)还原。为制得高纯度的还原铁粉,以下还原剂最合适的是_______ 。
A.碳粉 B.铝粉 C.氢气
 )为原料先制备
)为原料先制备 ,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:
,再通过灼烧、还原制备高纯度还原铁粉的工艺流程如下:
(1)酸溶。将铁屑溶于足量的稀
 中过滤所得溶液经检验不含
中过滤所得溶液经检验不含 。
。①检验酸溶后的溶液是否含
 的实验操作是
的实验操作是②滤液中不存在
 的原因是
的原因是(2)沉淀、过滤。向酸溶后的溶液中滴加稍过量的
 ,过滤得
,过滤得 。
。①沉淀反应的离子方程式为
②沉淀中
 含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
含量的测定:准确称取6.300g沉淀,加入适量蒸馏水和稀硫酸溶解、酸化,并转移入250mL容量瓶中定容,取25.00mL溶液,向其中滴加
 溶液,完全反应时,消耗
溶液,完全反应时,消耗 溶液20.00mL。
溶液20.00mL。过程中发生的反应为:
 (未配平,假设杂质不参与反应)。计算沉淀中
(未配平,假设杂质不参与反应)。计算沉淀中 (相对分子质量为180)的质量分数
(相对分子质量为180)的质量分数(3)灼烧。在氧气流中灼烧
 得
得 、
、 。
。①灼烧时发生反应的化学方程式为
②研究发现,
 也可以灼烧得到
也可以灼烧得到 ,但灼烧
,但灼烧 得到的
得到的 比灼烧
比灼烧 得到的
得到的 更容易被还原,可能的原因是
更容易被还原,可能的原因是(4)还原。为制得高纯度的还原铁粉,以下还原剂最合适的是
A.碳粉 B.铝粉 C.氢气
您最近一年使用:0次
2022-08-29更新
|
666次组卷
|
3卷引用:江苏省苏州市2021-2022学年高一下学期期末学业质量阳光指标调研(延期到8月)化学试题
20-21高一下·江苏苏州·期中
名校
解题方法
2 . 铁及其化合物在日常生活中应用广泛,请回答下列问题:
(1) Fe(NO3)3·9H2O易溶于水,微溶于硝酸,主要用作催化剂和媒染剂,工业上用细铁屑与稀硝随反应制备,主要流程如下:

①写出铁屑与稀硝酸反应的化学方程式___________ 。反应时温度控制在40 -50℃,不宜过高的原因是___________ 。
②制备过程中需控制加入铁屑的量,原因是___________ (用离子方程式回答)。
③制得的Fe(NO3)3·9H2O用20%HNO3洗涤,其原因是___________ 。
(2)上述工业生产的尾气中含有氮氧化物NOx,(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁,工业上常用Na2CO3溶液吸收处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO3+CO2 (I)
2NO2+Na2CO3=NaNO2+NaNO3+CO2 (II)
①将1 mol NOx通入Na2CO3溶液中被完全吸收时,溶液中生成的 、
、 两种离子的物质的量随x变化关系如下图所示,则图中线段a表示
两种离子的物质的量随x变化关系如下图所示,则图中线段a表示___________ (填离子符号)随x值变化的关系。

②为了检测吸收液中NaNO2含量,某兴趣小组取100 mL该吸收液,用0.0050 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液的体积为16.00 mL。
已知: 被氧化成
被氧化成 ,写出离子方程式
,写出离子方程式___________ ,则吸收液中NaNO2的物质的量浓度为___________ 。
(1) Fe(NO3)3·9H2O易溶于水,微溶于硝酸,主要用作催化剂和媒染剂,工业上用细铁屑与稀硝随反应制备,主要流程如下:

①写出铁屑与稀硝酸反应的化学方程式
②制备过程中需控制加入铁屑的量,原因是
③制得的Fe(NO3)3·9H2O用20%HNO3洗涤,其原因是
(2)上述工业生产的尾气中含有氮氧化物NOx,(NO和NO2的混合物,假设不含N2O4),对生态环境和人类健康带来较大的威胁,工业上常用Na2CO3溶液吸收处理NOx。
已知:NO不能与Na2CO3溶液反应。
NO+NO2+Na2CO3=2NaNO3+CO2 (I)
2NO2+Na2CO3=NaNO2+NaNO3+CO2 (II)
①将1 mol NOx通入Na2CO3溶液中被完全吸收时,溶液中生成的
 、
、 两种离子的物质的量随x变化关系如下图所示,则图中线段a表示
两种离子的物质的量随x变化关系如下图所示,则图中线段a表示
②为了检测吸收液中NaNO2含量,某兴趣小组取100 mL该吸收液,用0.0050 mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液的体积为16.00 mL。
已知:
 被氧化成
被氧化成 ,写出离子方程式
,写出离子方程式
您最近一年使用:0次
3 . 下列关于各图的叙述正确的是
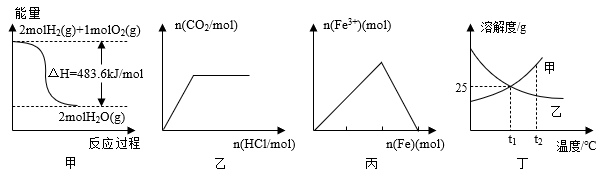

| A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8kJ•mol-1 |
| B.乙表示向碳酸钠溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸的物质的量的关系 |
| C.丙表示在稀硝酸溶液中加入铁粉,溶液中Fe3+的变化曲线 |
| D.丁表示t1℃时质量分数均为20%的甲、乙两种溶液,升温到t2℃时,两种溶液中溶质的质量分数仍然相等 |
您最近一年使用:0次
2016-12-09更新
|
191次组卷
|
3卷引用:2016届江苏省泰州中学高三上学期期中测试化学试卷



