解题方法
1 . 向含xmolHNO3和ymolH2SO4的混合稀溶液中缓慢加入铁粉,其氧化产物与所加铁粉的物质的量关系如图所示:
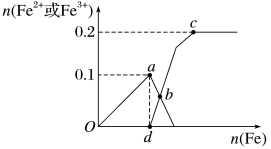
A.a点溶液中所含离子主要为Fe3+、 、 、 |
| B.dc段表示Fe2+物质的量变化,dc全段发生反应的离子方程式为Fe+2Fe3+=3Fe2+ |
| C.x=0.1,y=0.2 |
| D.反应至c点,可收集到标准状况下的气体体积为2.24L |
您最近半年使用:0次
名校
2 . 室温下,下列实验方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向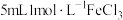 溶液中滴加 溶液中滴加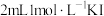 溶液,充分反应后,滴加KSCN溶液,观察现象 溶液,充分反应后,滴加KSCN溶液,观察现象 | 该反应是否为可逆反应 |
| B | 用pH计分别测定的 溶液和 溶液和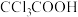 溶液的pH 溶液的pH | 探究键的极性对羧酸酸性的影响 |
| C | 向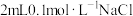 溶液中滴加2滴 溶液中滴加2滴 ,观察现象。振荡试管,再滴加2滴 ,观察现象。振荡试管,再滴加2滴 溶液,观察现象 溶液,观察现象 | 比较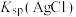 与 与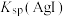 的大小 的大小 |
| D | 向CO还原Fe2O3所得到的产物中加入稀盐酸,滴加KSCN溶液,观察颜色变化 | Fe2O3全部被还原 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-03-17更新
|
496次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高三下学期阶段练习化学试题
名校
3 . 把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是
| A.硫酸铁溶液 | B.硫酸铜溶液 | C.稀硫酸 | D.硝酸银溶液 |
您最近半年使用:0次
名校
解题方法
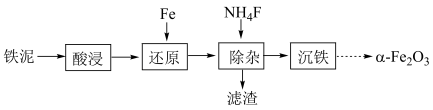
4 . 实验室由铁泥(主要成分为铁的氧化物及少量氧化钙)制备软磁性材料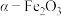 ,其主要实验流程如图。
,其主要实验流程如图。
已知: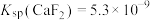 ,则下列说法
,则下列说法不正确 的是
 ,其主要实验流程如图。
,其主要实验流程如图。
已知:
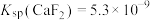 ,则下列说法
,则下列说法| A.“酸浸”时,可通过延长时间来提高铁元素浸出率 |
B.“还原”过程中除生成 外,还会生成 外,还会生成 |
C.“除杂”时,酸性条件下,更有利于 去除 去除 |
D.“沉铁”时,用氨水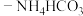 混合溶液代替 混合溶液代替 溶液,更有利于生成 溶液,更有利于生成 沉淀 沉淀 |
您最近半年使用:0次
5 . 分析以下几个反应(未配平),填空:
①Fe2++Zn→Zn2++Fe
②Fe2++Cl2→Fe3++Cl—
③Fe3++Fe→Fe2+
(1)Fe2+体现氧化性的是___________ (填反应的序号)。
(2)写出反应①对应的一个化学反应方程式___________ 。
(3)反应②中每1molCl2完全反应转移电子为___________ mol。
(4)对反应③进行配平,并用单线桥标注电子转移的方向和数目。______
___________Fe3++___________Fe=___________Fe2+
①Fe2++Zn→Zn2++Fe
②Fe2++Cl2→Fe3++Cl—
③Fe3++Fe→Fe2+
(1)Fe2+体现氧化性的是
(2)写出反应①对应的一个化学反应方程式
(3)反应②中每1molCl2完全反应转移电子为
(4)对反应③进行配平,并用单线桥标注电子转移的方向和数目。
___________Fe3++___________Fe=___________Fe2+
您最近半年使用:0次
6 . 对印刷电路板制作过程中( )产生废液
)产生废液 进行回收处理,流程如图所示。下列说法不正确的是
进行回收处理,流程如图所示。下列说法不正确的是

 )产生废液
)产生废液 进行回收处理,流程如图所示。下列说法不正确的是
进行回收处理,流程如图所示。下列说法不正确的是
A. 与 与 完全反应,转移电子数约为 完全反应,转移电子数约为 |
| B.实验室中进行操作①②时,需用到的玻璃仪器有烧杯、漏斗和玻璃棒 |
| C.若向溶液A中、溶液B中分别加入少量铁粉,铁粉均有减少 |
D.若废液 中滴加 中滴加 溶液变红,则 溶液变红,则 中 中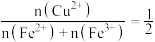 |
您最近半年使用:0次
解题方法
7 . 纳米铁是一种黑色粉末,可用于制作高密度磁性材料。以铁屑(含少量 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下:
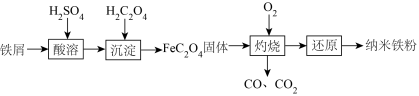
已知:草酸( )是一种二元酸
)是一种二元酸
(1)取少量产品分散于水中,___________ (填操作步骤),可验证所得铁粉直径是否为纳米级。
(2)写出“酸溶”时氧化还原反应的离子方程式:___________ 、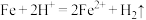 。
。
(3)若加入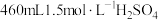 时,铁屑与
时,铁屑与 恰好完全反应,为了使
恰好完全反应,为了使 元素完全转化,则沉淀过程中加入
元素完全转化,则沉淀过程中加入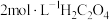 的体积至少为
的体积至少为___________  。
。
(4) 固体经灼烧后得到红棕色固体和
固体经灼烧后得到红棕色固体和 、
、 混合气体,若产物中
混合气体,若产物中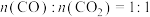 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为___________ 。
(5)纳米铁粉可用于处理含氧酸性废水中的 ,反应原理如图所示。
,反应原理如图所示。
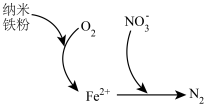
①该过程中体现了纳米铁粉的___________ 性(填“氧化”或“还原”)。
②在铁粉总量一定的条件下,废水中的溶解氧过多不利于 的去除,原因是
的去除,原因是___________ 。
 杂质)为原料制备纳米铁粉流程如下:
杂质)为原料制备纳米铁粉流程如下:
已知:草酸(
 )是一种二元酸
)是一种二元酸(1)取少量产品分散于水中,
(2)写出“酸溶”时氧化还原反应的离子方程式:
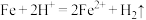 。
。(3)若加入
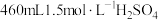 时,铁屑与
时,铁屑与 恰好完全反应,为了使
恰好完全反应,为了使 元素完全转化,则沉淀过程中加入
元素完全转化,则沉淀过程中加入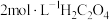 的体积至少为
的体积至少为 。
。(4)
 固体经灼烧后得到红棕色固体和
固体经灼烧后得到红棕色固体和 、
、 混合气体,若产物中
混合气体,若产物中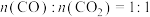 ,则“灼烧”过程中发生反应的化学方程式为
,则“灼烧”过程中发生反应的化学方程式为(5)纳米铁粉可用于处理含氧酸性废水中的
 ,反应原理如图所示。
,反应原理如图所示。
①该过程中体现了纳米铁粉的
②在铁粉总量一定的条件下,废水中的溶解氧过多不利于
 的去除,原因是
的去除,原因是
您最近半年使用:0次
8 . 氯气是一种重要的化工原料,在生产和生活中的应用十分广泛,可用于制漂白剂等。
Ⅰ.制新型灭菌消毒剂ClO2.在通常状况下,ClO2能溶于水,在水中的杀菌、消毒能力比Cl2强,且ClO2、Cl2在杀菌、消毒时均被还原为Cl-;浓的ClO2受热时易爆炸。
(1)制备ClO2反应为Cl2+2NaClO2=2NaCl+2ClO2,实验装置如下图所示:
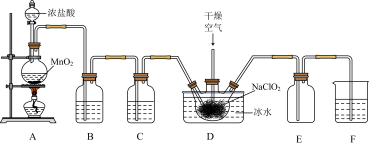
①装置A中发生反应的化学方程式为___________ ,装置B中盛放的试剂为___________ 。
②装置D中将三颈烧瓶置于冰水浴中并向其中通入干燥空气的目的是___________ 。
(2)等物质的量的ClO2和Cl2相比,ClO2的杀菌、消毒能力强于Cl2的原因是___________ 。
Ⅱ.制优良的饮用水消毒剂Na2FeO4.Na2FeO4具有很强的氧化性,能有效地杀灭水中的病菌和病毒,同时自身被还原成新生态的Fe(OH)3。
(3)制备方法如下:Fe(NO3)3+NaOH+Cl2—Na2FeO4+NaNO3+NaCl+H2O(未配平)。
①Na2FeO4中铁元素的化合价是___________ ,Na2FeO4属于___________ (填序号)。
A.酸 B.碱 C.盐 D.氧化物
②Na2FeO4作饮用水消毒剂的同时也能够起到净水作用的原因是___________ 。
Ⅰ.制新型灭菌消毒剂ClO2.在通常状况下,ClO2能溶于水,在水中的杀菌、消毒能力比Cl2强,且ClO2、Cl2在杀菌、消毒时均被还原为Cl-;浓的ClO2受热时易爆炸。
(1)制备ClO2反应为Cl2+2NaClO2=2NaCl+2ClO2,实验装置如下图所示:

①装置A中发生反应的化学方程式为
②装置D中将三颈烧瓶置于冰水浴中并向其中通入干燥空气的目的是
(2)等物质的量的ClO2和Cl2相比,ClO2的杀菌、消毒能力强于Cl2的原因是
Ⅱ.制优良的饮用水消毒剂Na2FeO4.Na2FeO4具有很强的氧化性,能有效地杀灭水中的病菌和病毒,同时自身被还原成新生态的Fe(OH)3。
(3)制备方法如下:Fe(NO3)3+NaOH+Cl2—Na2FeO4+NaNO3+NaCl+H2O(未配平)。
①Na2FeO4中铁元素的化合价是
A.酸 B.碱 C.盐 D.氧化物
②Na2FeO4作饮用水消毒剂的同时也能够起到净水作用的原因是
您最近半年使用:0次
9 . 下列实验的方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 实验方案设计 | 实验现象和结论 |
| A | 检验某固体试样中是否存在三价铁 | 取少量固体试样完全溶于盐酸,再滴加KSCN溶液 | 没有出现血红色,说明该固体试样中不存在三价铁 |
| B | 检验溴乙烷中溴元素 | 溴乙烷和NaOH溶液混合,振荡后加热,静置分层后,取少量上层清液,移入另一支试管中,加入2滴 溶液 溶液 | 若有淡黄色沉淀产生,则说明溴乙烷中含溴元素 |
| C | 比较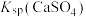 与 与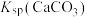 的大小 的大小 | 向饱和 溶液中滴加相同浓度的 溶液中滴加相同浓度的 溶液 溶液 | 产生白色沉淀,说明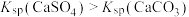 |
| D | 探究电石与水的反应 | 将电石与饱和食盐水反应产生的气体通入酸性高锰酸钾溶液 | 若酸性高锰酸钾溶液褪色,说明电石与水反应生成了乙炔 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-09-01更新
|
1161次组卷
|
8卷引用:江苏省句容三中、海安实验中学联考2023-2024学年高三上学期10月月考化学试题
10 . 除去下列物质中所含的少量杂质(括号内),所选用的试剂和分离方法均正确的是
| 选项 | 物质 | 试剂 | 分离方法 |
| A | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| B | 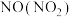 |  溶液 溶液 | 洗气 |
| C | 溴苯(液溴) |  溶液 溶液 | 分液 |
| D | 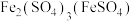 | Fe粉 | 过滤 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



