名校
1 . 化工生产中常利用硫酸厂煅烧黄铁矿石的烧渣(主要成分为 及少量
及少量 、
、 等)来制取绿矾
等)来制取绿矾 。具体制备流程如下:
。具体制备流程如下:

回答下列关于上述流程图中转化关系及操作的有关问题:
(1)在“灼烧”过程中发生的主要反应为: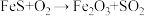 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为___________ ,氧化产物是___________ (填化学式)。
(2)足量“气体产物”通入下列溶液中,溶液会褪色的是___________(填字母序号)。
(3)“气体产物”易形成酸雨,酸雨是指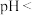
___________ 的雨水。技术员用氨水对“气体产物”进行吸收后再处理,可以回收 ,请你写出用过量氨水吸收
,请你写出用过量氨水吸收 时发生反应的化学方程式
时发生反应的化学方程式___________ 。
(4)加入足量稀硫酸时发生反应的离子方程式为:___________ 。
(5)“滤渣”的主要成分是___________ (填化学式)。
(6)加入足量X时发生反应的离子方程式为:___________ 。
(7)系列操作包括:___________ 、过滤、洗涤、干燥。
(8)绿矾保存不当,容易被氧化变质,为了检验所得产品是否变质,技术人员进行了以下操作:取少量产品(绿矾)置于试管中,加水溶解,向溶液中加入___________ 溶液,发现___________ (填现象),则绿矾已经变质。
 及少量
及少量 、
、 等)来制取绿矾
等)来制取绿矾 。具体制备流程如下:
。具体制备流程如下:
回答下列关于上述流程图中转化关系及操作的有关问题:
(1)在“灼烧”过程中发生的主要反应为:
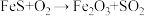 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(2)足量“气体产物”通入下列溶液中,溶液会褪色的是___________(填字母序号)。
| A.品红溶液 | B.紫色石蕊溶液 | C.酸性 溶液 溶液 | D.溴水 |
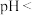
 ,请你写出用过量氨水吸收
,请你写出用过量氨水吸收 时发生反应的化学方程式
时发生反应的化学方程式(4)加入足量稀硫酸时发生反应的离子方程式为:
(5)“滤渣”的主要成分是
(6)加入足量X时发生反应的离子方程式为:
(7)系列操作包括:
(8)绿矾保存不当,容易被氧化变质,为了检验所得产品是否变质,技术人员进行了以下操作:取少量产品(绿矾)置于试管中,加水溶解,向溶液中加入
您最近一年使用:0次
2 . 从刻蚀印刷电路板的废液(主要成分为FeCl2、FeCl3、CuCl2)中回收铜并制备氯化铁晶体的一种工业流程如图:

回答下列问题:
(1)操作I的名称是___________ ,试剂a的化学式为___________ 。
(2)用FeCl3溶液刻蚀铜电路板的化学方程式为___________ 。
(3)试剂c可选用___________ (填标号)。若选择上述试剂,反应I中氧化剂与还原剂的物质的量之比为___________ 。
A.Zn B.H2O2 C.NaOH D.稀H2SO4
(4)为检验氯化铁晶体中是否混有FeCl2,某同学设计方案为:取少许样品于试管中,滴加稀硝酸。若观察到产生气泡,试管口附近有___________ 色气体产生,则混有FeCl2.从环保角度考虑,该实验方案存在的不足之处是___________ 。
(5)取1.000g产物溶于水中,加入足量NaOH溶液,经过滤、洗涤、灼烧后,所得红棕色固体的质量为0.320g,则该产物中铁元素的质量分数为___________ %。

回答下列问题:
(1)操作I的名称是
(2)用FeCl3溶液刻蚀铜电路板的化学方程式为
(3)试剂c可选用
A.Zn B.H2O2 C.NaOH D.稀H2SO4
(4)为检验氯化铁晶体中是否混有FeCl2,某同学设计方案为:取少许样品于试管中,滴加稀硝酸。若观察到产生气泡,试管口附近有
(5)取1.000g产物溶于水中,加入足量NaOH溶液,经过滤、洗涤、灼烧后,所得红棕色固体的质量为0.320g,则该产物中铁元素的质量分数为
您最近一年使用:0次



