名校
1 . 下列说法中正确的有几项
①钠在空气中燃烧生成淡黄色的Na2O2
②配制500mL0.6mol·L的NaOH溶液,需用托盘天平(用纸垫着)称量氢氧化钠固体12.0g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
①钠在空气中燃烧生成淡黄色的Na2O2
②配制500mL0.6mol·L的NaOH溶液,需用托盘天平(用纸垫着)称量氢氧化钠固体12.0g
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeSO4、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性
⑥将质量分数为5%和25%的硫酸等体积混合后,所得溶液中溶质的质量分数小于15%
⑦干燥的Cl2和氯水均能使鲜花褪色
| A.6项 | B.5项 | C.4项 | D.3项 |
您最近一年使用:0次
2 . Fe(OH)2具有较强的还原性,新制的白色Fe(OH)2会逐渐转变为灰绿色,使学生误认为氢氧化亚铁的颜色是灰绿色。为能较长时间观察到白色Fe(OH)2,某实验小组做了如下探究实验。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、___________ 、___________ 。
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是___________ 。
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:___________ 。___________ (用离子方程式表示)。
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:___________ 。
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
①由以上实验可得到的规律是___________ 。
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为___________ (填“1.0”“1.5”或“2.0”)mol/L。
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为___________ (任写一条)。
(1)配制实验所需一定物质的量浓度的溶液备用,配制溶液时所用仪器有托盘天平、烧杯、量筒、玻璃棒、
(2)实验时发现即使是用煮沸过的蒸馏水配制实验所用的溶液,新生成的Fe(OH)2也仅能存在几分钟,其原因可能是
(3)甲同学按如图a所示操作制备Fe(OH)2 (溶液均用煮沸过的蒸馏水配制)。挤入少量NaOH溶液后,立即出现白色沉淀,但很快变成浅绿色,一会儿后变为灰绿色,最终变为红褐色。请分析固体变色的原因:

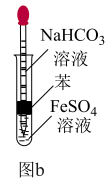
②结合原理和装置特点分析能较长时间观察到白色Fe(OH)2的原因:
(5)实验试剂最佳浓度探究:
采用不同浓度的试剂进行实验,记录如下。
c(NaHCO3)/(mol/L) c(FeSO4)/(mol/L) | 1.0 | 1.5 | 2.0 | |
| 1.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 3.5 min | 9 min | 24 min | |
| 1.5 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率较快 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率迅速 |
| 稳定时间 | 13 min | 15 min | 22 min | |
| 2.0 | 现象 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡增多 | 产生白色沉淀和气泡,沉淀逐渐变暗,气泡产生速率加快 | 常温下无现象,加热后产生白色沉淀 |
| 稳定时间 | 3 min | 8 min | 30 min | |
②NaHCO3溶液的浓度为1.5 mol/L时,FeSO4溶液的最佳浓度为
(6)实验创新:
延长Fe(OH)2沉淀的稳定时间还可以采取的措施为
您最近一年使用:0次
2024-04-16更新
|
306次组卷
|
2卷引用:广东省湛江市2024届高三下学期第二次模拟测试化学试题
3 . 坦克、导弹的制造材料主要是金属合金,钢铁便是其中十分重要的一种。下列关于铁的说法中正确的是
| A.铁元素属于过渡元素,其原子序数为26 |
| B.单质铁与浓硫酸在常温下不反应 |
| C.铁单质只具有还原性,其阳离子只具有氧化性 |
| D.与相同浓度的盐酸反应生成氢气的速率,纯铁比生铁的快 |
您最近一年使用:0次
解题方法
4 . A、B、C、D四种物质(或离子)均含有同一种元素,其中A是常见单质,它们之间存在如图所示的转化关系:

(1)若B、C均属于盐类,B溶液呈黄色,遇氨水能形成红褐色沉淀;D是一种不溶性碱;B、C中的阴离子均是 ,则A只有与
,则A只有与________ (填分子式)反应才能得到B;实验室制备的D物质不稳定,相应反应的化学方程式为__________________ 。
(2)若B具有强氧化性, 时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为
时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为____________ ,实验室可用D制备少量的C,反应的化学方程式为__________

(1)若B、C均属于盐类,B溶液呈黄色,遇氨水能形成红褐色沉淀;D是一种不溶性碱;B、C中的阴离子均是
 ,则A只有与
,则A只有与(2)若B具有强氧化性,
 时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为
时能产生黄色火焰,C、D的溶液均呈碱性且D与酸反应能生成一种无色气体,则B的化学式为
您最近一年使用:0次
2019-12-20更新
|
52次组卷
|
2卷引用:黑龙江省齐齐哈尔市三立高级中学2021-2022学年高三上学期第一次月考(10月)化学试题
5 . 某小组设计实验探究 是否能与
是否能与 形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯
形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯 进行实验,实验结果如图所示:
进行实验,实验结果如图所示:
 是否能与
是否能与 形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯
形成络离子。查阅资料:向难溶电解质中加入具有不同离子的可溶性强电解质溶液,会使难溶电解质溶解度增大,这种现象叫做“盐效应”。实验表明:“盐效应”与离子浓度、离子所带电量有关。分别取等量的纯 进行实验,实验结果如图所示:
进行实验,实验结果如图所示: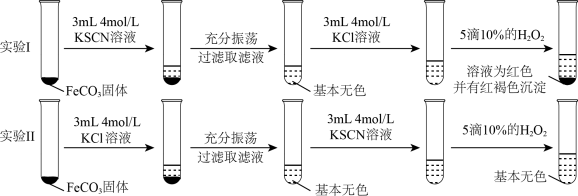
A.实验Ⅱ中,KCl溶液能促进 溶解 溶解 | B.相同浓度下,KSCN溶液盐效应大于KCl溶液 |
| C.滤液中+2价铁离子总浓度:实验Ⅰ=实验Ⅱ | D.实验表明, 和 和 不能形成络离子 不能形成络离子 |
您最近一年使用:0次
2023-01-03更新
|
923次组卷
|
5卷引用:湖南省长沙市长郡中学2022-2023学年高三上学期月考(四)化学试题
湖南省长沙市长郡中学2022-2023学年高三上学期月考(四)化学试题(已下线)专题11 化学实验基础(练)-2023年高考化学二轮复习讲练测(新高考专用)湖南省醴陵市第一中学2023届高三第六次月考化学试题山东省沂水县第一中学2022-2023学年高一上学期期末考试化学试题章末检测卷(三) 物质的性质与转化
6 . 某化学课外小组在制备Fe(OH)2实验过程中观察到生成的白色沉淀迅速变为灰绿色,一段时间后变为红褐色,该小组同学对产生灰绿色沉淀的原因,进行实验探究。
Ⅰ.乙同学查阅资料得知,Fe(OH)2沉淀具有较强的吸附性,猜测灰绿色可能是Fe(OH)2吸附Fe2+引起的,设计并完成了实验3~实验5。
(1)依据乙同学的猜测,实验4中沉淀无灰绿色的原因为___________ 。
(2)该小组同学依据实验5的实验现象,间接证明了乙同学猜测的正确性,则实验5的实验现象可能为___________ 。
II.该小组同学再次查阅资料得知当沉淀形成时,若得到的沉淀单一,则沉淀结构均匀,也紧密;若有杂质固体存在时,得到的沉淀便不够紧密,与溶液的接触面积会更大。
(3)当溶液中存在Fe3+或溶解较多O2时,白色沉淀更容易变成灰绿色的原因为___________ 。
(4)该小组同学根据上述实验得出结论:制备Fe(OH)2时能较长时间观察到白色沉淀的适宜条件和操作有___________ 、___________ 。
Ⅰ.乙同学查阅资料得知,Fe(OH)2沉淀具有较强的吸附性,猜测灰绿色可能是Fe(OH)2吸附Fe2+引起的,设计并完成了实验3~实验5。
| 编号 | 实验操作 | 实验现象 |
| 实验3 | 向10mL4mol·L-1NaOH溶液中逐滴加入0.1mol·L-1FeSO4溶液(两溶液中均先加几滴维生素C溶液) | 液面上方产生白色沉淀(带有较多灰绿色)。沉淀下沉后,部分灰绿色沉淀变为白色 |
| 实验4 | 向10mL8mol·L-1NaOH溶液中逐滴加入0.1mol·L-1FeSO4溶液(两溶液中均先加几滴维生素C溶液) | 液面上方产生白色沉淀(无灰绿色)。沉淀下沉后,仍为白色 |
| 实验5 | 取实验4中白色沉淀,洗净后放在潮湿的空气中 |
(2)该小组同学依据实验5的实验现象,间接证明了乙同学猜测的正确性,则实验5的实验现象可能为
II.该小组同学再次查阅资料得知当沉淀形成时,若得到的沉淀单一,则沉淀结构均匀,也紧密;若有杂质固体存在时,得到的沉淀便不够紧密,与溶液的接触面积会更大。
(3)当溶液中存在Fe3+或溶解较多O2时,白色沉淀更容易变成灰绿色的原因为
(4)该小组同学根据上述实验得出结论:制备Fe(OH)2时能较长时间观察到白色沉淀的适宜条件和操作有
您最近一年使用:0次
7 . 利用下图装置可制备 沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是
沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是
 沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是
沉淀,且能较长时间保存该物质而不变质。下列说法不正确的是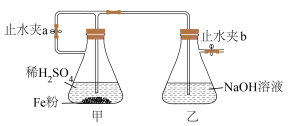
| A.实验开始时,打开止水夹a和止水夹b |
| B.关闭止水夹a,打开止水夹b,甲中溶液可流入乙中 |
C. 能较长时间保存是因 能较长时间保存是因 无氧化性 无氧化性 |
| D.抽滤瓶甲中的稀硫酸可以用稀硝酸代替 |
您最近一年使用:0次
名校
8 . 油画的白色燃料中曾含二价铅盐,二价铅盐经过长时间空气(含有微量H2S)的侵蚀,生成PbS而变黑。可用一定量的H2O2溶液擦铁修复。完成下列填空:
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式___________ 。
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为___________ 。当PbSO4和CH3COONH4恰好完全反应时,溶液显___________ 性(选填“酸性”、“中性”或“碱性”)。
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为___________ ;该物质在空气中很快变为红褐色,原因是___________ 。
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为___________ 。从开始通SO2至饱和,再继续通一段时间,整个过程中c(H+)的变化情况为___________ 。
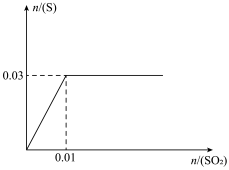
(1)H2O2与PbS反应生成PbSO4的和H2O,写出该反应的化学方程式
(2)在PbSO4的悬浊液中滴加一定量的CH3COONH4溶液,发生复分解反应,溶液变为澄清,有弱电解质生成,该弱电解质的化学式为
(3)H2S为二元弱酸,向Na2S溶液中加入FeSO4溶液,生成FeS沉淀,还可能生成白色沉淀,其化学式为
(4)向200mLH2S溶液中缓慢通入SO2,发生反应2H2S+SO2→3S
 +2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
+2H2O,生成S的物质的量与通入SO2的物质的量的关系如图(溶液体积变化忽略不计),由此可知原溶液中H2S的物质的量浓度为
您最近一年使用:0次
名校
9 .  的制备实验是实验研究的热点,某化学学习小组设计了如图所示装置(夹持仪器省略)制备氢氧化亚铁。
的制备实验是实验研究的热点,某化学学习小组设计了如图所示装置(夹持仪器省略)制备氢氧化亚铁。
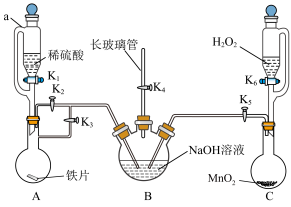
实验步骤如下:
Ⅰ.检查装置气密性后,关闭K2、K5、K6,打开K1、K3、K4使装置A中产生的气体进入装置B中,排尽B中空气。
Ⅱ.待B中空气排尽后,关闭K3,打开K2,将A中溶液压入B中并观察现象。
Ⅲ.关闭K1、K2,打开K5、K6,使C中气体通入B中并观察现象。
回答下列问题:
(1)仪器a的名称是_____ ,B中长玻璃管的作用是_____ 。
(2)装置A中金属离子的检验方法是_____
(3)步骤Ⅲ装置B中的现象是_____ ,其发生反应的化学方程式为_____ 。
(4)在FeSO4溶液中加入 固体可制备摩尔盐晶体[
固体可制备摩尔盐晶体[ ](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
①从摩尔盐水溶液中提取 晶体的具体操作是
晶体的具体操作是_____ 。
②为了测定产品的纯度,称取10g产品溶于50mL水中,配制成250mL溶液,用浓度为 的酸性KMnO4溶液滴定,每次所取待测液体积均为25.00mL。实验结果记录如下:
的酸性KMnO4溶液滴定,每次所取待测液体积均为25.00mL。实验结果记录如下:
通过实验数据计算该产品纯度为_____ ,上表中第一次实验中记录数据明显大于后两次,其原因可能是_____ 。
A.第一次滴定前滴定管尖嘴有气泡
B.第一次实验结束时俯视刻度线读取酸性高锰酸钾溶液的体积
C.第一次滴定用的锥形瓶用待测液润洗过
D.第一次实验装高锰酸钾的滴定管清洗后没有润洗
 的制备实验是实验研究的热点,某化学学习小组设计了如图所示装置(夹持仪器省略)制备氢氧化亚铁。
的制备实验是实验研究的热点,某化学学习小组设计了如图所示装置(夹持仪器省略)制备氢氧化亚铁。
实验步骤如下:
Ⅰ.检查装置气密性后,关闭K2、K5、K6,打开K1、K3、K4使装置A中产生的气体进入装置B中,排尽B中空气。
Ⅱ.待B中空气排尽后,关闭K3,打开K2,将A中溶液压入B中并观察现象。
Ⅲ.关闭K1、K2,打开K5、K6,使C中气体通入B中并观察现象。
回答下列问题:
(1)仪器a的名称是
(2)装置A中金属离子的检验方法是
(3)步骤Ⅲ装置B中的现象是
(4)在FeSO4溶液中加入
 固体可制备摩尔盐晶体[
固体可制备摩尔盐晶体[ ](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。
](相对分子质量392),该晶体比一般亚铁盐稳定,不易被氧化,易溶于水,不溶于乙醇。①从摩尔盐水溶液中提取
 晶体的具体操作是
晶体的具体操作是②为了测定产品的纯度,称取10g产品溶于50mL水中,配制成250mL溶液,用浓度为
 的酸性KMnO4溶液滴定,每次所取待测液体积均为25.00mL。实验结果记录如下:
的酸性KMnO4溶液滴定,每次所取待测液体积均为25.00mL。实验结果记录如下:| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
A.第一次滴定前滴定管尖嘴有气泡
B.第一次实验结束时俯视刻度线读取酸性高锰酸钾溶液的体积
C.第一次滴定用的锥形瓶用待测液润洗过
D.第一次实验装高锰酸钾的滴定管清洗后没有润洗
您最近一年使用:0次
名校
解题方法
10 . 下列说法不正确的是
| A.既有单质参加又有单质生成的反应不一定是氧化还原反应 |
| B.焰色反应是物理变化,实验中用稀硫酸洗铂丝或光洁无锈的铁丝 |
| C.铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物 |
| D.FeCl2、NaHCO3、Fe(OH)3都能通过用化合反应制得 |
您最近一年使用:0次



