1 . 实验室以(NH4)2CO3和Cu(OH)2为原料制备高纯Cu2(OH)2CO3的方法如下:___________ (答两点)。
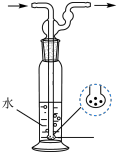
(2)“蒸氨”在如图所示的实验装置中进行。___________ 。
②实验采用三个盛有水的洗气瓶吸收尾气的目的为___________ ;与上图所示洗气瓶相比,采用三个如图所示装置的优点为___________ 。___________ 。
(3)已知:①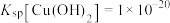 ;
;
②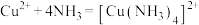
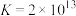 ;
;
③沉淀速率过快时,Cu(OH)2絮状沉淀易裹挟杂质。
以CuSO4∙5H2O固体为原料,补充完整制备纯净Cu(OH)2的实验方案:取一定质量的CuSO4∙5H2O固体分批加入蒸馏水中,搅拌至完全溶解,___________ ,低温烘干。(须使用的试剂:浓氨水、1mol∙L-1 NaOH溶液、0.1mol∙L-1 BaCl2溶液、蒸馏水)
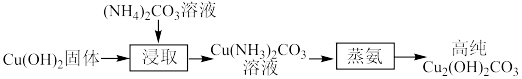
(2)“蒸氨”在如图所示的实验装置中进行。

②实验采用三个盛有水的洗气瓶吸收尾气的目的为
(3)已知:①
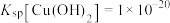 ;
;②
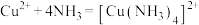
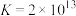 ;
;③沉淀速率过快时,Cu(OH)2絮状沉淀易裹挟杂质。
以CuSO4∙5H2O固体为原料,补充完整制备纯净Cu(OH)2的实验方案:取一定质量的CuSO4∙5H2O固体分批加入蒸馏水中,搅拌至完全溶解,
您最近半年使用:0次
名校
2 . 乙研究小组为了利用稀硫酸制备 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:
①
②……
(1)反应②的离子方程式 为______________ 。
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是__________ 。
取 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。 时,固体的成分为
时,固体的成分为________ (写出计算步骤 )。
(4)当剩余固体为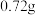 时,加热的温度不能低于
时,加热的温度不能低于_____ ℃,如果此时产生的气体中含有 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式________ 。
 ,进行了如图所示的实验设计。
,进行了如图所示的实验设计。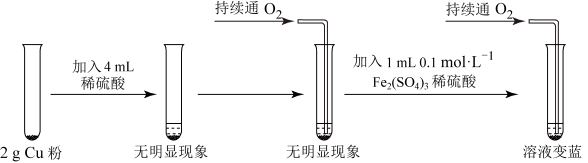
 能加快生成
能加快生成 的反应速率,发挥作用的原理可表述为:
的反应速率,发挥作用的原理可表述为:①

②……
(1)反应②的
(2)某小组通过向铜和稀硫酸的混合物中加入过氧化氢的方法制备硫酸铜,但是在实际操作时,发现所消耗的
 的量往往会大于理论值,原因是
的量往往会大于理论值,原因是取
 晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。
晶体隔绝空气加热,剩余固体的质量随温度的变化如图所示。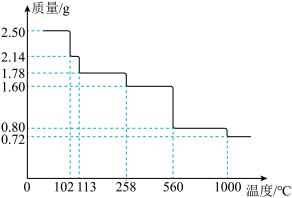
 时,固体的成分为
时,固体的成分为(4)当剩余固体为
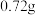 时,加热的温度不能低于
时,加热的温度不能低于 ,请写出
,请写出 受热分解的化学方程式
受热分解的化学方程式
您最近半年使用:0次
名校
3 . 硝酸铜是一种重要的化工原料,可由工业含铜废料制备,含铜废料的主要成分为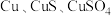 等,制备流程如图所示:
等,制备流程如图所示:
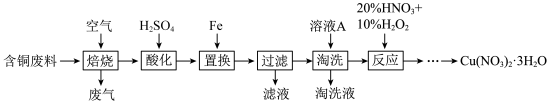
回答下列问题:
(1)焙烧时, 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“淘洗”所用的溶液A可以是___________ 。(填标号)。
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。
①理论上反应所消耗的 和
和 的物质的量之比为
的物质的量之比为___________ 。
②若不加10%的 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为___________ 。
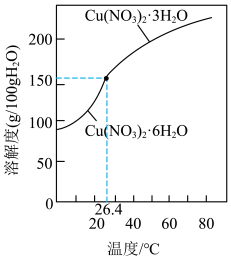
③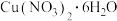 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是___________ 。
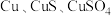 等,制备流程如图所示:
等,制备流程如图所示:
回答下列问题:
(1)焙烧时,
 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)“淘洗”所用的溶液A可以是
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的
 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。①理论上反应所消耗的
 和
和 的物质的量之比为
的物质的量之比为②若不加10%的
 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为③
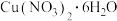 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是
您最近半年使用:0次
4 . 第四周期过渡元素形成的化合物具有重要作用。黄铜( )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。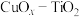 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: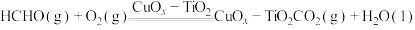 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、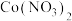 、
、 和
和 反应制备的配合物
反应制备的配合物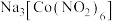 可应用于
可应用于 的鉴定。
的鉴定。
下列化学反应表示正确的是
 )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。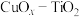 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: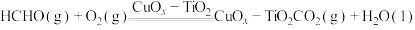 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、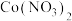 、
、 和
和 反应制备的配合物
反应制备的配合物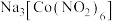 可应用于
可应用于 的鉴定。
的鉴定。下列化学反应表示正确的是
A. 与稀硫酸反应: 与稀硫酸反应: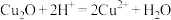 |
B. 溶液和 溶液和 反应: 反应: |
C. 与足量盐酸反应: 与足量盐酸反应: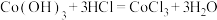 |
D.制备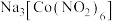 的反应: 的反应: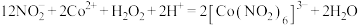 |
您最近半年使用:0次
名校
5 . 硫酸铜晶体、硫酸四氨合铜晶体 均是常见的含铜化合物,可以由铜或含铜矿物制取得到。
均是常见的含铜化合物,可以由铜或含铜矿物制取得到。
(1)兴趣小组用图所示装置进行硫酸铜的制备,二连球的作用是鼓入空气。CuCl是白色难溶于水的固体, 是墨绿色难溶于水的固体。
是墨绿色难溶于水的固体。
①三颈烧瓶中主要涉及三个反应,写出反应Ⅱ的化学方程式。
反应Ⅰ.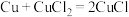
反应Ⅱ.___________
反应Ⅲ.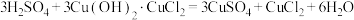
②按如图所示装置连接并加好试剂后,进行如下操作:
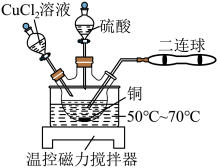
操作1:向三颈烧瓶中加入一定量的 溶液,充分搅拌至有大量白色固体生成;
溶液,充分搅拌至有大量白色固体生成;
操作2:鼓入空气,待有大量墨绿色固体生成后,滴加稀硫酸至墨绿色固体完全溶解;
重复操作2至铜完全溶解。
操作1中加入 溶液不能过多的原因是
溶液不能过多的原因是___________ ,也不能过少的原因是___________ 。
③Cu和浓硫酸直接反应也可制取硫酸铜,与上述实验方案相比,Cu和浓硫酸直接反应制取硫酸铜的缺点有___________ 和___________ 。
(2)黄铜矿(主要成分为 )可用于制取
)可用于制取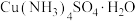 晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有
晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有 、
、 和
和 。设计由浸出液制取
。设计由浸出液制取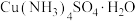 晶体的实验方案:
晶体的实验方案:___________ ,得到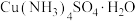 晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、
晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、 溶液、3%
溶液、3% 溶液、无水乙醇)
溶液、无水乙醇)
已知Ⅰ.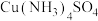 加热时易失去
加热时易失去
Ⅱ.实验中金属离子开始沉淀为氢氧化物及沉淀完全的pH如下表所示:
 均是常见的含铜化合物,可以由铜或含铜矿物制取得到。
均是常见的含铜化合物,可以由铜或含铜矿物制取得到。(1)兴趣小组用图所示装置进行硫酸铜的制备,二连球的作用是鼓入空气。CuCl是白色难溶于水的固体,
 是墨绿色难溶于水的固体。
是墨绿色难溶于水的固体。①三颈烧瓶中主要涉及三个反应,写出反应Ⅱ的化学方程式。
反应Ⅰ.
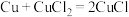
反应Ⅱ.
反应Ⅲ.
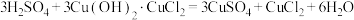
②按如图所示装置连接并加好试剂后,进行如下操作:

操作1:向三颈烧瓶中加入一定量的
 溶液,充分搅拌至有大量白色固体生成;
溶液,充分搅拌至有大量白色固体生成;操作2:鼓入空气,待有大量墨绿色固体生成后,滴加稀硫酸至墨绿色固体完全溶解;
重复操作2至铜完全溶解。
操作1中加入
 溶液不能过多的原因是
溶液不能过多的原因是③Cu和浓硫酸直接反应也可制取硫酸铜,与上述实验方案相比,Cu和浓硫酸直接反应制取硫酸铜的缺点有
(2)黄铜矿(主要成分为
 )可用于制取
)可用于制取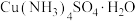 晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有
晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有 、
、 和
和 。设计由浸出液制取
。设计由浸出液制取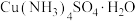 晶体的实验方案:
晶体的实验方案: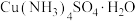 晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、
晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、 溶液、3%
溶液、3% 溶液、无水乙醇)
溶液、无水乙醇)已知Ⅰ.
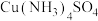 加热时易失去
加热时易失去
Ⅱ.实验中金属离子开始沉淀为氢氧化物及沉淀完全的pH如下表所示:
 |  |  | |
| 开始沉淀的pH | 1.9 | 4.7 | 5.8 |
| 沉淀完全的pH | 3.2 | 6.7 | 9.0 |
您最近半年使用:0次
2024-02-24更新
|
301次组卷
|
2卷引用:江苏省 徐州市第七中学2023-2024学年高三上学期12月月考化学试题
6 . 某工厂的固体废渣中主要含Cu和CuO,还含有少量Cu2O和SiO2。利用该固体废渣制取Cu(NO3)2溶液的工艺流程如图所示:
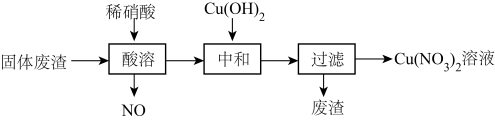
已知:①Cu+在酸性溶液中不稳定,会转变成Cu和Cu2+。
②SiO2是酸性氧化物,难于水和酸。
(1)写出Cu2O与稀硝酸反应的离子反应方程式为___________ ;
(2)酸溶时,反应温度不宜超过70℃,其主要原因是___________ ;
(3)将酸溶步骤排放的NO循环利用既环保又能提高产量,具体操作流程是___________ ;
(4)酸溶试剂改用绿色氧化剂(10%H2O2和20%稀硝酸的混合液),基本无氮氧化物排放,写出废渣中Cu与绿色氧化剂反应的离子反应方程式___________ ;
(5)中和试剂选择Cu(OH)2,若改为NaOH,缺点是___________ ;
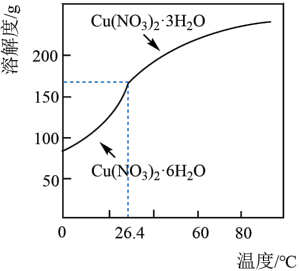
(6)以某工业废水(主要含Cu2+、Na+、SO )为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
)为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入___________ ,洗涤,干燥。(须使用的试剂有:蒸馏水、1mol/L NaOH溶液、1mol/LHNO3溶液;Cu(NO3)2的溶解度曲线如图所示。)

已知:①Cu+在酸性溶液中不稳定,会转变成Cu和Cu2+。
②SiO2是酸性氧化物,难于水和酸。
(1)写出Cu2O与稀硝酸反应的离子反应方程式为
(2)酸溶时,反应温度不宜超过70℃,其主要原因是
(3)将酸溶步骤排放的NO循环利用既环保又能提高产量,具体操作流程是
(4)酸溶试剂改用绿色氧化剂(10%H2O2和20%稀硝酸的混合液),基本无氮氧化物排放,写出废渣中Cu与绿色氧化剂反应的离子反应方程式
(5)中和试剂选择Cu(OH)2,若改为NaOH,缺点是
(6)以某工业废水(主要含Cu2+、Na+、SO
 )为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
)为原料,设计制取Cu(NO3)2·3H2O晶体的实验方案:向工业废水中加入
您最近半年使用:0次
解题方法
7 . 铜的氯化物是重要的化工原料,常用作有机合成催化剂。实验室用粗铜(含杂质Fe)制备氯化亚铜、氯化铜晶体的流程如下:
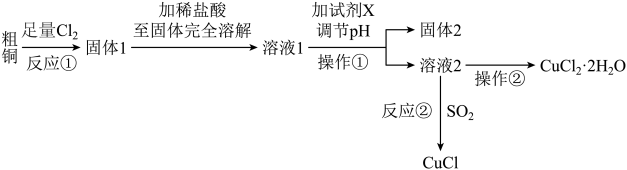
下列说法错误的是

下列说法错误的是
A.反应②的离子方程式为2Cu2++SO2+2H2O+2Cl-=2CuCl↓+SO +4H+ +4H+ |
| B.检验溶液2中的杂质离子是否除尽可以选用KSCN溶液 |
| C.试剂X可能是CuO,操作②中结晶时需要通入HCl气体 |
| D.固体1和固体2中Fe元素的价态不相同 |
您最近半年使用:0次
名校
解题方法
8 . 取一定量胆矾晶体(CuSO4·5H2O)加热分解,固体残留率( ) 随温度的变化如图所示:
) 随温度的变化如图所示:
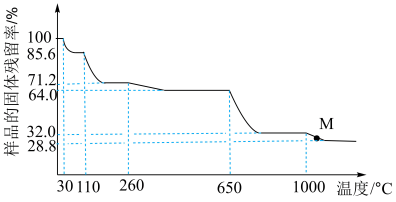
下列说法中不正确的是
 ) 随温度的变化如图所示:
) 随温度的变化如图所示:
下列说法中不正确的是
| A.110°C 时的晶体化学式 CuSO4·3H2O |
B.260°C~ 650°C 过程中的反应方程式为CuSO4·H2O CuSO4+H2O CuSO4+H2O |
| C.已知 650°C 加热至 1000°C ,产物为一种固体与一种气体, 则气体为SO2 |
| D.M 点所得固体是 CuO 与 Cu2O 的混合物 |
您最近半年使用:0次
名校
9 . 秦始皇兵马俑是世界文化遗产,兵马俑表面的彩绘体现了当时彩绘工艺和颜料制作工艺水平,具有极高的历史价值和艺术价值。下列对于兵马俑使用颜料的主要成分与其类别的对应关系正确的是


| 选项 | A | B | C | D |
| 颜色 | 绿色 | 棕红色 | 大红色 | 黑色 |
| 主要成分 | 石绿 | 赭石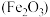 | 朱砂( ) ) | 炭黑(C) |
| 类别 | 碱 | 酸性氧化物 | 电解质 | 有机物 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-07-16更新
|
312次组卷
|
3卷引用:江苏省无锡市第一中学2023-2024学年高一上学期期末考试化学试题
名校
10 . 回答下列问题:
(1) 可用作有机合成的催化剂。
可用作有机合成的催化剂。 是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
次磷酸 是一种强还原剂,将它加入
是一种强还原剂,将它加入 水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生
水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生 。写出生成CuH的化学方程式:
。写出生成CuH的化学方程式:___________ 。
(2)某同学利用如下图所示装置,测定高炉煤气中CO、 、
、 和
和 的百分组成。
的百分组成。
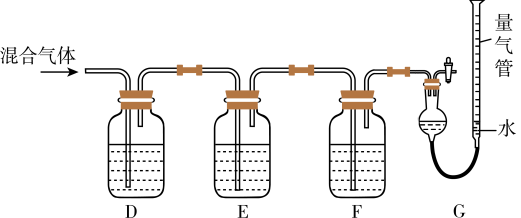
已知:i. 的盐酸溶液能吸收CO形成
的盐酸溶液能吸收CO形成 。
。
ii.保险粉 和KOH的混合溶液能吸收氧气。
和KOH的混合溶液能吸收氧气。
请回答以下问题:
①G中测出的是___________ (填物质的化学式)的体积。
②F洗气瓶中宜盛放的试剂是___________ 。
(3)工业上可以在酸性介质中用 氧化浸出黄铜矿
氧化浸出黄铜矿 。
。
① 反应后转化为
反应后转化为 、
、 、
、 。将
。将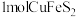 完全转化,理论上所需
完全转化,理论上所需 的物质的量为
的物质的量为___________ 。
②浸出过程中发现, 的反应实际用量远大于理论用量,原因是
的反应实际用量远大于理论用量,原因是___________ 。
③若浸出过程中,溶液中含有少量 ,则会析出黄钠铁矾
,则会析出黄钠铁矾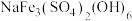 沉淀。写出
沉淀。写出 转化为黄钠铁矾沉淀的离子方程式:
转化为黄钠铁矾沉淀的离子方程式:___________ 。
(1)
 可用作有机合成的催化剂。
可用作有机合成的催化剂。 是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。
是一种难溶于水和乙醇的白色固体,露置于潮湿空气中易被氧化。次磷酸
 是一种强还原剂,将它加入
是一种强还原剂,将它加入 水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生
水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH,次磷酸转化为磷酸。待CuH生成后将HCl气体通入,可产生 。写出生成CuH的化学方程式:
。写出生成CuH的化学方程式:(2)某同学利用如下图所示装置,测定高炉煤气中CO、
 、
、 和
和 的百分组成。
的百分组成。
已知:i.
 的盐酸溶液能吸收CO形成
的盐酸溶液能吸收CO形成 。
。ii.保险粉
 和KOH的混合溶液能吸收氧气。
和KOH的混合溶液能吸收氧气。请回答以下问题:
①G中测出的是
②F洗气瓶中宜盛放的试剂是
(3)工业上可以在酸性介质中用
 氧化浸出黄铜矿
氧化浸出黄铜矿 。
。①
 反应后转化为
反应后转化为 、
、 、
、 。将
。将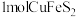 完全转化,理论上所需
完全转化,理论上所需 的物质的量为
的物质的量为②浸出过程中发现,
 的反应实际用量远大于理论用量,原因是
的反应实际用量远大于理论用量,原因是③若浸出过程中,溶液中含有少量
 ,则会析出黄钠铁矾
,则会析出黄钠铁矾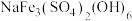 沉淀。写出
沉淀。写出 转化为黄钠铁矾沉淀的离子方程式:
转化为黄钠铁矾沉淀的离子方程式:
您最近半年使用:0次



