名校
1 . 硝酸铜是一种重要的化工原料,可由工业含铜废料制备,含铜废料的主要成分为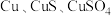 等,制备流程如图所示:
等,制备流程如图所示:
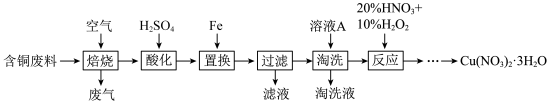
回答下列问题:
(1)焙烧时, 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“淘洗”所用的溶液A可以是___________ 。(填标号)。
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。
①理论上反应所消耗的 和
和 的物质的量之比为
的物质的量之比为___________ 。
②若不加10%的 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为___________ 。
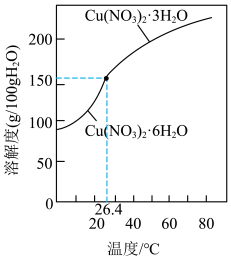
③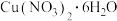 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是___________ 。
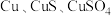 等,制备流程如图所示:
等,制备流程如图所示:
回答下列问题:
(1)焙烧时,
 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)“淘洗”所用的溶液A可以是
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的
 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。①理论上反应所消耗的
 和
和 的物质的量之比为
的物质的量之比为②若不加10%的
 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为③
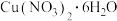 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是
您最近半年使用:0次
2 . 第四周期过渡元素形成的化合物具有重要作用。黄铜( )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。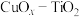 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: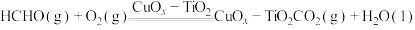 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、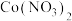 、
、 和
和 反应制备的配合物
反应制备的配合物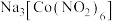 可应用于
可应用于 的鉴定。
的鉴定。
下列化学反应表示正确的是
 )用
)用 溶液浸泡后生成单质硫,所得
溶液浸泡后生成单质硫,所得 溶液可用于制取纳米
溶液可用于制取纳米 ,
, 能与酸发生反应。
能与酸发生反应。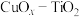 可用于低温下催化氧化HCHO:
可用于低温下催化氧化HCHO: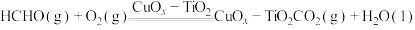 。
。 具有强氧化性,可与盐酸反应生成氯气。由
具有强氧化性,可与盐酸反应生成氯气。由 、
、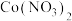 、
、 和
和 反应制备的配合物
反应制备的配合物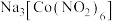 可应用于
可应用于 的鉴定。
的鉴定。下列化学反应表示正确的是
A. 与稀硫酸反应: 与稀硫酸反应: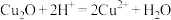 |
B. 溶液和 溶液和 反应: 反应: |
C. 与足量盐酸反应: 与足量盐酸反应: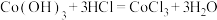 |
D.制备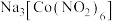 的反应: 的反应: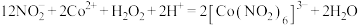 |
您最近半年使用:0次
名校
3 . 硫酸铜晶体、硫酸四氨合铜晶体 均是常见的含铜化合物,可以由铜或含铜矿物制取得到。
均是常见的含铜化合物,可以由铜或含铜矿物制取得到。
(1)兴趣小组用图所示装置进行硫酸铜的制备,二连球的作用是鼓入空气。CuCl是白色难溶于水的固体, 是墨绿色难溶于水的固体。
是墨绿色难溶于水的固体。
①三颈烧瓶中主要涉及三个反应,写出反应Ⅱ的化学方程式。
反应Ⅰ.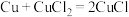
反应Ⅱ.___________
反应Ⅲ.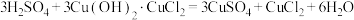
②按如图所示装置连接并加好试剂后,进行如下操作:
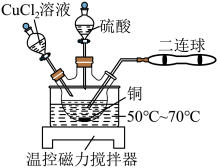
操作1:向三颈烧瓶中加入一定量的 溶液,充分搅拌至有大量白色固体生成;
溶液,充分搅拌至有大量白色固体生成;
操作2:鼓入空气,待有大量墨绿色固体生成后,滴加稀硫酸至墨绿色固体完全溶解;
重复操作2至铜完全溶解。
操作1中加入 溶液不能过多的原因是
溶液不能过多的原因是___________ ,也不能过少的原因是___________ 。
③Cu和浓硫酸直接反应也可制取硫酸铜,与上述实验方案相比,Cu和浓硫酸直接反应制取硫酸铜的缺点有___________ 和___________ 。
(2)黄铜矿(主要成分为 )可用于制取
)可用于制取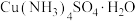 晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有
晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有 、
、 和
和 。设计由浸出液制取
。设计由浸出液制取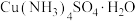 晶体的实验方案:
晶体的实验方案:___________ ,得到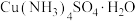 晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、
晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、 溶液、3%
溶液、3% 溶液、无水乙醇)
溶液、无水乙醇)
已知Ⅰ.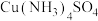 加热时易失去
加热时易失去
Ⅱ.实验中金属离子开始沉淀为氢氧化物及沉淀完全的pH如下表所示:
 均是常见的含铜化合物,可以由铜或含铜矿物制取得到。
均是常见的含铜化合物,可以由铜或含铜矿物制取得到。(1)兴趣小组用图所示装置进行硫酸铜的制备,二连球的作用是鼓入空气。CuCl是白色难溶于水的固体,
 是墨绿色难溶于水的固体。
是墨绿色难溶于水的固体。①三颈烧瓶中主要涉及三个反应,写出反应Ⅱ的化学方程式。
反应Ⅰ.
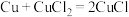
反应Ⅱ.
反应Ⅲ.
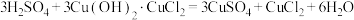
②按如图所示装置连接并加好试剂后,进行如下操作:

操作1:向三颈烧瓶中加入一定量的
 溶液,充分搅拌至有大量白色固体生成;
溶液,充分搅拌至有大量白色固体生成;操作2:鼓入空气,待有大量墨绿色固体生成后,滴加稀硫酸至墨绿色固体完全溶解;
重复操作2至铜完全溶解。
操作1中加入
 溶液不能过多的原因是
溶液不能过多的原因是③Cu和浓硫酸直接反应也可制取硫酸铜,与上述实验方案相比,Cu和浓硫酸直接反应制取硫酸铜的缺点有
(2)黄铜矿(主要成分为
 )可用于制取
)可用于制取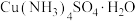 晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有
晶体。将黄铜矿在有氧条件下用硫酸浸出,所得浸出液中含有 、
、 和
和 。设计由浸出液制取
。设计由浸出液制取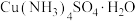 晶体的实验方案:
晶体的实验方案: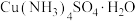 晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、
晶体。(实验中须使用的试剂有:1 mol⋅L-1氨水、 溶液、3%
溶液、3% 溶液、无水乙醇)
溶液、无水乙醇)已知Ⅰ.
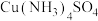 加热时易失去
加热时易失去
Ⅱ.实验中金属离子开始沉淀为氢氧化物及沉淀完全的pH如下表所示:
 |  |  | |
| 开始沉淀的pH | 1.9 | 4.7 | 5.8 |
| 沉淀完全的pH | 3.2 | 6.7 | 9.0 |
您最近半年使用:0次
2024-02-24更新
|
282次组卷
|
2卷引用:江苏省 徐州市第七中学2023-2024学年高三上学期12月月考化学试题
4 . 废弃的锂离子电池中含有多种金属元素,需回收处理。柠檬酸因具有酸性和较好的络合性,可用于浸出金属离子并得到柠檬酸浸出液。下图是某小组研究从柠檬酸浸出液中分离出铜并制备碱式碳酸铜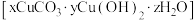 的制备流程。
的制备流程。

(1)在“调pH分离铜”的步骤中,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小于理论分析结果,可能的原因为___________ 。
(2)在“还原法沉铜”的步骤中,利用抗坏血酸(C6H8O6)能有效的将Cu(Ⅱ)还原成金属Cu。抗坏血酸(C6H8O6)易被氧化为脱氢抗坏血酸(C6H6O6);且受热易分解。
①抗坏血酸还原 的离子方程式为
的离子方程式为___________ 。
②某实验小组研究了相同条件下温度对Cu沉淀率的影响。从如图可以看出,随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降,下降可能的原因是___________ 。

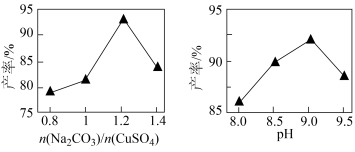
(3)将所得铜粉制备为 溶液后再制备碱式碳酸铜。已知碱式碳酸铜的产率随起始:
溶液后再制备碱式碳酸铜。已知碱式碳酸铜的产率随起始: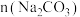 与
与 的比值和溶液pH的关系如图所示。
的比值和溶液pH的关系如图所示。
①补充完整由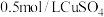 溶液制取碱式碳酸铜的实验方案:向烧杯中加入
溶液制取碱式碳酸铜的实验方案:向烧杯中加入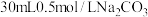 溶液,将烧杯置于70℃的水浴中,
溶液,将烧杯置于70℃的水浴中,___________ ,低温烘干,得到碱式碳酸铜(实验中可选用的试剂或仪器: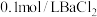 溶液、0.1mol/LNaOH溶液、0.1mol/L盐酸、pH计)。
溶液、0.1mol/LNaOH溶液、0.1mol/L盐酸、pH计)。
②实验时发现,若反应时溶液pH过大,所得碱式碳酸铜的产率偏低,但产品中Cu元素含量偏大,原因是___________ 。
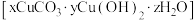 的制备流程。
的制备流程。
(1)在“调pH分离铜”的步骤中,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小于理论分析结果,可能的原因为
(2)在“还原法沉铜”的步骤中,利用抗坏血酸(C6H8O6)能有效的将Cu(Ⅱ)还原成金属Cu。抗坏血酸(C6H8O6)易被氧化为脱氢抗坏血酸(C6H6O6);且受热易分解。
①抗坏血酸还原
 的离子方程式为
的离子方程式为②某实验小组研究了相同条件下温度对Cu沉淀率的影响。从如图可以看出,随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降,下降可能的原因是

(3)将所得铜粉制备为
 溶液后再制备碱式碳酸铜。已知碱式碳酸铜的产率随起始:
溶液后再制备碱式碳酸铜。已知碱式碳酸铜的产率随起始: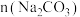 与
与 的比值和溶液pH的关系如图所示。
的比值和溶液pH的关系如图所示。
①补充完整由
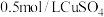 溶液制取碱式碳酸铜的实验方案:向烧杯中加入
溶液制取碱式碳酸铜的实验方案:向烧杯中加入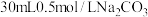 溶液,将烧杯置于70℃的水浴中,
溶液,将烧杯置于70℃的水浴中,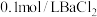 溶液、0.1mol/LNaOH溶液、0.1mol/L盐酸、pH计)。
溶液、0.1mol/LNaOH溶液、0.1mol/L盐酸、pH计)。②实验时发现,若反应时溶液pH过大,所得碱式碳酸铜的产率偏低,但产品中Cu元素含量偏大,原因是
您最近半年使用:0次
5 . 名画《千里江山图》用到了一种矿物颜料石青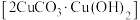 。下列说法
。下列说法不 正确的是
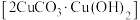 。下列说法
。下列说法| A.石青难溶于水 |
| B.石青结构中只含有离子键 |
| C.石青充分加热能得到种黑色固体 |
D.石青与盐酸反应的化学方程式为: |
您最近半年使用:0次
名校
解题方法
6 . Cu2S在高温下与O2反应转化为Cu2O和SO2,生成的Cu2O与Cu2S进一步反应得到Cu和SO2。Cu2O在酸性溶液中会转化为Cu和 ;Cu在O2存在下能与氨水反应生成
;Cu在O2存在下能与氨水反应生成 ;CuSO4可用于水体的净化。下列物质的结构与性质或物质的性质与用途具有对应关系的是
;CuSO4可用于水体的净化。下列物质的结构与性质或物质的性质与用途具有对应关系的是
 ;Cu在O2存在下能与氨水反应生成
;Cu在O2存在下能与氨水反应生成 ;CuSO4可用于水体的净化。下列物质的结构与性质或物质的性质与用途具有对应关系的是
;CuSO4可用于水体的净化。下列物质的结构与性质或物质的性质与用途具有对应关系的是| A.Cu2S熔点高,可用作电池的负极材料 |
| B. SO2具有还原性,可用作纸浆的漂白剂 |
| C. NH3存在孤电子对,可与Cu+形成配位键 |
D. 溶液显酸性,可用于游泳池内水的消毒 溶液显酸性,可用于游泳池内水的消毒 |
您最近半年使用:0次
名校
解题方法
7 . 俗名往往反映了物质的组成、性质或用途。下列对物质俗名的理解不正确的是
A.纯碱: 去油污 去油污 | B.胆矾: 净水 净水 |
C.酒精: 消毒杀菌 消毒杀菌 | D.葡萄糖: 营养成分 营养成分 |
您最近半年使用:0次
2024-01-12更新
|
198次组卷
|
2卷引用: 江苏省盐城市2023-2024学年高二学业水平合格性考试模拟预测化学试题
8 . 部分含 或含
或含 物质的分类与相应化合价关系如图所示。下列推断合理的是
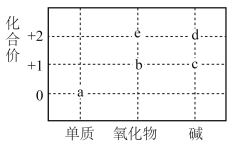
物质的分类与相应化合价关系如图所示。下列推断合理的是
 或含
或含 物质的分类与相应化合价关系如图所示。下列推断合理的是
物质的分类与相应化合价关系如图所示。下列推断合理的是
A. 与 与 溶液的反应: 溶液的反应: |
B.能与 反应生成c的物质只有b 反应生成c的物质只有b |
C.存在 的转化 的转化 |
D.若b能与 反应生成c和 反应生成c和 ,则b是碱性氧化物 ,则b是碱性氧化物 |
您最近半年使用:0次
名校
9 . 冶炼铜时可使 在高温下与
在高温下与 反应转化为
反应转化为 ,生成的
,生成的 与
与 进一步反应得到
进一步反应得到 。
。 在酸性溶液中会转化为
在酸性溶液中会转化为 和
和 ;
; 能被浓硝酸氧化为
能被浓硝酸氧化为 。
。 在
在 存在下能与氨水反应生成
存在下能与氨水反应生成 。则下列化学反应表示正确的是
。则下列化学反应表示正确的是
 在高温下与
在高温下与 反应转化为
反应转化为 ,生成的
,生成的 与
与 进一步反应得到
进一步反应得到 。
。 在酸性溶液中会转化为
在酸性溶液中会转化为 和
和 ;
; 能被浓硝酸氧化为
能被浓硝酸氧化为 。
。 在
在 存在下能与氨水反应生成
存在下能与氨水反应生成 。则下列化学反应表示正确的是
。则下列化学反应表示正确的是A. 在高温下与 在高温下与 反应: 反应: |
B. 与浓硝酸反应: 与浓硝酸反应: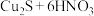 (浓) (浓)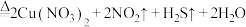 |
C. 溶于稀硫酸: 溶于稀硫酸: |
D. 在 在 存在下与氨水反应: 存在下与氨水反应: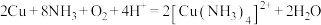 |
您最近半年使用:0次
名校
10 . 柠檬酸因具有酸性和较好的络合性,可用于浸出金属离子并得到柠檬酸浸出液。下图是从柠檬酸浸出液中分离出铜并制备碱式碳酸铜: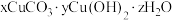 的流程
的流程

实验:(1)调pH值分离铜时,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小干理论分析结果
(2)“还原法沉铜”的步骤中,利用抗坏血酸C6H8O6能有效的将Cu(OH)2还原成金属Cu,抗坏血酸C6H8O6易被氧化为脱氢抗坏血酸C6H6O6;且受热易分解。
(3)相同条件下温度对Cu沉淀率的影响是:随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降。
(4)实验称取9.55g碱式碳酸铜 产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
则下列说法不正确的是
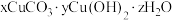 的流程
的流程
实验:(1)调pH值分离铜时,理论上铜离子完全沉淀时pH为6.67,本实验中测得pH=8时铜的沉淀率仅为7.2%,远小干理论分析结果
(2)“还原法沉铜”的步骤中,利用抗坏血酸C6H8O6能有效的将Cu(OH)2还原成金属Cu,抗坏血酸C6H8O6易被氧化为脱氢抗坏血酸C6H6O6;且受热易分解。
(3)相同条件下温度对Cu沉淀率的影响是:随着温度的升高,相同时间内Cu的沉淀率先逐渐增加,在80℃时达到最高点,后略有下降。
(4)实验称取9.55g碱式碳酸铜
 产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。
产品,通入氢气充分加热反应后,得到4.8g固体残留物,同时生成2.2g二氧化碳和2.7g水。则下列说法不正确的是
A.经过计算碱式碳酸铜的化学式组成为 |
| B.调pH分离铜时,因Cu2+与柠檬酸根形成配合物,则与OH-形成Cu(OH)2减少 |
C.抗坏血酸还原Cu(OH)2的化学反应方程式为: |
| D.温度超过80℃时,因抗坏血酸受热易分解,使浓度降低,还原铜的能力减弱 |
您最近半年使用:0次



