解题方法
1 . 中华诗词中蕴含着许多化学知识。下列说法错误的是
| A.“铁孟汤雪早,石炭煮茶迟”中的“石炭”指的是煤 |
| B.“一般皎洁羞云母,四射光茫突水精”中“水精(精同晶)”的主要成分是二氧化硅 |
| C.“九秋风露越窑开,夺得千峰翠色来”中的“翠色”来自氧化亚铜 |
| D.“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”具有胶体的性质 |
您最近半年使用:0次
2 . 一水硫酸四氨合铜[Cu(NH3)4SO4·H2O]是一种易溶于水,难溶于乙醇的绛蓝色晶体,可作高效安全的广谱杀菌剂。成外某兴趣小组查阅资料后设计实验方案制备出该晶体并对制备出的晶体进行成分检验和性质探究。
I.制备少量Cu(NH3)4SO4·H2O晶体:___________ (填仪器名称)。___________ 。
(3)步骤Ⅲ的离子方程式为___________ 。
(4)有同学查阅资料得知:(NH4)2SO4也难溶于乙醇。故对于制备出的晶体的成分,该同学提出如下假设:
假设一:只有(NH4)2SO4
假设二:只有Cu(NH3)4SO4·H2O
假设三:(NH4)2SO4和Cu(NH3)4SO4·H2O两种成分都有
已知产物晶体为蓝色,则无需实验即可排除___________ 。(填“假设一”、“假设二”、“假设三”)
Ⅱ.对制备出的晶体的成分进行检验和性质探究
(5)检验该晶体中阴离子的方法:___________ 。
(6)用所得晶体加水得到深蓝色溶液。取三份1L试样,分别加入一定量的水、稀硫酸、热的浓氢氧化钠溶液,实验现象记录如下:
结合化学用语,解释加入稀硫酸后出现的现象的原因___________ 。请补充完整加入热的浓氢氧化钠溶液后的现象:___________ 。
(7)晶体中N含量的测定
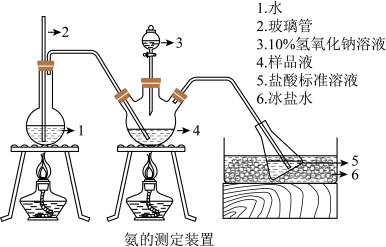
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸气,并用蒸馏水冲洗导管内壁,用V1mLc1mol/L的盐酸标准溶液完全吸收。取下接收瓶,用c2mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V2mL溶液。___________ ,样品中N的质量分数的表达式为___________ ,最终通过N的质量分数确定了样品的成分。
I.制备少量Cu(NH3)4SO4·H2O晶体:
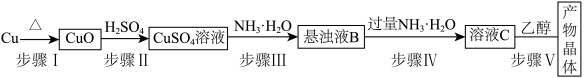
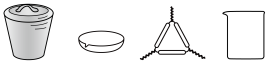
(3)步骤Ⅲ的离子方程式为
(4)有同学查阅资料得知:(NH4)2SO4也难溶于乙醇。故对于制备出的晶体的成分,该同学提出如下假设:
假设一:只有(NH4)2SO4
假设二:只有Cu(NH3)4SO4·H2O
假设三:(NH4)2SO4和Cu(NH3)4SO4·H2O两种成分都有
已知产物晶体为蓝色,则无需实验即可排除
Ⅱ.对制备出的晶体的成分进行检验和性质探究
(5)检验该晶体中阴离子的方法:
(6)用所得晶体加水得到深蓝色溶液。取三份1L试样,分别加入一定量的水、稀硫酸、热的浓氢氧化钠溶液,实验现象记录如下:
| 加入试剂 | 水 | 稀硫酸 | 热的氢氧化钠溶液 |
| 现象 | 深蓝色稍变浅 | 溶液颜色变成浅蓝色且与同浓度硫酸铜颜色相当 | 溶液最终变为无色 |
(7)晶体中N含量的测定
精确称取mg晶体,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸气,并用蒸馏水冲洗导管内壁,用V1mLc1mol/L的盐酸标准溶液完全吸收。取下接收瓶,用c2mol/LNaOH标准溶液滴定过剩的HCl,到终点时消耗V2mL溶液。
您最近半年使用:0次
解题方法
3 . 广安代市镇火力发电厂需要燃烧大量的煤,产生大量CO2和SO2等,并留下大量煤渣,对环境有较大影响。其中一种不能继续燃烧的煤渣成分俗名叫“铁甲石”,主要成分为:Al2O3(15%~24%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)、FeO(0.9%~2.0%)、CuO(8.5%~11.0%)以及其他不溶性杂质,铁甲石中的氧化铝难溶于酸,可以通过煅烧改变铁甲石结构,使其溶于酸。铁甲石经过下列化工工艺,可以制取无水CuCl2。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
(1)第一次过滤的滤渣为___________ 。
(2)加H2O2后发生反应的离子方程式为___________ 。
(3)调节溶液pH需要控制的范围是___________ ,“调节溶液pH”的过程中除添加试剂,还需借助于___________ 测定溶液pH值。
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
(5)从滤液2中得到无水CuCl2的操作为___________ 。

已知Cu2+、Fe2+、Fe3+、Al3+生成沉淀pH范围如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
| 开始沉淀pH | 5.8 | 5.8 | 2.0 | 4.0 |
| 沉淀完成pH | 7.5 | 8.3 | 3.1 | 5.4 |
(1)第一次过滤的滤渣为
(2)加H2O2后发生反应的离子方程式为
(3)调节溶液pH需要控制的范围是
(4)调节pH值用到的试剂或物质是___________(填下列字母)。
| A.氢氧化钠 | B.氨水 | C.CuO | D.AlCl3 |
(5)从滤液2中得到无水CuCl2的操作为
您最近半年使用:0次
解题方法
4 . 钠、铁、铜等金属在空气中容易变质腐蚀。下列说法错误的是
A. 很活泼,在湿润空气中久置变质为 很活泼,在湿润空气中久置变质为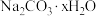 |
B. 表面包裹一层植物油可以减缓锈蚀 表面包裹一层植物油可以减缓锈蚀 |
C.生活中大量使用铝制品的原因是 常温下不与氧气反应 常温下不与氧气反应 |
D.古铜器表面生成铜绿 ,说明铜在空气中腐蚀时 ,说明铜在空气中腐蚀时 和 和 参与反应 参与反应 |
您最近半年使用:0次
名校
解题方法
5 . 云南省博物馆收藏的“四牛鎏金骑士铜贮贝器”,是滇青铜文明的代表性文物之一、下列有关该文物的说法正确的是


| A.青铜是合金 | B.青铜的熔点高于纯净的铜单质 |
C.表面的铜绿是 | D.在青铜器上鎏金是化学变化 |
您最近半年使用:0次
6 . 化学促进了科技进步和社会发展,下列叙述中没有涉及化学变化的是
| A.《神农本草经》中记载的“石胆能化铁为铜” | B.利用废弃的秸秆生产生物质燃料乙醇 |
| C.利用基本的化学原料生产化学合成药物 | D.北京冬奥会场馆使用CO2跨临界直冷制冰 |
您最近半年使用:0次
2023-11-04更新
|
326次组卷
|
2卷引用:四川省宜宾市叙州区第一中学校2023-2024学年高一上学期11月期中化学试题
7 . 常温下,下列各组粒子在指定溶液中一定能大量共存的是
A.澄清透明溶液:K+、Na+、SO 、MnO 、MnO |
| B.遇KSCN变红色的溶液:Na+、Mg2+、I-、Cl- |
C.pH=0的溶液: 、Fe2+、S2O 、Fe2+、S2O 、ClO- 、ClO- |
D.通入足量NH3的溶液:K+、Cu2+、SO 、Cl- 、Cl- |
您最近半年使用:0次
名校
解题方法
8 . 下列离子能大量共存的是
A.在含大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.无色澄清透明的溶液中: 、 、 、 、 、 、 、 、 |
C.使无色酚酞试液呈红色的溶液中: 、 、 、 、 、 、 |
D.使石蕊试液变红的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
2023-10-13更新
|
330次组卷
|
6卷引用:四川省宜宾市叙州区第一中学校2023-2024学年高一上学期11月期中化学试题
名校
解题方法
9 . 中华优秀传统文化涉及了很多化学知识,下列有关说法错误的是
| A.《本草纲目拾遗》中对强水的记载:“性最猛烈,能蚀五金。”强水为强电解质 |
| B.《神农本草经》中“石胆……能化铁为铜、成金银”描述的是湿法炼铜 |
| C.刘长卿诗云“水声冰下咽,砂路雪中平”,固态冰转化为液态水为熵增的过程 |
| D.“火树银花合,星桥铁锁开”中涉及化学能转化为热能和光能 |
您最近半年使用:0次
2023-10-12更新
|
737次组卷
|
5卷引用:四川省成都外国语学校2023-2024学年高二上学期10月月考化学试题
名校
10 . 成都理工大学刘兴诗教授提出了三星堆青铜器源自四川彭州龙门山的猜想并展开科考活动,经过调查初步判断,三星堆的铜来自龙门山区。经调查,上世纪80~90年代,该地利用资源优势,大规模进行冶铜及生产大量附属产品。以黄铜矿为原料生产硫酸、铁红、胆矾的流程如下:

已知:黄铜矿中 含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含
含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含 的
的 (Fe化合价为+2价)矿粉。
(Fe化合价为+2价)矿粉。
回答下列问题:
(1)已知信息中涉及的“浮选”过程是为了使矿石中的 含量大大增加,该过程在工业上称为矿石(元素)的
含量大大增加,该过程在工业上称为矿石(元素)的_________ 。
(2)黄铜矿粉在空气中焙烧时的化学方程式为 ,该反应中还原产物为
,该反应中还原产物为___________ ,若有标准状况下的空气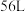 (假设空气中氧气的体积分数为
(假设空气中氧气的体积分数为 )参与反应,则反应过程中转移电子的物质的量为
)参与反应,则反应过程中转移电子的物质的量为___________ 。
(3)若在实验室环境下由固体C制得铁红,需要在___________ (填仪器名称)中进行。
(4)由气体B制硫酸的过程中,为了避免___________ ,用 的浓硫酸代替水进行气体的吸收。
的浓硫酸代替水进行气体的吸收。
(5)由固体B通过一系列操作制备 溶液的过程中,有以下四种方案:
溶液的过程中,有以下四种方案:
①固体B先在空气中充分灼烧,再用稀硫酸溶解,过滤;
②直接用浓硫酸溶解,过滤;
③边通空气边加热,在稀硫酸中溶解,过滤;
④在混酸(按一定比例混合的稀硝酸和稀硫酸)溶液中溶解,过滤;
ⅰ.方案②相对方案①,不足之处有___________ ;
ⅰ.方案③中发生反应的离子方程式为___________ ;
ⅲ.方案④中当金属和酸同时消耗完,所得溶液不含硝酸铜,则硝酸和硫酸的物质的量浓度比为___________ 时恰好满足。

已知:黄铜矿中
 含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含
含量不高,工业上一般通过浮选除去矿石中的其他成分,得到仅含 的
的 (Fe化合价为+2价)矿粉。
(Fe化合价为+2价)矿粉。回答下列问题:
(1)已知信息中涉及的“浮选”过程是为了使矿石中的
 含量大大增加,该过程在工业上称为矿石(元素)的
含量大大增加,该过程在工业上称为矿石(元素)的(2)黄铜矿粉在空气中焙烧时的化学方程式为
 ,该反应中还原产物为
,该反应中还原产物为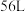 (假设空气中氧气的体积分数为
(假设空气中氧气的体积分数为 )参与反应,则反应过程中转移电子的物质的量为
)参与反应,则反应过程中转移电子的物质的量为(3)若在实验室环境下由固体C制得铁红,需要在
(4)由气体B制硫酸的过程中,为了避免
 的浓硫酸代替水进行气体的吸收。
的浓硫酸代替水进行气体的吸收。(5)由固体B通过一系列操作制备
 溶液的过程中,有以下四种方案:
溶液的过程中,有以下四种方案:①固体B先在空气中充分灼烧,再用稀硫酸溶解,过滤;
②直接用浓硫酸溶解,过滤;
③边通空气边加热,在稀硫酸中溶解,过滤;
④在混酸(按一定比例混合的稀硝酸和稀硫酸)溶液中溶解,过滤;
ⅰ.方案②相对方案①,不足之处有
ⅰ.方案③中发生反应的离子方程式为
ⅲ.方案④中当金属和酸同时消耗完,所得溶液不含硝酸铜,则硝酸和硫酸的物质的量浓度比为
您最近半年使用:0次



