名校
1 . 在中华文明的历史长河中,江西人才辈出,文化璀璨,下列说法正确的是
| A.“落木千山天远大,澄江一道月分明”,月亮倒映在江水中的现象属于丁达尔效应 |
B.白鹿洞书院建筑群易受酸雨腐蚀, 的雨水为酸雨 的雨水为酸雨 |
C.“庐山山南刷铜绿”,“铜绿”的主要成分为 |
| D.“白如玉,明如镜,薄如纸,声如馨”的景德镇白瓷的主要成分为无机硅酸盐材料 |
您最近半年使用:0次
名校
解题方法
2 . 化学为生活创造美。下列说法正确的是
| A.用氢氟酸在玻璃上雕刻花纹,利用了氢氟酸的强酸性 |
| B.节日里的烟花表演利用了焰色试验,焰色试验属于化学变化 |
| C.游泳池里定期添加硫酸铜,主要目的是使池水更美丽梦幻 |
| D.发黑的银首饰置于盛有热食盐溶液的锡纸碗中,很快恢复光亮,利用了氧化还原反应 |
您最近半年使用:0次
2024-01-07更新
|
195次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
3 . 某课外研究小组,用杂铜(含有较多杂质的铜粉),通过不同的途径制取胆矾,实验过程如下:
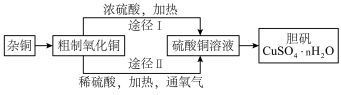
回答下列问题:
(1)杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于___________ 上,灼烧后的坩埚应放在___________ 上,不能直接放在桌面上。
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物。灼烧后含有少量铜的原因可能是___________ (填字母)。
a.灼烧过程中部分氧化铜被有机物还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解生成铜 d.该条件下铜无法被氧气氧化
(3)由粗制氧化铜(含单质铜)通过两种途径制取胆矾,与途径I相比,途径Ⅱ有明显的两个优点是:___________ 。
(4)胆矾(CuSO4・nH2O)中结晶水n值的测定,步骤如下:
i.称量坩埚的质量,记为m1 g;ii.称量坩埚和胆矾的质量,记为m2 g;iii.加热、冷却、称量坩埚和固体的质量,记为m3 g;iv.再次加热、冷却、称量坩埚和固体的质量,最终总质量恒定为m4 g(注:上述过程无 CuSO4分解)。
①步骤iii中的坩埚应放在___________ 中冷却。
②胆矾(CuSO4・nH₂O)中结晶水n=___________ 。
③下列不规范操作会导致测定结果“偏大”或“偏小”,请将结果填在每种情况后面的横线上:
胆矾晶体的颗粒较大_______ ;加热后放在空气中冷却_____ ;加热温度过高_______ 。

回答下列问题:
(1)杂铜中含有大量的有机物,可采用灼烧的方法除去有机物,灼烧时将瓷坩埚置于
(2)杂铜经灼烧后得到的产物是氧化铜及少量铜的混合物。灼烧后含有少量铜的原因可能是
a.灼烧过程中部分氧化铜被有机物还原 b.灼烧不充分铜未被完全氧化
c.氧化铜在加热过程中分解生成铜 d.该条件下铜无法被氧气氧化
(3)由粗制氧化铜(含单质铜)通过两种途径制取胆矾,与途径I相比,途径Ⅱ有明显的两个优点是:
(4)胆矾(CuSO4・nH2O)中结晶水n值的测定,步骤如下:
i.称量坩埚的质量,记为m1 g;ii.称量坩埚和胆矾的质量,记为m2 g;iii.加热、冷却、称量坩埚和固体的质量,记为m3 g;iv.再次加热、冷却、称量坩埚和固体的质量,最终总质量恒定为m4 g(注:上述过程无 CuSO4分解)。
①步骤iii中的坩埚应放在
②胆矾(CuSO4・nH₂O)中结晶水n=
③下列不规范操作会导致测定结果“偏大”或“偏小”,请将结果填在每种情况后面的横线上:
胆矾晶体的颗粒较大
您最近半年使用:0次
解题方法
4 . 传世名画《千里江山图》的主要取景地是庐山与鄱阳湖,其采用的绿蓝两种颜料——优质孔雀石【Cu2(OH)2CO3】和蓝铜矿【Cu2(OH)2(CO3)2】。
(1)从地表采掘的孔雀石【Cu2(OH)2CO3】,还是古代冶炼铜的原料。流程如下:
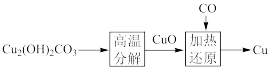
孔雀石【Cu2(OH)2CO3】中铜元素的化合价为___________ ,其高温分解的化学方程式是___________ ;加热还原过程中氧化剂、还原剂分别为___________ 、___________ 。
(2)地表深处的黄铜矿(CuFeS2)被氧气氧化:xCuFeS2+yO2→zCu2++qFe2++nSO ;形成Cu2+流入地表后,遇到石灰石形成孔雀石,同时还有CaSO4和CO2生成。
;形成Cu2+流入地表后,遇到石灰石形成孔雀石,同时还有CaSO4和CO2生成。
①x=___________ ,y=___________ 。
②形成孔雀石的化学方程式是___________ 。
③孔雀石虽然较稳定,遇到足量盐酸则完全溶解,其离子方程式为___________ 。
④Cu2+流入地表后可以形成孔雀石、蓝铜矿或Cu(OH)2三种矿物质,当HCO 浓度相对较大时,产物主要取决于地表水溶液的pH大小。弱酸性水中,一般以
浓度相对较大时,产物主要取决于地表水溶液的pH大小。弱酸性水中,一般以___________ (填化学式)为主;pH>10的碱性水中,一般以___________ (填化学式)为主。
(1)从地表采掘的孔雀石【Cu2(OH)2CO3】,还是古代冶炼铜的原料。流程如下:
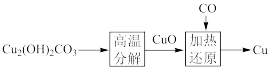
孔雀石【Cu2(OH)2CO3】中铜元素的化合价为
(2)地表深处的黄铜矿(CuFeS2)被氧气氧化:xCuFeS2+yO2→zCu2++qFe2++nSO
 ;形成Cu2+流入地表后,遇到石灰石形成孔雀石,同时还有CaSO4和CO2生成。
;形成Cu2+流入地表后,遇到石灰石形成孔雀石,同时还有CaSO4和CO2生成。①x=
②形成孔雀石的化学方程式是
③孔雀石虽然较稳定,遇到足量盐酸则完全溶解,其离子方程式为
④Cu2+流入地表后可以形成孔雀石、蓝铜矿或Cu(OH)2三种矿物质,当HCO
 浓度相对较大时,产物主要取决于地表水溶液的pH大小。弱酸性水中,一般以
浓度相对较大时,产物主要取决于地表水溶液的pH大小。弱酸性水中,一般以
您最近半年使用:0次
解题方法
5 . 下列各组离子在同一溶液中一定能大量共存的是
A.含大量Ba2+的溶液中:Cl-、K+、 、 、 |
B.含大量H+的溶液中:Mg2+、Na+、 、 、 |
C.含大量OH-的溶液中:K+、 、 、 、Cu2+ 、Cu2+ |
D.含大量Na+的溶液中:H+、K+、 、 、 |
您最近半年使用:0次
2023-11-26更新
|
73次组卷
|
2卷引用:江西省南昌市南钢学校2023-2024学年高一上学期期中考试化学试卷
6 . 钠及其化合物的生产、应用,是化工生产与研究的重要组成部分。
(1) 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:

①生成 的化学方程式是
的化学方程式是_______ 。
② 样品加水溶解的化学方程式为
样品加水溶解的化学方程式为_______ ,样液中加入 后产生
后产生 ,说明
,说明 与水反应的过程中生成了
与水反应的过程中生成了_______ (填化学式)。
③滤液中加入 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为
样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为_______ 。
(2)工业上以侯氏制碱法为基础生产焦亚硫酸钠( ,能溶于水)的工艺流程如图:
,能溶于水)的工艺流程如图:
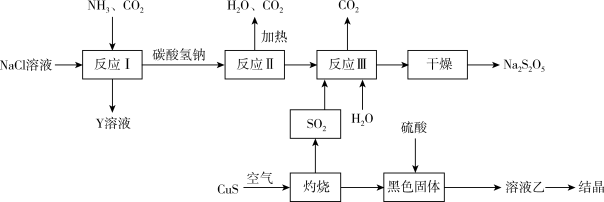
①反应Ⅱ的化学方程式为_______ 。
②关于该流程,下列说法正确的是_______ (填字母)
A.反应Ⅰ属于氧化还原反应 B.该流程中, 可以循环使用
可以循环使用
C.反应Ⅰ中应先通入 ,再通入
,再通入 D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
(3) 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为_______ 。
(1)
 用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备
用途广泛,可用于医药、印染、漂白及用作分析试剂等。实验室模拟工业制备 并检验其纯度的实验流程如图所示。回答下列问题:
并检验其纯度的实验流程如图所示。回答下列问题:
①生成
 的化学方程式是
的化学方程式是②
 样品加水溶解的化学方程式为
样品加水溶解的化学方程式为 后产生
后产生 ,说明
,说明 与水反应的过程中生成了
与水反应的过程中生成了③滤液中加入
 溶液产生白色沉淀,说明
溶液产生白色沉淀,说明 样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为
样品中含有碳酸钠杂质,生成白色沉淀的离子方程式为(2)工业上以侯氏制碱法为基础生产焦亚硫酸钠(
 ,能溶于水)的工艺流程如图:
,能溶于水)的工艺流程如图:
①反应Ⅱ的化学方程式为
②关于该流程,下列说法正确的是
A.反应Ⅰ属于氧化还原反应 B.该流程中,
 可以循环使用
可以循环使用C.反应Ⅰ中应先通入
 ,再通入
,再通入 D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体
D.溶液乙通过蒸发浓缩、冷却结晶可得硫酸铜晶体(3)
 在空气中灼烧的化学方程式为
在空气中灼烧的化学方程式为
您最近半年使用:0次
2023-11-14更新
|
261次组卷
|
2卷引用:江西省赣州市全南中学2023-2024学年高一上学期11月期中考试化学试题
7 . 铜元素的价类二维图如图,下列有关说法正确的是
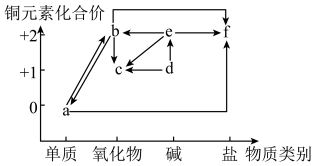
| A.a可直接转化为e |
| B.b转化为c一定需要另加还原剂 |
| C.新制的e可用于检验葡萄糖中的醛基 |
| D.直接加热f溶液一定可得到f固体 |
您最近半年使用:0次
2023-11-10更新
|
217次组卷
|
2卷引用:江西省赣州市部分市县学校2023-2024学年高三上学期期中考试化学试题
名校
解题方法
8 . 足量C(s)与H2O(g)反应生成1mol H2(g)和1mol CO(g)时,吸收131.3kJ的热量,该反应可用于制取水煤气;下列化学反应表示正确的是
A.制取水煤气的热化学方程式: 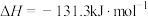 |
B.高温下甲烷还原氧化铜: |
C.乙酸除水垢: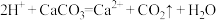 |
D.CaC2与水反应: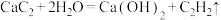 |
您最近半年使用:0次
2023-10-17更新
|
217次组卷
|
2卷引用:江西省广丰中学2023-2024学年高二上学期10月月考化学试题
9 . 《淮南万毕术》中,有“曾青得铁则化为铜”的记载。这说明早在西汉时期,我国劳动人民就已经发现铁能从某些含铜(+2价)化合物的溶液中置换出铜,这个反应是现代湿法冶金的基础。下列说法正确的是
| A.无水硫酸铜粉末为蓝色 |
B.对于反应 ,氧化性: ,氧化性: |
| C.四大基本反应类型不包括置换反应 |
D.理论上,可用湿法冶金的方法来提取 溶液中的Fe 溶液中的Fe |
您最近半年使用:0次
10 . 现对一批已生锈的弹壳进行回收利用,主要流程如下:
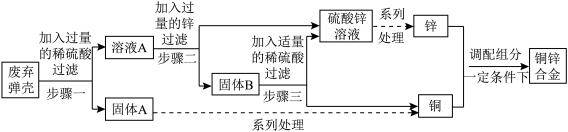
(资料)①该弹壳由铜锌合金制成,其锈的主要成分是Cu2(OH)2CO3。
②Cu2(OH)2CO3能与稀硫酸反应生成硫酸铜,其他杂质不溶于水,也不参与反应。
(1)为加快步骤一的反应速率,可采用的方法是___________ (填一种即可);
(2)溶液A中的溶质是(写化学式)___________ ;固体B含有的物质为(写化学式)___________ ;
(3)步骤三中发生反应的化学方程式为___________ ;
(4)回收锌的质量___________ 废弃弹壳中锌元素的质量(选填“大于”、“小于”或“等于”);
(5)改变铜锌合金中锌的含量可以得到不同机械性能的黄铜。现欲制备120吨(t)含锌量小于35%的黄铜,该类黄铜具有良好的塑性,能承受冷热加工,但在200℃~700℃之间热加工时易断裂。下列符合原料配比及热加工条件的是___________ (填字母序号)。
a.锌44t 铜76t 750℃ b.锌38t 铜82t 500℃
c.锌55t 铜65t 190℃ d.锌25t 铜95t 750℃

(资料)①该弹壳由铜锌合金制成,其锈的主要成分是Cu2(OH)2CO3。
②Cu2(OH)2CO3能与稀硫酸反应生成硫酸铜,其他杂质不溶于水,也不参与反应。
(1)为加快步骤一的反应速率,可采用的方法是
(2)溶液A中的溶质是(写化学式)
(3)步骤三中发生反应的化学方程式为
(4)回收锌的质量
(5)改变铜锌合金中锌的含量可以得到不同机械性能的黄铜。现欲制备120吨(t)含锌量小于35%的黄铜,该类黄铜具有良好的塑性,能承受冷热加工,但在200℃~700℃之间热加工时易断裂。下列符合原料配比及热加工条件的是
a.锌44t 铜76t 750℃ b.锌38t 铜82t 500℃
c.锌55t 铜65t 190℃ d.锌25t 铜95t 750℃
您最近半年使用:0次



