名校
解题方法
1 . 向CuSO4溶液中加入H2O2溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。下列关于上述过程的说法不正确的是
| A.Cu2+是H2O2分解反应的催化剂 |
| B.Cu2+将H2O2还原为O2 |
| C.H2O2既表现氧化性又表现还原性 |
| D.发生了反应:Cu2O+H2O2+4H+=2Cu2++3H2O |
您最近半年使用:0次
2021-06-23更新
|
3168次组卷
|
39卷引用:江西省上饶市万年中学2020-2021学年高一上学期期中考试化学试题
江西省上饶市万年中学2020-2021学年高一上学期期中考试化学试题江西省高安中学2021-2022学年高一上学期期中考试化学试题北京市西城区2018届高三4月一模理综化学试题黑龙江省哈尔滨师范大学附属中学2019届高三上学期第一次月考化学试题福建省尤溪县第一中学2019届高三第一学期第一次月考化学试题【区级联考】天津市河东区2019届高三高考一模考试化学试题河南省洛阳市第一高级中学2019-2020学年高一9月月考化学试题河北省辛集中学2020届高三9月月考化学试题(已下线)【新东方】2020-18安徽省淮南市寿县一中2020 届高三素质测试化学试题湖南省长沙市雅礼中学2020届高三上学期第2次月考化学试题(已下线)第三节 氧化还原反应(二)-2020-2021学年高一化学必修第一册课时同步练(新人教)湖南省常德市第二中学2021届高三上学期开学考试化学试题(已下线)第1章 章末检测-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)北京市北京师范大学附属中学2020—2021学年高一上学期期中考试化学试题河北省保定市定州市第二中学2020-2021学年高一上学期11月月考化学试题天津市静海区第一中学2020-2021学年高一12月考化学试题上海市普陀区2021届高三二模化学试题河北省石家庄二中2020-2021学年高一第二学期6月月考化学试题(已下线)专题1.3.1 氧化还原反应(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点16 铜及其金属材料-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题卷二 氧化还原反应(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)甘肃省天水市第一中学2021-2022高三上学期第三次考试化学试题北京师范大学附属中学2021-2022学年高一上学期期中考试化学试题河南省名校联盟2021-2022学年高三上学期第三次诊断考试化学试题(已下线)一轮巩固卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(上海卷)吉林省吉林市第一中学2021-2022学年高二下学期(平行班)期中考试化学试题(已下线)微专题15 铜及其化合物的性质、制备与实验探究-备战2023年高考化学一轮复习考点微专题陕西省西安高新第一中学2022-2023学年高一上学期期中考试化学试题天津市第四十七中学2021-2022学年高一上学期第二次月考化学试题天津市北辰区四十七中学2022-2023高一上学期期末考试化学试题山东省菏泽第一中学2022-2023学年高一上学期期末考试化学试题(已下线)题型49 臭氧和过氧化氢 环境保护(已下线)【2023】【高一下】【其他】【杭二中-期中复习卷】【高中化学】【邵威宏收集】安徽省安庆市第一中学2023-2024学年高一上学期第一次阶段测化学试题四川省眉山市彭山区第一中学2023-2024学年高一上学期10月月考化学试题北京市第三十五中学2021-2022学年高一上学期期中考试化学试题天津市滨海新区塘沽第一中学2022届高三毕业班第三次月考化学试题
名校
解题方法
2 . 碘化钠在光学器件石油探测、安检、环境监测等领域有重要应用。某研究小组开发设计的制备高纯NaI的简化流程如图:
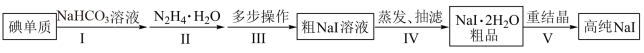
已知:
①I2(s)+I-(aq) I
I (aq)。
(aq)。
②水合肼(N2H4•H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO 离子。
离子。
①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为__ 。
②实验过程中,加少量NaI固体能使反应速率加快,其原因是__ 。
(2)步骤Ⅱ,水合肼与IO-反应的离子方程式为__ 。
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH值时依次加入的试剂为__ 。
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有__ 。
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为__ 。
(5)将制备的NaI•2H2O粗品以95%乙醇为溶剂进行重结晶。请给出合理的操作排序__ 。
加热95%乙醇→____→___→___→____→纯品(选填序号)。
①减压蒸发结晶 ②NaI•2H2O粗品溶解 ③趁热过滤 ④真空干燥
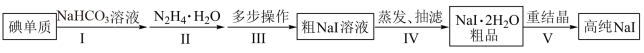
已知:
①I2(s)+I-(aq)
 I
I (aq)。
(aq)。②水合肼(N2H4•H2O)具有强还原性,可分别将碘的各种酸根和I2还原为I-,本身被氧化为无毒物质。
③NaI易溶于水,也易溶于酒精,在酒精中的溶解度随温度的升高增加不大。
请回答:
(1)步骤Ⅰ,I2与NaHCO3溶液发生歧化反应,生成物中含IO-和IO
 离子。
离子。①I2与NaHCO3溶液反应适宜温度为40~70℃,则采用的加热方式为
②实验过程中,加少量NaI固体能使反应速率加快,其原因是
(2)步骤Ⅱ,水合肼与IO-反应的离子方程式为
(3)步骤Ⅲ,多步操作为:
①将步骤Ⅱ得到的pH为6.5~7的溶液调整pH值至9~10,在100℃下保温8h,得到溶液A;
②将溶液A的pH值调整至3~4,在70~80℃下保温4h,得溶液B;
③将溶液B的pH调整至6.5~7,得溶液C;
④在溶液C中加入活性炭,混合均匀后煮沸,静置10~24h后,过滤除杂得粗NaI溶液。
上述①②③操作中,调整pH值时依次加入的试剂为
A.NaOH B.HI C.NH3•H2O D.高纯水
(4)步骤Ⅳ,采用改进的方案为用“减压蒸发”代替“常压蒸发”。
①“减压蒸发”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管、接收瓶之外,还有
A.直形冷凝管 B.球形冷凝管 C.烧杯 D.抽气泵
②采用“减压蒸发”的优点为
(5)将制备的NaI•2H2O粗品以95%乙醇为溶剂进行重结晶。请给出合理的操作排序
加热95%乙醇→____→___→___→____→纯品(选填序号)。
①减压蒸发结晶 ②NaI•2H2O粗品溶解 ③趁热过滤 ④真空干燥
您最近半年使用:0次
2020-07-10更新
|
305次组卷
|
4卷引用:江西省南昌市第二中学2020届高三下学期校测(一)理科综合化学试题
解题方法
3 . 下列有关物质性质的应用正确的是
| A.钠具有很强的还原性,可用钠与TiCl4溶液反应制取钛 |
| B.铝表面易形成致密的氧化膜,可用铝制贮罐盛装稀硝酸 |
| C.FeCl3具有很强的氧化性,可用于包括铜、不锈钢、铝等材料的蚀刻 |
| D.硫酸铜能与氯化钡反应,可用于给误食氯化钡的患者洗胃 |
您最近半年使用:0次
名校
4 . 某校化学研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式______________________________________ ;
(2)在实验室中,还可以用浓氨水与____________ (填写一种试剂)快速制取少量氨气;
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:
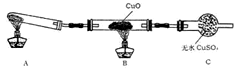
(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是____ 。
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与CuO反应的化学方程式:_________________________
(三)问题讨论
(1)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+ Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O
Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O_______________________________________________ 。
(2)在解决了问题(1)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取98 gCu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变为红色粉末A。冷却后称量,A的质量为72g。据此可推得,A的化学式为____________ 。由此,得到的结论是:________________________________ 。
(一)制取氨气
(1)写出实验制取氨气的化学方程式
(2)在实验室中,还可以用浓氨水与
(二)该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:

(1)该装置在设计上有一定缺陷,为保证实验结果的准确性,对该装置的改进措施是
(2)利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的气体。写出氨气与CuO反应的化学方程式:
(三)问题讨论
(1)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O。已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+
 Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O
Cu+Cu2+)。请你设计一个简单的实验检验该红色物质中是否含有Cu2O(2)在解决了问题(1)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是他们进行了如下实验:取98 gCu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1000℃以上,黑色粉末全部变为红色粉末A。冷却后称量,A的质量为72g。据此可推得,A的化学式为
您最近半年使用:0次
5 . 《淮南万毕术》中,有“曾青得铁则化为铜”的记载。这说明早在西汉时期,我国劳动人民就已经发现铁能从某些含铜(+2价)化合物的溶液中置换出铜,这个反应是现代湿法冶金的基础。下列说法正确的是
| A.无水硫酸铜粉末为蓝色 |
B.对于反应 ,氧化性: ,氧化性: |
| C.四大基本反应类型不包括置换反应 |
D.理论上,可用湿法冶金的方法来提取 溶液中的Fe 溶液中的Fe |
您最近半年使用:0次
名校
6 . 中国传统文化对人类文明贡献巨大,很早就把化学技术应用到生产生活中。下列与化学有关的说法不正确 的是
| A.《天工开物》中“至于矾现五金色之形硫为群石之将,皆变化于烈火”,其中矾指金属硫酸盐 |
B.《神农本草经》中捉到:“白青[ ]得铁化为铜”,其中白青属于碱 ]得铁化为铜”,其中白青属于碱 |
| C.《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以烽燧铳极”这是利用了“KNO3的氧化性” |
| D.《本草经集注》中记载了区分硝石(KNO3)和朴消(Na2SO4)的方法:“以火烧之,烟起,乃真硝石也”,二者也可以利用“焰色试验”区分 |
您最近半年使用:0次
2021-11-20更新
|
498次组卷
|
3卷引用:江西省丰城中学 2021-2022 学年高三上学期第四次段考化学试题(尖子重点班)
江西省丰城中学 2021-2022 学年高三上学期第四次段考化学试题(尖子重点班)广东省广州市第六中学2021-2022学年高一上学期期中化学试题(已下线)3.2.2 硫酸 不同价态硫元素间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
名校
解题方法
7 . 以下是中华民族为人类文明进步做出巨大贡献的几个事例,运用化学知识对其进行的分析不合理的是( )
| A.《本草纲目》中有如下记载:“火药乃焰硝(KNO3)、硫黄、杉木炭所合,以为烽燧铳机诸药者”,其中利用了KNO3的氧化性 |
| B.商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品 |
| C.宋代《千里江山图》卷中的绿色颜料铜绿的主要成分是碱式碳酸铜,该颜料耐酸耐碱 |
| D.屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作 |
您最近半年使用:0次
名校
8 . 已知:①甲醛(HCHO)与葡萄糖化学性质相似,都具有还原性。②甲醛易挥发,甲酸钙易溶于水。为探究过量的甲醛和新制Cu(OH)2反应的产物,进行如下实验:
(1)在下图装置中进行实验,向a中加入0.5mol·L-1CuSO4溶液50mL和5mol·L-1NaOH 溶液100mL,振荡,再加入40%的甲醛溶液50mL,缓慢加热20分钟后冷却至室温。

仪器a、b的名称分别是________________ 、_______________ 。
(2)上述实验有副反应发生,产生的气体为CO、H2中的一种或两种。为确认气体成分,将装置A 和如下图所示装置连接后进行实验。
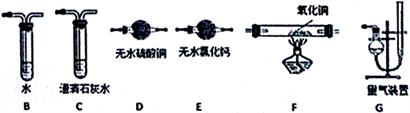
依次连接的合理顺序为A→____ →____→____→____→____→G。副产物中如果有CO,实验现象是:_____________________________________ 。
(3)已知HCHO 最终被氧化为CO32-,请写出a容器中发生的反应化学方程式:_________________________________________ 。
(4)反应后a中有红色固体产生,为探究其组成,提出如下假设:
假设一:只有Cu2O 假设二:只有Cu
假设三:CuO和Cu 假设四:_______________ ;
其中假设三明显不成立,理由是___________________________________ 。
(5)为了对(4)的猜想进行验证,进行如下实验(以下任步均充分反应):
已知:已知:Cu2O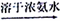 [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色) [Cu(NH3)4]2+ (蓝色)
[Cu(NH3)4]2+ (蓝色)
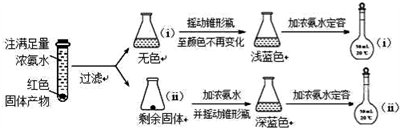
①锥形瓶ii中固体加入浓氨水后,完全溶解得到深蓝色溶液,该过程所发生的离子方程式为__________________________________________ ;
②将容量瓶ii中的溶液稀释20倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为_________________________________ 。
(1)在下图装置中进行实验,向a中加入0.5mol·L-1CuSO4溶液50mL和5mol·L-1NaOH 溶液100mL,振荡,再加入40%的甲醛溶液50mL,缓慢加热20分钟后冷却至室温。

仪器a、b的名称分别是
(2)上述实验有副反应发生,产生的气体为CO、H2中的一种或两种。为确认气体成分,将装置A 和如下图所示装置连接后进行实验。

依次连接的合理顺序为A→
(3)已知HCHO 最终被氧化为CO32-,请写出a容器中发生的反应化学方程式:
(4)反应后a中有红色固体产生,为探究其组成,提出如下假设:
假设一:只有Cu2O 假设二:只有Cu
假设三:CuO和Cu 假设四:
其中假设三明显不成立,理由是
(5)为了对(4)的猜想进行验证,进行如下实验(以下任步均充分反应):
已知:已知:Cu2O
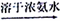 [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色) [Cu(NH3)4]2+ (蓝色)
[Cu(NH3)4]2+ (蓝色) 
①锥形瓶ii中固体加入浓氨水后,完全溶解得到深蓝色溶液,该过程所发生的离子方程式为
②将容量瓶ii中的溶液稀释20倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为
您最近半年使用:0次
名校
9 . 下列现象或事实、解释都正确的是
| 选项 | 现象或事实 | 解释 |
| A | 金属镁着火不能用泡沫灭火器灭火 | 燃烧生成的MgO与CO2反应 |
| B | K2FeO4用于自来水的消毒和净化 | K2FeO4具有强氧化性可杀菌消毒,其还原产物Fe3+水解得到的胶状物能净水 |
| C | 古代青铜器表面有铜锈,可放入盐酸中浸泡除锈 | 铜锈是铜在空气中缓慢氧化生成的氧化物,可溶于盐酸 |
| D | 常温下,将铁片浸入足量的浓硫酸中,铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2019-11-13更新
|
531次组卷
|
11卷引用:江西省兴国三中2021届高三上学期第一次月考化学试题
江西省兴国三中2021届高三上学期第一次月考化学试题山东省聊城市冠县2020届高三10月月考化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——盐类水解的基础考查陕西省延安市吴起高级中学2019-2020学年高二下学期第四次质量检测(期末)化学试题河北省唐山市第十一中学2021届高三9月入学检测化学试题内蒙古赤峰市宁城县2021届高三9月摸底考试化学试题四川省内江市第六中学2021届高三上学期10月月考化学试题安徽省泗县第一中学2022届高三上学期开学考试化学试题安徽省亳州市第五完全中学2021-2022学年高三上学期期中考试化学试题安徽省六安中学2021-2022学年高三上学期第三次月考化学试题广东省广州市第一中学2021-2022学年高三下学期2月教学质量监测化学试题
名校
解题方法
10 . 已知 为
为 和
和 的混合物,且知氧化性顺序:
的混合物,且知氧化性顺序: ,取
,取 样品进行如下图所示的实验:
样品进行如下图所示的实验:
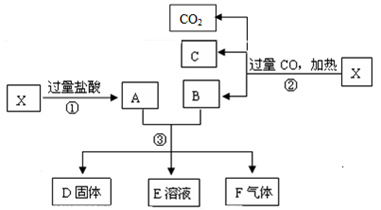
(1)写出③步可能发生反应的3个离子方程式为________________________ 、________________________ 、________________________ 。
(2)若溶液E中只有一种金属离子,则一定是______ ;若D固体是纯净物,该固体是______ 。(填化学式)
(3)向溶液A中加入 粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上
粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上__________________________________________ 。
 为
为 和
和 的混合物,且知氧化性顺序:
的混合物,且知氧化性顺序: ,取
,取 样品进行如下图所示的实验:
样品进行如下图所示的实验:
(1)写出③步可能发生反应的3个离子方程式为
(2)若溶液E中只有一种金属离子,则一定是
(3)向溶液A中加入
 粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上
粉,若会反应,则写出反应的离子方程式,若不会反应,则填“不能”在横线上
您最近半年使用:0次
2019-01-12更新
|
299次组卷
|
4卷引用:【全国百强校】江西省抚州市临川第一中学2018-2019学年高一上学期12月月考化学试题
【全国百强校】江西省抚州市临川第一中学2018-2019学年高一上学期12月月考化学试题四川省泸县第四中学2019-2020学年高一下学期第一次在线月考化学试题(已下线)第二章 元素与物质世界(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)山西省芮城中学2021-2022学年高一上学期阶段性月考化学试题



