名校
1 . 工业上制备下列物质的生产流程不合理的是
A.以废铜屑制硝酸铜: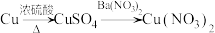 |
B.由黄铁矿制硫酸: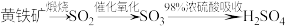 |
C.工业制硝酸: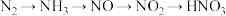 |
D.由石英砂制高纯硅: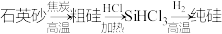 |
您最近半年使用:0次
解题方法
2 .  在工业生产中有着重要应用。利用以下装置制备
在工业生产中有着重要应用。利用以下装置制备 并测定产品纯度。
并测定产品纯度。
已知:Ⅰ. 是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
Ⅱ.浓的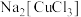 溶液为无色,加水稀释即析出
溶液为无色,加水稀释即析出 白色固体。
白色固体。

回答下列问题:
(1)①图中制取 的反应中,氧化剂和还原剂的物质的量之比为
的反应中,氧化剂和还原剂的物质的量之比为_____ 。
②装有浓盐酸的仪器名称为:_____ 。
③为吸收 尾气,C中可选用试剂
尾气,C中可选用试剂_____ (填标号)。
A. 溶液 B.饱和食盐水 C.浓
溶液 B.饱和食盐水 C.浓 D.
D. 溶液
溶液
(2)制备 :打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:
:打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:
①
②_____
③
观察到_____ 时停止反应。将B中溶液倾入盛有蒸馏水的烧杯中,立即得到白色 沉淀,抽滤得
沉淀,抽滤得 粗品。
粗品。
(3)洗涤 :洗涤时最好用95%的乙醇洗涤滤饼,其目的是
:洗涤时最好用95%的乙醇洗涤滤饼,其目的是_____ 。
(4) 纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的
纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用
溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用 的
的 溶液滴定至终点,再重复滴定2次,三次平均消耗
溶液滴定至终点,再重复滴定2次,三次平均消耗 溶液25.00mL(滴定过程中
溶液25.00mL(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。
①产品中加入 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为_____ ;
②产品中 的质量分数为
的质量分数为_____ 。
 在工业生产中有着重要应用。利用以下装置制备
在工业生产中有着重要应用。利用以下装置制备 并测定产品纯度。
并测定产品纯度。已知:Ⅰ.
 是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。
是白色固体,不溶于水和乙醇,在潮湿空气中可被迅速氧化。Ⅱ.浓的
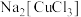 溶液为无色,加水稀释即析出
溶液为无色,加水稀释即析出 白色固体。
白色固体。
回答下列问题:
(1)①图中制取
 的反应中,氧化剂和还原剂的物质的量之比为
的反应中,氧化剂和还原剂的物质的量之比为②装有浓盐酸的仪器名称为:
③为吸收
 尾气,C中可选用试剂
尾气,C中可选用试剂A.
 溶液 B.饱和食盐水 C.浓
溶液 B.饱和食盐水 C.浓 D.
D. 溶液
溶液(2)制备
 :打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:
:打开分液漏斗旋塞与搅拌器,装置B中依次发生反应的离子方程式为:①

②
③

观察到
 沉淀,抽滤得
沉淀,抽滤得 粗品。
粗品。(3)洗涤
 :洗涤时最好用95%的乙醇洗涤滤饼,其目的是
:洗涤时最好用95%的乙醇洗涤滤饼,其目的是(4)
 纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的
纯度测定:称取所制备的氯化亚铜成品3.00g,将其置于过量的 溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用
溶液中,待样品完全溶解后,加入适量稀硫酸,配成250mL溶液。移取25.00mL溶液于锥形瓶中,用 的
的 溶液滴定至终点,再重复滴定2次,三次平均消耗
溶液滴定至终点,再重复滴定2次,三次平均消耗 溶液25.00mL(滴定过程中
溶液25.00mL(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。①产品中加入
 溶液时,发生反应的离子方程式为
溶液时,发生反应的离子方程式为②产品中
 的质量分数为
的质量分数为
您最近半年使用:0次
3 . 下表中,对陈述I、II的正确性及两者间是否具有因果关系的判断都正确的是
| 选项 | 陈述I | 陈述II | 判断 |
| A | 碳酸钠溶液显碱性 | 碳酸钠可做胃酸中和剂 | I对,II对,无 |
| B | Fe2+可以与酸性 KMnO4 发生氧化还原反应,能使酸性高锰酸钾溶液褪色 | 用酸性 KMnO4 溶液检验 Fe2(SO4)3溶液中是否含有 FeSO4 | I对,II对,有 |
| C | 铝单质既能与盐酸反应放出氢气,又能与氢氧化钠溶液反应放出氢气 | 常温下铝制容器可以盛装浓硫酸 | I对,II对,有 |
| D | 铜绿的主要成分是碱式碳酸铜,碱式碳酸铜能溶于稀盐酸 | 可用盐酸除去铜器表面的铜绿 | I对,II错,无 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
4 . 某无色透明溶液中可能大量含有 、
、 、
、 、
、 、
、 、
、 中的若干种,现对其进行如下实验:
中的若干种,现对其进行如下实验:
i:取少量该溶液,加入过量 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;
ii:向i中所得沉淀中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
iii:向i中所得滤液中加入足量硝酸酸化后,再加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为___________ 。
(2)通过实验i可知溶液中一定不会大量存在的离子为___________ 。
(3)由实验ii可知溶液中一定不会大量存在的离子为___________ 。
(4)由上述实验得到结论:该溶液一定大量存在的离子为___________ ,可能大量存在的离子为___________ 。
(5)写出实验ii中沉淀溶解的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 中的若干种,现对其进行如下实验:
中的若干种,现对其进行如下实验:i:取少量该溶液,加入过量
 溶液,产生白色沉淀,过滤;
溶液,产生白色沉淀,过滤;ii:向i中所得沉淀中加入足量盐酸,沉淀全部溶解,并有无色气体生成;
iii:向i中所得滤液中加入足量硝酸酸化后,再加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。回答下列问题:
(1)无需实验即可推断溶液中一定不会大量存在的离子为
(2)通过实验i可知溶液中一定不会大量存在的离子为
(3)由实验ii可知溶液中一定不会大量存在的离子为
(4)由上述实验得到结论:该溶液一定大量存在的离子为
(5)写出实验ii中沉淀溶解的离子方程式
您最近半年使用:0次
名校
5 . 有一包白色粉末,由BaCl2、K2SO4、CaCO3、NaOH、CuSO4中的一种或几种组成,为了探究它的成分,进行了如下实验。下列判断正确的是


| A.BaCl2、CaCO3一定存在,NaOH可能存在 |
| B.NaOH、CuSO4一定不存在 |
| C.K2SO4、NaOH、CaCO3、BaCl2一定存在,CuSO4可能存在 |
| D.无色滤液C含两种溶质 |
您最近半年使用:0次
2023-11-01更新
|
353次组卷
|
3卷引用:湖南省常德市第一中学2023-2024学年高一上学期期中考试化学试题
6 . 随着现代工业的发展,人类生活水平的提高,生活中产生的废铜合金垃圾越来越多,为了变废为宝,工业上一种利用废铜合金(主要成分:Cu、Fe、Al的单质及少量氧化物)制备胆矾( )的流程如下:
)的流程如下:
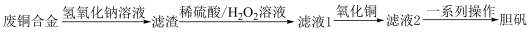
回答下列问题:
(1)废铜合金在反应前需要粉碎,目的是___________ ,将其先溶于氢氧化钠溶液,目的是___________ ,实验室中上述四步操作都需要的玻璃仪器名称是___________ 。
(2)写出第二步中铜与稀硫酸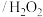 溶液反应的离子方程式:
溶液反应的离子方程式:___________ 。
(3)加入氧化铜的目的是除铁,检验铁离子是否除尽的试剂是___________ (填化学式)。一系列操作包括___________ 、过滤、洗涤、干燥。
(4)上述流程同时能够得到的副产品有___________ (填化学式)。若用100g废铜合金经上述转化,最后得到胆矾300g,___________ (填“能”或“不能”)据此求出废铜合金中铜元素的百分含量。
 )的流程如下:
)的流程如下: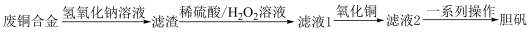
回答下列问题:
(1)废铜合金在反应前需要粉碎,目的是
(2)写出第二步中铜与稀硫酸
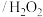 溶液反应的离子方程式:
溶液反应的离子方程式:(3)加入氧化铜的目的是除铁,检验铁离子是否除尽的试剂是
(4)上述流程同时能够得到的副产品有
您最近半年使用:0次
7 . 下列物质的主要化学成分不正确的是
| A.水晶:SiO2 | B.不锈钢: Fe—Cr—Ni合金 |
| C.生石膏 :2CaSO4•H2O | D.黄铜矿:CuFeS2 |
您最近半年使用:0次
解题方法
8 . 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值。但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)某青铜器中 Sn、Pb的质量分别为 119g、20.7g,则该青铜器中 Sn和Pb原子的数目之比为___________ 。
(2)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分 CuCl发生复分解反应,该化学方程式为___________ 。
(3)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
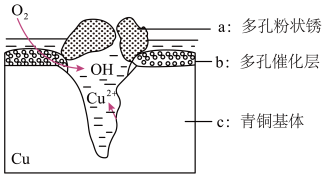
①腐蚀过程中, 负极是___________ (填“a”或“b”或“c”);
②环境中的 Cl⁻扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状铜锈Cu2(OH)3Cl,其离子方程式为___________ 。
(1)某青铜器中 Sn、Pb的质量分别为 119g、20.7g,则该青铜器中 Sn和Pb原子的数目之比为
(2)采用“局部封闭法”可以防止青铜器进一步被腐蚀。如将糊状Ag2O涂在被腐蚀部位,Ag2O与有害组分 CuCl发生复分解反应,该化学方程式为
(3)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中, 负极是
②环境中的 Cl⁻扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状铜锈Cu2(OH)3Cl,其离子方程式为
您最近半年使用:0次
名校
9 . 下列图示与对应的叙述不相符的是
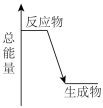 | 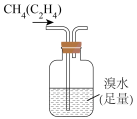 | 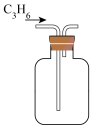 |  |
A.稀盐酸与 溶液反应的能量变化 溶液反应的能量变化 | B.除去 中少量的 中少量的 | C.收集 | D.新制 的制备 的制备 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-06-02更新
|
56次组卷
|
2卷引用:湖南省衡阳市三校2022-2023学年高一下学期6月期末联考化学试题
10 . 中国古代诗词和书籍中蕴含着化学知识。下列说法错误的是
| A.“白玉金边素瓷胎,雕龙描凤巧安排”,陶瓷材料是人类应用最早的硅酸盐材料 |
| B.“忽闻海上有仙山,山在虚无缥缈间”,海市蜃楼是一种自然现象,与胶体知识有关 |
| C.“九秋风露越窑开,夺得千峰翠色来”,“翠色”来自氧化亚铜 |
| D.镀金时“以汞和金涂银器上,入火则汞去,而金存”,其中“入火则汞去”指汞的挥发 |
您最近半年使用:0次
2023-06-01更新
|
524次组卷
|
5卷引用:湖南省部分学校2023-2024学年高三上学期第二次联考化学试题



