解题方法
1 . 为探索某工厂的废金属屑(主要成分为Fe、Cu、Al、Al2O3、Fe2O3等)的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的合金废料制取氯化铝、胆矾晶体(CuSO4·5H2O,M=250g/mol)和水处理剂高铁酸钾(K2FeO4)
(1)试剂X是___________ ;试剂Y是___________ 。
(2)分离溶液A和固体B的操作中,所需要的玻璃仪器除了烧杯外还需要___________ 。
(3)写出溶液A转化为固体C的离子方程式___________ 。
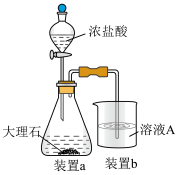
(4)在步骤Ⅱ时,小组成员小明用下图装置进行试验,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,你的建议是___________ 。___________ 。___________ 。
(7)该小组同学取用100.0g该废金属屑,经过实验,最终得到胆矾晶体25.0g,该废料中铜的质量分数约为___________ 。

(1)试剂X是
(2)分离溶液A和固体B的操作中,所需要的玻璃仪器除了烧杯外还需要
(3)写出溶液A转化为固体C的离子方程式
(4)在步骤Ⅱ时,小组成员小明用下图装置进行试验,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,你的建议是
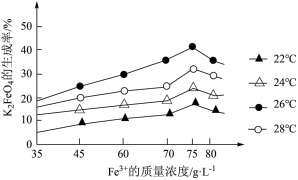
(7)该小组同学取用100.0g该废金属屑,经过实验,最终得到胆矾晶体25.0g,该废料中铜的质量分数约为
您最近半年使用:0次
2 . 某实验小组的同学为了探究CuSO4溶液与Na2CO3溶液的反应原理并验证产物,进行如下实验。
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
(2)为进一步确定蓝绿色固体的组成,使用如下装置再进行定量实验。

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是________________ ,装置E的作用是____________________ ,反应结束时要通入适量的空气,其作用是____________________________________ 。
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为____________ 。
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式______________ 。
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是_________________________ 。
(5)有同学为了降低实验误差,提出如下建议,其中合理的是______ (填字母序号)。
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
实验I:将CuSO4溶液与Na2CO3溶液混合,一定温度下充分反应至不产生气泡为止,
过滤、冷水洗涤、低温干燥,得到蓝绿色固体。该小组同学猜想此固体为xCuCO3·yCu(OH)2。
(1)为了验证猜想,先进行定性实验。
| 实验序号 | 实验步骤 | 实验现象 | 结论 |
| 实验Ⅱ | 取适量蓝绿色固体,加入足量稀硫酸 | 固体溶解,生成蓝色溶液, | 蓝绿色固体中含有CO32- |

实验Ⅲ:称取5.190g样品,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置C和D中。
①装置C中盛放的试剂是
②实验结束后,测得装置C增重0.270g,装置D增重1.320g。则该蓝绿色固体的化学式为
(3)若x=y=1,写出CuSO4溶液与Na2CO3溶液混合时反应的化学方程式
(4)已知20℃时溶解度数据:S[Ca(OH)2] =" 0.16" g,S[Ba(OH)2] =" 3.89" g。有同学据此提出可将装置D中的澄清石灰水换成等体积的饱和Ba(OH)2溶液,其可能的依据之一是
(5)有同学为了降低实验误差,提出如下建议,其中合理的是
A.加热装置B前,先通空气一段时间后再称量C、D的初始质量
B.将D换为盛有碱石灰的U形管
C.将C、D颠倒并省去E装置
您最近半年使用:0次
名校
解题方法
3 . 碱式碳酸铜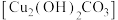 是孔雀石的主要成分,呈暗绿色或淡蓝绿色,难溶于水。某研究性学习小组制定了如下实验来探究制备碱式碳酸铜的最佳配比:将浓度均为
是孔雀石的主要成分,呈暗绿色或淡蓝绿色,难溶于水。某研究性学习小组制定了如下实验来探究制备碱式碳酸铜的最佳配比:将浓度均为 的
的 、
、 溶液混合,磁力搅拌30分钟后置于75℃恒温装置中反应75分钟,冷却至室温后抽滤、洗涤、干燥、称重。实验数据如下表所示。
溶液混合,磁力搅拌30分钟后置于75℃恒温装置中反应75分钟,冷却至室温后抽滤、洗涤、干燥、称重。实验数据如下表所示。
回答下列问题:
(1)本实验中,制备碱式碳酸铜的离子方程式为___________ 。
(2)实现恒温75℃加热可采取的方式为___________ 。
(3)实验过程中,需对碱式碳酸铜沉淀进行抽滤(减压过滤),装置如图甲,抽滤的主要优点是___________ ;检验滤渣是否洗涤干净的实验操作是___________ 。

(4)由以上实验数据判断,生成碱式碳酸铜的反应中, 的最佳比例为
的最佳比例为___________ ;在该比例下,碱式碳酸铜的产率为___________ (保留2位有效数字)。
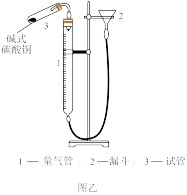
(5)取mg制得的碱式碳酸铜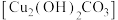 样品,在如图乙装置中加热分解(加热装置已省略),量气管及导管内盛装的试剂为
样品,在如图乙装置中加热分解(加热装置已省略),量气管及导管内盛装的试剂为___________ ,若收集到气体体积为VL(已折算成标准状况下),则样品中 的纯度为
的纯度为___________ %(用含m、V的式子表示)。
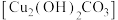 是孔雀石的主要成分,呈暗绿色或淡蓝绿色,难溶于水。某研究性学习小组制定了如下实验来探究制备碱式碳酸铜的最佳配比:将浓度均为
是孔雀石的主要成分,呈暗绿色或淡蓝绿色,难溶于水。某研究性学习小组制定了如下实验来探究制备碱式碳酸铜的最佳配比:将浓度均为 的
的 、
、 溶液混合,磁力搅拌30分钟后置于75℃恒温装置中反应75分钟,冷却至室温后抽滤、洗涤、干燥、称重。实验数据如下表所示。
溶液混合,磁力搅拌30分钟后置于75℃恒温装置中反应75分钟,冷却至室温后抽滤、洗涤、干燥、称重。实验数据如下表所示。| 实验编号 | I | II | III | IV | V |
 体积/mL 体积/mL | 30 | 30 | 30 | 30 | 30 |
 体积/mL 体积/mL | 24 | 30 | 36 | 42 | 48 |
| 产物成分 | 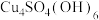 | 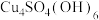  |  |  |  |
| 产物质量/g | 1.4725 | 1.5218 | 1.5473 | 1.5357 | 1.5315 |
(1)本实验中,制备碱式碳酸铜的离子方程式为
(2)实现恒温75℃加热可采取的方式为
(3)实验过程中,需对碱式碳酸铜沉淀进行抽滤(减压过滤),装置如图甲,抽滤的主要优点是

(4)由以上实验数据判断,生成碱式碳酸铜的反应中,
 的最佳比例为
的最佳比例为(5)取mg制得的碱式碳酸铜
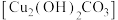 样品,在如图乙装置中加热分解(加热装置已省略),量气管及导管内盛装的试剂为
样品,在如图乙装置中加热分解(加热装置已省略),量气管及导管内盛装的试剂为 的纯度为
的纯度为
您最近半年使用:0次
2022-08-21更新
|
522次组卷
|
3卷引用:云南省昆明市第一中学2022-2023学年高三上学期第一次摸底测试化学试题
云南省昆明市第一中学2022-2023学年高三上学期第一次摸底测试化学试题(已下线)云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题云南师范大学附属中学2023-2024学年高三上学期开学考试化学试题



