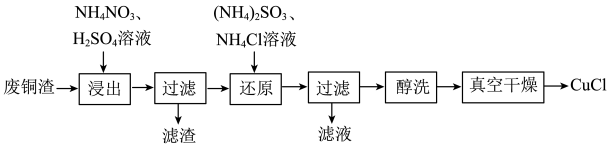
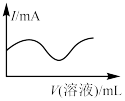1 . 氯化亚铜(CuCl)微溶于水,难溶于乙醇,易被氧化,广泛应用于医药、有机合成催化剂等工业。以废铜渣(主要含Cu、CuO,还有少量其他难溶物)为原料制备CuCl的工艺流程如图所示。 被还原为
被还原为 ,该过程中发生氧化还原反应的离子方程式为
,该过程中发生氧化还原反应的离子方程式为____________ 。
(2)若“浸出”过程中0.2 mol 参加反应时,转移1 mol电子,则还原产物为
参加反应时,转移1 mol电子,则还原产物为______ (填化学式)。
(3)“还原”过程中逐滴加入 、
、 溶液,初始时生成沉淀反应的离子方程式是
溶液,初始时生成沉淀反应的离子方程式是____________ 。“还原”过程中 溶液加入至过量的原因:一是让
溶液加入至过量的原因:一是让 全部被还原,二是
全部被还原,二是____________ 。
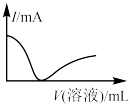
(4)“还原”过程中加入 溶液的体积(V)与溶液pH的关系如图所示。
溶液的体积(V)与溶液pH的关系如图所示。 溶液体积大于一定量时,溶液pH增大的原因是
溶液体积大于一定量时,溶液pH增大的原因是____________ 。
(5)用无水乙醇洗涤CuCl的优点是____________ (填一条)。
 被还原为
被还原为 ,该过程中发生氧化还原反应的离子方程式为
,该过程中发生氧化还原反应的离子方程式为(2)若“浸出”过程中0.2 mol
 参加反应时,转移1 mol电子,则还原产物为
参加反应时,转移1 mol电子,则还原产物为(3)“还原”过程中逐滴加入
 、
、 溶液,初始时生成沉淀反应的离子方程式是
溶液,初始时生成沉淀反应的离子方程式是 溶液加入至过量的原因:一是让
溶液加入至过量的原因:一是让 全部被还原,二是
全部被还原,二是(4)“还原”过程中加入
 溶液的体积(V)与溶液pH的关系如图所示。
溶液的体积(V)与溶液pH的关系如图所示。
 溶液体积大于一定量时,溶液pH增大的原因是
溶液体积大于一定量时,溶液pH增大的原因是(5)用无水乙醇洗涤CuCl的优点是
您最近半年使用:0次
名校
2 . 工业上制备下列物质的生产流程不合理的是
A.以废铜屑制硝酸铜: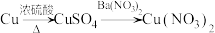 |
B.由黄铁矿制硫酸: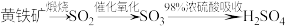 |
C.工业制硝酸: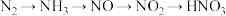 |
D.由石英砂制高纯硅: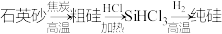 |
您最近半年使用:0次
3 . 向一定量的CuSO4溶液中逐滴加入Ba(OH)2溶液至沉淀刚好不再增加,然后再逐滴加入稀盐酸至过量,下列各项中的曲线可近似表示整个过程中混合溶液的导电能力(用电流强度I表示)变化的是
|
|
|
|
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
4 . 电镀废水中常含有阴离子A,排放前可加 溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验:
溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验:
(1)组成B的三种元素为______ ,黑色固体E的化学式为______ 。
(2)气体F的结构式______ ,阴离子A的电子式______
(3)沉淀B隔绝空气加热分解的化学方程式是______
(4)固体C在沸腾的稀盐酸中会生成一种弱酸和一种白色沉淀,该白色沉淀是共价化合物(测其分子量为99.5),则反应的化学方程式是______ 。
 溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验:
溶液处理,使之转化为沉淀B。取一定质量沉淀B按如图流程进行实验: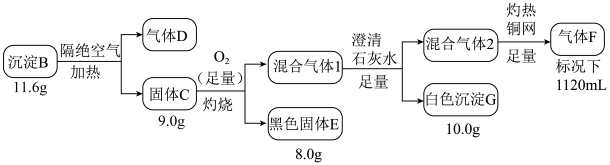
(1)组成B的三种元素为
(2)气体F的结构式
(3)沉淀B隔绝空气加热分解的化学方程式是
(4)固体C在沸腾的稀盐酸中会生成一种弱酸和一种白色沉淀,该白色沉淀是共价化合物(测其分子量为99.5),则反应的化学方程式是
您最近半年使用:0次
5 . 某工厂的固体废渣中主要含 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
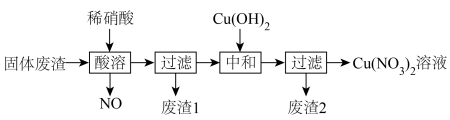
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
已知: 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。___________ 写出 与稀硝酸反应的离子反应方程式
与稀硝酸反应的离子反应方程式___________ 。
(2)酸溶时,反应温度不宜超过 ,其主要原因是
,其主要原因是___________ 。
(3)废渣1主要成分为___________ 。
(4)酸溶时产生的NO在一定条件下可以用氨气转化为对环境无害的物质,该反应中氧化剂和还原剂的物质的量之比为___________ 。
 和
和 ,还含有少量
,还含有少量 和
和 。利用该固体废渣制取
。利用该固体废渣制取 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:已知:
 在酸性溶液中不稳定,会转变成
在酸性溶液中不稳定,会转变成 和
和 。
。
 与稀硝酸反应的离子反应方程式
与稀硝酸反应的离子反应方程式(2)酸溶时,反应温度不宜超过
 ,其主要原因是
,其主要原因是(3)废渣1主要成分为
(4)酸溶时产生的NO在一定条件下可以用氨气转化为对环境无害的物质,该反应中氧化剂和还原剂的物质的量之比为
您最近半年使用:0次
名校
6 . 在中华文明的历史长河中,江西人才辈出,文化璀璨,下列说法正确的是
| A.“落木千山天远大,澄江一道月分明”,月亮倒映在江水中的现象属于丁达尔效应 |
B.白鹿洞书院建筑群易受酸雨腐蚀, 的雨水为酸雨 的雨水为酸雨 |
C.“庐山山南刷铜绿”,“铜绿”的主要成分为 |
| D.“白如玉,明如镜,薄如纸,声如馨”的景德镇白瓷的主要成分为无机硅酸盐材料 |
您最近半年使用:0次
名校
7 . 下列物质对应的化学式不正确的是
| A.干冰:CO2 | B.金刚砂:SiC |
| C.胆矾:CuSO4·5H2O | D.重晶石:CaSO4 |
您最近半年使用:0次
名校
8 . 硝酸铜是一种重要的化工原料,可由工业含铜废料制备,含铜废料的主要成分为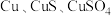 等,制备流程如图所示:
等,制备流程如图所示:
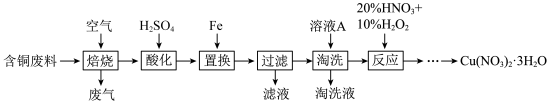
回答下列问题:
(1)焙烧时, 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)“淘洗”所用的溶液A可以是___________ 。(填标号)。
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。
①理论上反应所消耗的 和
和 的物质的量之比为
的物质的量之比为___________ 。
②若不加10%的 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为___________ 。
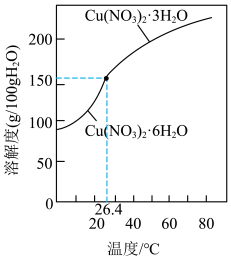
③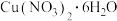 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是___________ 。
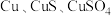 等,制备流程如图所示:
等,制备流程如图所示:
回答下列问题:
(1)焙烧时,
 与空气中的
与空气中的 反应生成
反应生成 和
和 ,该反应的化学方程式为
,该反应的化学方程式为(2)“淘洗”所用的溶液A可以是
a.稀硝酸 b.浓硝酸 c.稀硫酸 d.浓硫酸
(3)“反应”阶段所用的试剂是20%的
 溶液和10%的
溶液和10%的 溶液,反应过程中无红棕色气体生成。
溶液,反应过程中无红棕色气体生成。①理论上反应所消耗的
 和
和 的物质的量之比为
的物质的量之比为②若不加10%的
 溶液,只用20%的
溶液,只用20%的 溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为
溶液,随着反应的进行,温度上升并出现大量红棕色气体,反应的离子方程式为③
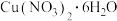 和
和 的溶解度如图所示。从“反应”阶段所得溶液中析出
的溶解度如图所示。从“反应”阶段所得溶液中析出 的方法是
的方法是
您最近半年使用:0次
9 . 红珊瑚栖息于200~2000米深的海域,它与琥珀、珍珠统称为有机宝石,红珊瑚是由无数珊瑚虫分泌的石灰质大量堆积形成的干支状物,呈红色是因为在海底长期积淀某种元素的氧化物。该元素可能是
| A.Na | B.Fe | C.Si | D.Cu |
您最近半年使用:0次
解题方法
10 . 下列反应的离子方程式书写正确的是
A.碳酸钙与稀盐酸反应: +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
| B.金属钠加入硫酸铜溶液的反应中:2Na+CuSO4=Na2SO4+Cu |
| C.铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
| D.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
您最近半年使用:0次