1 . 以高氯冶炼烟灰(主要成分为铜锌的氯化物、氧化物、硫酸盐,少量铁元素和砷元素)为原料,可回收制备Cu和ZnSO4·H2O,其主要实验流程如下:

已知:砷元素进入水体中对环境污染大,可通过沉淀法除去。
(1)两段脱氯均需在85 ℃条件下进行,适宜的加热方式为_________ 。
(2)碱洗脱氯时,溶液中Cu2+主要转化为Cu(OH)2和Cu2(OH)2CO3,也会发生副反应得到Cu2(OH)3Cl沉淀并放出气体,该副反应的离子方程式为_________ 。若用NaOH溶液进行碱洗操作时,浓度不宜过大,通过下表的数据分析其原因是______________ 。
(3)滤液1和滤液2中含一定量的Cu2+、Zn2+。为提高原料利用率,可采取的措施有:将滤液1和滤液2混合,回收铜锌沉淀物;循环使用电解过程产生的________ (填化学式)。
(4)某化学兴趣小组要以硫酸锌溶液(含少量硫酸亚铁杂质)制备氧化锌。已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)
实验中可选用的试剂:30% H2O2、1.0 mol·L-1HNO3、1.0 mol·L-1 NaOH。实验步骤依次为:_______ ;过滤;_______ ;过滤、洗涤、干燥;900℃煅烧,得到氧化锌。

已知:砷元素进入水体中对环境污染大,可通过沉淀法除去。
(1)两段脱氯均需在85 ℃条件下进行,适宜的加热方式为
(2)碱洗脱氯时,溶液中Cu2+主要转化为Cu(OH)2和Cu2(OH)2CO3,也会发生副反应得到Cu2(OH)3Cl沉淀并放出气体,该副反应的离子方程式为
NaOH溶液浓度对脱氯率和其他元素浸出率的影响 | ||||
NaOH浓度/mol•L-1 | 脱氯率/% | 元素浸出率/% | ||
Cl | Zn | Cu | As | |
1.0 | 51.20 | 0.51 | 0.04 | 0.00 |
2.0 | 80.25 | 0.89 | 0.06 | 58.87 |
3.0 | 86.58 | 7.39 | 0.26 | 78.22 |
(4)某化学兴趣小组要以硫酸锌溶液(含少量硫酸亚铁杂质)制备氧化锌。已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-。下表列出了几种离子生成氢氧化物沉淀pH(开始沉淀的pH按金属离子浓度为1.0 mol·L-1计算)
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
您最近一年使用:0次
名校
解题方法
2 . 歌曲《青花瓷》,唱道“帘外芭蕉惹骤雨,门环惹铜绿”,其中的“铜绿”即是铜锈,它的化学成分是 (碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为
(碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为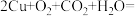
 。下列有关该反应的说法正确的是( )
。下列有关该反应的说法正确的是( )
 (碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为
(碱式碳酸铜)。铜在潮湿的空气中生锈的化学反应为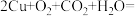
 。下列有关该反应的说法正确的是( )
。下列有关该反应的说法正确的是( )| A.该反应不属于氧化还原反应 | B.该反应中氧元素和碳元素化合价发生变化 |
C.该反应中 是酸性氧化物 是酸性氧化物 | D.该反应中 是酸式盐 是酸式盐 |
您最近一年使用:0次
2020-12-18更新
|
185次组卷
|
5卷引用:江苏省扬州市高邮临泽中学2020-2021学年高一下学期开学考化学试题
10-11高一上·浙江绍兴·期中
3 . 取一定量的CuO粉末与0.5 L稀硫酸充分反应后,将一根50 g铁棒插入上述溶液中,至铁棒质量不再变化时,铁棒增重0.24 g, 并收集到224 mL气体(标准状况)。求此CuO粉末的质量____ 。
您最近一年使用:0次
名校
4 . 氯化亚铜(CuCl)常用作催化剂、杀菌剂等。
(1)将Na2SO3溶液逐滴加入到CuCl2溶液中,再加入少量浓盐酸混匀,得到CuCl沉淀。写出该反应的离子方程式____________________________ 。
(2)为测定制得CuCl样品的纯度,进行下列实验:
a.称取0.5000 g样品,放入盛有20 mL过量FeCl3 溶液和玻璃珠的锥形瓶中,不断摇动;
b.待样品溶解后,加水50 mL;
c.立即用0.2000 mol/LCe(SO4)2标准溶液滴至反应完全,记录消耗标准溶液的体积;
d.重复步骤a至c操作2次,记录消耗标准溶液的平均体积为25.00 mL。已知:CuC1+Fe3+=Cu2++Fe2++Cl-、 Fe2++Ce4+=Fe3++Ce3+
①配制100 mL 0.2000 mol/L的Ce(SO4)2标准溶液时,需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管,还需要______________ 。
②进行步骤c时若操作缓慢,则测得CuCl的纯度________ (填“偏大”、“偏小”或“无影响”)。
③通过计算确定该样品中CuCl的纯度_____________ (写出计算过程)。
(1)将Na2SO3溶液逐滴加入到CuCl2溶液中,再加入少量浓盐酸混匀,得到CuCl沉淀。写出该反应的离子方程式
(2)为测定制得CuCl样品的纯度,进行下列实验:
a.称取0.5000 g样品,放入盛有20 mL过量FeCl3 溶液和玻璃珠的锥形瓶中,不断摇动;
b.待样品溶解后,加水50 mL;
c.立即用0.2000 mol/LCe(SO4)2标准溶液滴至反应完全,记录消耗标准溶液的体积;
d.重复步骤a至c操作2次,记录消耗标准溶液的平均体积为25.00 mL。已知:CuC1+Fe3+=Cu2++Fe2++Cl-、 Fe2++Ce4+=Fe3++Ce3+
①配制100 mL 0.2000 mol/L的Ce(SO4)2标准溶液时,需要的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管,还需要
②进行步骤c时若操作缓慢,则测得CuCl的纯度
③通过计算确定该样品中CuCl的纯度
您最近一年使用:0次
名校
解题方法
5 . 下列变化不能通过一步化学反应实现的是( )
| A.BaCl2→BaSO4 | B.CuO→Cu(OH)2 | C.NaOH→Na2SO3 | D.MgSO4→Mg(OH)2 |
您最近一年使用:0次
2020-09-10更新
|
2513次组卷
|
31卷引用:江苏省启东中学2020-2021学年高一上学期期初考试化学试题
江苏省启东中学2020-2021学年高一上学期期初考试化学试题贵州省桐梓县育才中学2019-2020学年高二上学期开学考试化学试题辽宁省阜新市海州高级中学2019-2020学年高一10月月考化学试题2020年春季苏教版高中化学必修1专题一《化学家眼中的物质世界》测试卷云南省昭通市巧家县第四中学2019-2020学年高一上学期期末考试化学试题人教版(2019)高一必修第一册第一章 物质及其变化 第一节 物质的分类及转化课时2 物质的转化(已下线)1.1.2 物质的转化(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)高一必修第一册(苏教2019版)专题1 第一单元 物质及其反应的分类(已下线)【浙江新东方】hzomo化学001云南省昆明师范专科学校附属中学2020-2021学年高一上学期期中考试化学试题广西岑溪市2020-2021学年高二上学期期中考试化学(理)试题(已下线)【浙江新东方】【2020】【高一上】【期中】【hd-lp414】【化学】黑龙江省海林市朝鲜族中学2020-2021学年高一上学期第一次月考化学试题江苏省淮安市涟水县第一中学2022-2023学年高一上学期第二次阶段检测化学试题新疆维吾尔族自治区哈密市第十五中学2020-2021学年高一上学期期末考试化学试题辽宁省庄河市高级中学2021-2022学年高一10月月考化学试题山东省济南市平阴县第一中学2021-2022学年高一上学期10月阶段检测化学试题福建省南安市侨光中学2021-2022学年高一上学期第一次阶段考化学试题甘肃省甘南舟曲县第一中学2021-2022学年高一上学期第一次月考化学试卷新疆维吾尔自治区疏勒县2022 届高三第一次调研测试化学试题(已下线)专题05元素及其化合物-2022年高考真题+模拟题汇编(全国卷)(已下线)专题05元素及其化合物-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题05元素及其化合物-五年(2018~2022)高考真题汇编(全国卷)(已下线)衔接点05 物质间的相互转化-2022年初升高化学无忧衔接青海省西宁市湟中区多巴高级中学2021-2022学年高一下学期第一次月考化学试题河南省许昌市鄢陵县职业教育中心2021—2022学年高一上学期升学班第一次月考化学试题广西梧州市藤县第七中学2021-2022学年高一10月月考化学试题黑龙江省佳木斯市第八中学2021-2022学年高一上学期期中考试化学试题吉林省舒兰市第十八中学校2022-2023学年高一上学期期中考试化学试题(已下线)第2讲 物质的转化-【暑假自学课】2023年新高一暑假精品课(苏教版2019必修第一册)广东省梅州市大埔县虎山中学2023-2024学年高一上学期11月期中化学试题
6 . (1)称量一定质量表面含油污的纯铜屑(铜含量为99.84%),置于坩埚中灼烧,将油污充分氧化后除去,直至铜屑表面均呈黑色。冷却后称量,固体质量比灼烧前增加了3.2 %,固体中铜与氧化铜的质量之比为_______。(请将结果化为小数,且保留至小数点后两位)
(2)向1000克未知溶质质量分数的硫酸铜溶液中加入一定量的氢氧化钠溶液,过滤、干燥后得到蓝色固体19.6克。在所得滤液中加入过量铁粉,充分反应后,再加入足量盐酸,最后得到6.4克固体,求原溶液中硫酸铜的质量分数。(请写出计算过程)
(2)向1000克未知溶质质量分数的硫酸铜溶液中加入一定量的氢氧化钠溶液,过滤、干燥后得到蓝色固体19.6克。在所得滤液中加入过量铁粉,充分反应后,再加入足量盐酸,最后得到6.4克固体,求原溶液中硫酸铜的质量分数。(请写出计算过程)
您最近一年使用:0次
名校
解题方法
7 . 实验室利用下列实验装置来测定铜的氧化物CuXO的组成。
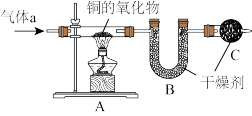
(1)若气体a为纯净的氢气,在点燃A装置中酒精灯以前,要将氢气通过整个装置一段时间,其目的是__ 。
(2)若气体a为纯净的氢气,当铜的氧化物CuXO完全被还原为Cu时,称得Cu的质量为6.4g,同时称得B装置的质量增加了0.9克,则这种铜的氧化物中铜元素和氧元素的原子个数之比的原始计算式为_____ ,该铜的氧化物的化学式为____ 。
(3)若气体a为混有少量H2O(g)的氢气,而又未经干燥处理直接通至装置A中,当铜的氧化物CuXO完全被还原为Cu时,仍然利用称量Cu的质量和B装置增加的质量的方法来完成这个实验,将使测定结果中铜元素与氧元素质量之比的值(选填“偏大”、“偏小”或“不受影响”)_____ 。
(4)若气体a为混有少量H2O(g)的氢气,不增加任何其他实验装置也不改动上述装置的连接顺序,仍用其来测定CuXO的组成,必须测得哪些数据才能得到x的值?___

(1)若气体a为纯净的氢气,在点燃A装置中酒精灯以前,要将氢气通过整个装置一段时间,其目的是
(2)若气体a为纯净的氢气,当铜的氧化物CuXO完全被还原为Cu时,称得Cu的质量为6.4g,同时称得B装置的质量增加了0.9克,则这种铜的氧化物中铜元素和氧元素的原子个数之比的原始计算式为
(3)若气体a为混有少量H2O(g)的氢气,而又未经干燥处理直接通至装置A中,当铜的氧化物CuXO完全被还原为Cu时,仍然利用称量Cu的质量和B装置增加的质量的方法来完成这个实验,将使测定结果中铜元素与氧元素质量之比的值(选填“偏大”、“偏小”或“不受影响”)
(4)若气体a为混有少量H2O(g)的氢气,不增加任何其他实验装置也不改动上述装置的连接顺序,仍用其来测定CuXO的组成,必须测得哪些数据才能得到x的值?
您最近一年使用:0次
名校
解题方法
8 . 下列有关物质性质与用途具有对应关系的是( )
| A.硅酸钠溶液呈碱性,可用作木材防火剂 |
| B.硫酸铜溶液呈蓝色,可用作游泳池中水的消毒剂 |
| C.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
| D.铅具有还原性和导电性,可用作铅蓄电池的负极材料 |
您最近一年使用:0次
2020-06-09更新
|
231次组卷
|
2卷引用:江苏省南京市2020届高三第三次模拟考试(6月) 化学试题
名校
解题方法
9 . 对中国古代著作涉及化学的叙述,下列解读不正确 的是
| A.《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 |
| B.《黄白第十六》中“曾青涂铁,铁赤如铜”,其“曾青”是可溶性铜盐 |
| C.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3 |
| D.《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油 |
您最近一年使用:0次
2019-09-13更新
|
322次组卷
|
19卷引用:江苏省海安高级中学2019-2020学年高二上学期入学考试化学试题
江苏省海安高级中学2019-2020学年高二上学期入学考试化学试题江苏省启东中学2016-2017学年高一下学期期终化学试题2016届广东省肇庆高三第三次模拟考试理综化学试卷2017届河北省武邑中学高三上调研四化学试卷辽宁省沈阳铁路实验中学2016-2017学年高二下学期期末考试化学试题河北省辛集市第一中学2018届高三上学期第一次月考化学试题河北省衡水中学2018届高三上学期一调考试化学试题安徽省淮北市第一中学2017-2018学年高二上学期第二次月考化学试题新疆阿克苏市农一师中学2018届高三上学期第二次月考化学试题湖北省部分重点高中协作体2018届高三上学期期中联考化学试题黑龙江省哈尔滨师范大学附属中学2018届高三上学期期中考试化学试题安徽省六安市第一中学2018届高三上学期第五次月考化学试题江西省景德镇市第一中学2017-2018学年高一上学期期末考试化学试题湖南省醴陵市第二中学2019届高三上学期第一次月考化学试题【全国百强校】福建省三明市第一中学2019届高三上学期期中考试化学试题吉林省长春市市田家炳实验中学2019届高三上学期12月月考化学试题江西省金溪县第一中学2018届高三假期开学考试化学试题第30届( 2016年)全国中学生化学竞赛(安徽赛区)初赛试题(已下线)课时02 化学与传统文化-2022年高考化学一轮复习小题多维练(全国通用)
10 . 用某铜矿(含CuS以及少量FeO和Fe2O3)制备CuCl的主要流程如下:
已知Fe3+、Mn2+、Cu2+生成氢氧化物沉淀时的pH如下表所示:
(1)浸取时,CuS被浸取的离子方程式为CuS+MnO2+4H+=Cu2++Mn2++S↓+2H2O,该反应的氧化剂是________ (填化学式),Fe2O3被浸取的离子方程式为________________ 。
(2)步骤③调整pH的范围为______ ,滤渣A的成分为________ (填化学式)。
(3)“沉铁”时,需要检验Fe3+是否沉淀完全,所用的试剂为________ (填化学式)。
(4)准确称取所制备的氯化亚铜样品1.600 g,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用0.100 0 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液25.00 mL,反应中Cr2O72-被还原为Cr3+,计算样品中CuCl的质量分数(写出计算过程)______ 。
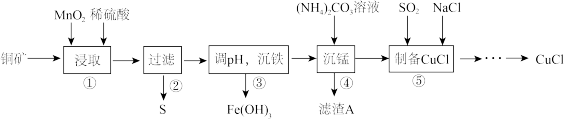
已知Fe3+、Mn2+、Cu2+生成氢氧化物沉淀时的pH如下表所示:
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mn(OH)2 | 7.1 | 10.1 |
| Cu(OH)2 | 4.7 | 6.7 |
(2)步骤③调整pH的范围为
(3)“沉铁”时,需要检验Fe3+是否沉淀完全,所用的试剂为
(4)准确称取所制备的氯化亚铜样品1.600 g,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用0.100 0 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液25.00 mL,反应中Cr2O72-被还原为Cr3+,计算样品中CuCl的质量分数(写出计算过程)
您最近一年使用:0次



