第30届( 2016年)全国中学生化学竞赛(安徽赛区)初赛试题
安徽
高二
竞赛
2021-08-15
740次
整体难度:
适中
考查范围:
物质结构与性质、竞赛、化学反应原理、常见无机物及其应用、化学与STSE、化学实验基础、认识化学科学、有机化学基础
一、单选题 添加题型下试题
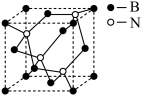
| A.纳米立方氮化硼属于离子晶体 |
| B.B和N之间可形成非极性共价键 |
| C.纳米立方氮化硼可用于钻探、切削工具 |
| D.25.0 g纳米立方氮化硼中含6.02×l023个原子 |
【知识点】 共价键的形成及主要类型解读 晶胞的有关计算解读 晶体
| A.溶液中水电离出的H+个数:② > ① |
| B.溶液中阴离子的总物质的量浓度之和① > ② |
| C.①溶液中:n(OH-)-n(H+)=n(HCO3-)+ 2n(H2CO3) |
| D.②溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |

| A.电极a为阴极,放出H2 |
| B.通电一段时间后,硫酸溶液的pH升高 |
| C.A-通过阴离子交换膜从阴极进入浓缩室 |
| D.对400mLl0g/L乳酸溶液通电后,当外电路通过0.5mole-时浓度,上升为145g.L-1(溶液体积变化忽略不计) |
| A.《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 |
| B.《黄白第十六》中“曾青涂铁,铁赤如铜”,其“曾青”是可溶性铜盐 |
| C.《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的碱是K2CO3 |
| D.《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的是石油 |
二、多选题 添加题型下试题
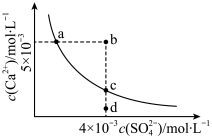
| A.a、c两点均可以表示常温下CaSO4在水溶液中形成的饱和溶液 |
| B.a点对应的Ksp等于c点对应的Ksp |
C.b点将有沉淀生成,平衡后溶液中c(SO )一定等于3×10-3mol·L-1 )一定等于3×10-3mol·L-1 |
| D.向d点溶液中加入适量CaCl2固体可以变到c点 |
三、单选题 添加题型下试题
| 操作和现象 | 结 论 | |
| A | 向盛有2mL 0.1mol/L AgNO3溶液的试管中,先滴几滴0.1mol/L KCl溶液,再滴加0.1mol/L KI溶液。试管中先出现白色沉淀,后出现淡黄色沉淀 | Ksp(AgCl)< Ksp(AgI) |
| B | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
| C | 在分液漏斗中加入碘水后再加入CCl4,充分振荡,分层,下层溶液呈紫色 | CCl4可作为碘的萃取剂 |
| D | 测定饱和NaClO溶液、CH3COONa溶液的pH,pH(NaClO)> pH(CH3COONa) | 弱酸的酸性:HClO < CH3COOH |
| A.A | B.B | C.C | D.D |
【知识点】 沉淀转化解读 化学实验方案的设计与评价
 C12H26 + 2CO2↑+H2↑+2CH3ONa,下列说法不正确的是
C12H26 + 2CO2↑+H2↑+2CH3ONa,下列说法不正确的是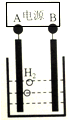
| A.图中电源的A极为直流电源的负极 |
| B.加入金属钠可以将酸转化为钠盐,提高离子浓度,增强导电性 |
| C.阳极电极反应为:2C6H13COO- -2e- =C12H26 + 2CO2↑ |
| D.反应一段时间后将电源正负极反接,会产生杂质影响正十二烷的制备 |
A.0.1mol·L-1FeCl3溶液中:Fe2+、NH 、SCN-、SO 、SCN-、SO |
B.室温下,pH=1的溶液中:Na+、Fe3+、NO 、SO 、SO |
C.加入铝粉有气泡产生的溶液中:Na+、NH 、Fe2+、NO 、Fe2+、NO |
D.在AlCl3溶液中:K+、Na+、HCO 、SO 、SO |
【知识点】 酸碱理论和水溶液中的离子平衡
①
 ②
②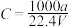
③上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
④上述溶液中再加入1.5VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:
c(Cl-)> c(NH4+) > c(H+) > c(OH-)
| A.①④ | B.②③ | C.①③ | D.②④ |
| A.氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl- |
| B.硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
| C.向氢氧化亚铁中加入足量稀硝酸:Fe(OH)2+2H+=Fe2++2H2O |
| D.将过量二氧化硫气体通入冷氨水中:SO2+NH3·H2O=HSO3-+NH4+ |
| A.暖冰中水分子是直线型分子 |
| B.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
| C.暖冰中水分子的氧原子的杂化方式为sp |
| D.水凝固形成20℃时的“暖冰”所发生的变化是化学变化 |
【知识点】 氢键对物质性质的影响解读
| A.在恒压下,凡是自发的过程一定是放热的 |
| B.因为焓是状态函数,而恒压反应的焓变等于恒压反应热,所以热也是状态函数 |
C.单质的 和 和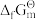 都为零 都为零 |
| D.在恒温恒压条件下,封闭体系自由能减少的过程是自发过程 |
| A.3,2,3 | B.4,3,2 | C.4,2,2 | D.4,2,3 |
【知识点】 分子结构
A.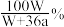 | B.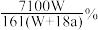 | C.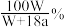 | D.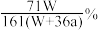 |
【知识点】 化学方程式计算中物质的量的运用解读 电化学计算 电化学 物质成分分析
| A.C6H5Cl | B.C6H5CH2Cl | C.(C6H5)2CHCl | D.(C6H5)3CCl |
【知识点】 分子的性质 键能、键长、键角及应用解读
A.I | B.I | C.CS2 | D.BeCl2 |
【知识点】 利用杂化轨道理论判断分子的空间构型解读 分子结构
四、多选题 添加题型下试题
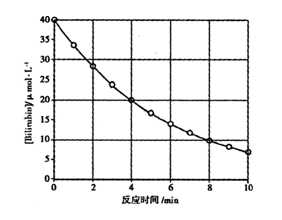
| A.2.5μ mol·L-1·min-1和2.0μ mol·L-1 |
| B.2.5μ mol·L-1·min-1和2.5μ mol·L-1 |
| C.该反应为零级反应 |
| D.该反应为一级反应 |
| A.2.8 g | B.4.2 g | C.5.6 g | D.11.2 g |
【知识点】 化学方程式计算中物质的量的运用解读 硝酸的强氧化性解读 氧化还原
五、单选题 添加题型下试题

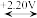 Fe3+
Fe3+ Fe2+
Fe2+ Fe,φ0(Cl2/Cl-)=+1.36V。下列有关说法正确的是
Fe,φ0(Cl2/Cl-)=+1.36V。下列有关说法正确的是| A.Fe2+在水溶液中可发生歧化反应 |
| B.无论在酸性或碱性条件下,Fe均可还原水 |
C.FeO 在水溶液中可稳定存在 在水溶液中可稳定存在 |
D.Cl2无论在何条件下均不能氧化Fe3+生成FeO |
| A.当溶液pH不变时,该反应一定达到平衡状态 |
| B.向该溶液中加水,平衡向正反应移动,K一定增大 |
| C.向该溶液中通入Cl2,平衡一定向正反应方向移动 |
| D.光照条件下HCl浓度增大,平衡一定向逆反应方向移动 |

| A.①⑤ | B.②④ | C.④⑤ | D.⑤⑥ |
六、多选题 添加题型下试题
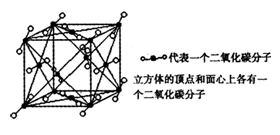
| A.每个晶胞含有4个CO2分子 |
| B.该晶胞属于面心立方晶胞 |
| C.晶胞中正四面体空隙数:正八面体空隙数=1:1 |
| D.每个CO2分子周围与之最近且等距离的CO2分子有12个 |
【知识点】 晶体
七、单选题 添加题型下试题
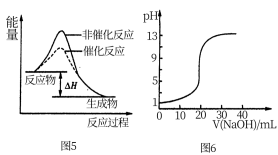
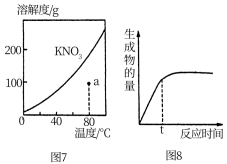
| A.图5表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图6表示0.1000mol•L-1NaOH溶液滴定20.00mL0.1000mol•L-1CH3COOH溶液所得到的滴定曲线 |
| C.图7表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D.图8 表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大 |
【知识点】 化学平衡图像分析 难溶电解质的溶解平衡
八、多选题 添加题型下试题
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A.反应在t1min内的平均速率为υ(H2)=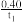 mol-1·L-1 ·min-1 mol-1·L-1 ·min-1 |
| B.保持其它条件不变,起始时向容器中充入0.60molCO和1.20molH2O,达到平衡时n(CO2)=0.40mol |
| C.保持其它条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 |
| D.温度升高至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
九、填空题 添加题型下试题
(1)将H2S通入酸性重铬酸钾溶液中
(2)在酸性高锰酸钾溶液中加入亚硫酸钠溶液
(3)在强碱性高锰酸钾溶液中,加入少量的亚硫酸钠溶液
(4)将氢氧化钾溶液缓慢加入到硫酸铬(Ⅲ)溶液中,直至过量。写出生成沉淀和反应最终的离子方程式
【知识点】 离子反应的发生及书写 氧化还原
(1)试写出A2B型离子化合物的离子式
(2)试画出A+与B2-离子团的空间几何构型(标出Sb原子上非键电子对)并指出构型中Sb原子的杂化类型
【知识点】 分子结构
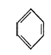 +3D2→
+3D2→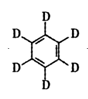 +3H2的反应中,使用的催化剂是
+3H2的反应中,使用的催化剂是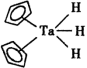 。
。(1)指出上述催化剂中Ta的配位数
(2)说明该催化剂不能直接参加催化反应的理由
(3)试用反应方程武将质给催化剂转变成活性催化剂,并指出该反应的类型
十、解答题 添加题型下试题
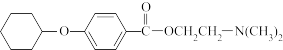 是一种麻醉剂,可以用
是一种麻醉剂,可以用 为原料经下列路线合成。
为原料经下列路线合成。
 (A)
(A)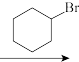 (B)
(B) 
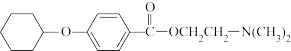
(1)请写出必要的试剂和中间产物(A)、(B)、(C)的结构式:A
(2)如用
 为原,加必要试剂合成HO-CH2CH2N(CH3)2
为原,加必要试剂合成HO-CH2CH2N(CH3)2【知识点】 根据题给物质选择合适合成路线解读 有机推断综合考查解读 有机化学
十一、填空题 添加题型下试题
十二、解答题 添加题型下试题
 ),(A)催化氢化得到(B)(C12H16O2)。(A)用碘和碳酸钾溶液处理得到碘仿和化合物(C)(C11H12O3),氧化(B)和(C)都得到酸(|D)(C9H10O3)。(D)用溴化氢处理得到另一个酸(E)(C7H6O3),(E)在水蒸气流中易挥发。试回答下列问题:
),(A)催化氢化得到(B)(C12H16O2)。(A)用碘和碳酸钾溶液处理得到碘仿和化合物(C)(C11H12O3),氧化(B)和(C)都得到酸(|D)(C9H10O3)。(D)用溴化氢处理得到另一个酸(E)(C7H6O3),(E)在水蒸气流中易挥发。试回答下列问题:(1)写出(A)—(E)的结构式:A
(2)将化合物(A)、(C)和(E)用系统命名法命名:A
(3)试说明(E)在水蒸气流中易挥发的原因
(4)化合物(C)和(E)中有无手性碳原子,若有,请用*符号表示出
十三、填空题 添加题型下试题
(1)计算此固体酸的溶解度
(2)计算此饱和溶液中酸根B-的分布分数
(3)已知HB中只含有C、H、O三种元素,其中C的质量分数为68.85%,H为4.95%,O为26.21%,写出此固体酸的分子式
(4)已知此固体酸含有苯环和Π
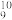 ,画出它的结构简式
,画出它的结构简式【知识点】 酸碱理论和水溶液中的离子平衡
(1)试画出该三元化合物晶体的晶胞图
 ,Si,
,Si, Li
Li )
)(2)硅原子占有铝原子围成的何类空隙中
(3)已知晶胞参数为5.93Å,试求颞与Al之间的共价键长
(4)试写出该晶体的结构基元的化学式
(5)指出该晶体的点阵型式
【知识点】 晶体
试卷分析
导出试卷题型(共 33题)
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 共价键的形成及主要类型 晶胞的有关计算 晶体 | |
| 2 | 0.4 | 盐类水解规律 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 3 | 0.65 | 电解原理的应用 电解池有关计算 | |
| 4 | 0.65 | 硫酸铜 化学科学对人类文明发展的意义 石油物理性质及组成成分 | |
| 6 | 0.4 | 沉淀转化 化学实验方案的设计与评价 | |
| 7 | 0.65 | 电解池电解基本判断 电解池电极反应式及化学方程式的书写与判断 电解原理的应用实验 | |
| 8 | 0.65 | 酸碱理论和水溶液中的离子平衡 | |
| 9 | 0.65 | 物质的量浓度的基础计算 物质的量浓度与溶质成分有关的计算 物质的量浓度与溶液稀释的计算 盐溶液中离子浓度大小的比较 | |
| 10 | 0.85 | 离子方程式的正误判断 氯气与还原性化合物的反应 氨水的性质 硝酸的强氧化性 酸性氧化物的通性 硅酸的制备 | |
| 11 | 0.65 | 氢键对物质性质的影响 | |
| 12 | 0.65 | 能量的相互转化 复合判据 化学热力学初步 | |
| 13 | 0.65 | 分子结构 | |
| 14 | 0.65 | 化学方程式计算中物质的量的运用 电化学计算 电化学 物质成分分析 | |
| 15 | 0.65 | 分子的性质 键能、键长、键角及应用 | |
| 16 | 0.65 | 利用杂化轨道理论判断分子的空间构型 分子结构 | |
| 19 | 0.15 | 氧化还原 电化学 | |
| 20 | 0.65 | 电子转移计算 | |
| 21 | 0.65 | 化学平衡状态的判断方法 浓度对化学平衡移动的影响 化学平衡常数的影响因素及应用 化学平衡 | |
| 22 | 0.65 | 核磁共振氢谱 | |
| 24 | 0.65 | 化学平衡图像分析 难溶电解质的溶解平衡 | |
| 二、多选题 | |||
| 5 | 0.65 | 同离子效应对难溶电解质溶解平衡的影响 溶度积常数相关计算 酸碱理论和水溶液中的离子平衡 | |
| 17 | 0.65 | 化学反应速率计算 化学平衡 | |
| 18 | 0.65 | 化学方程式计算中物质的量的运用 硝酸的强氧化性 氧化还原 | |
| 23 | 0.65 | 晶体 | |
| 25 | 0.4 | 化学反应速率计算 化学平衡的有关计算 化学平衡 | |
| 三、填空题 | |||
| 26 | 0.65 | 离子反应的发生及书写 氧化还原 | |
| 27 | 0.65 | 分子结构 | |
| 28 | 0.4 | 加成反应 消去反应 配合物的概念、组成及形成条件 有机化学 | |
| 30 | 0.65 | 有机化学 | |
| 32 | 0.65 | 酸碱理论和水溶液中的离子平衡 | |
| 33 | 0.65 | 晶体 | |
| 四、解答题 | |||
| 29 | 0.4 | 根据题给物质选择合适合成路线 有机推断综合考查 有机化学 | 有机推断题 |
| 31 | 0.15 | 红外光谱 烷烃系统命名法 分子的手性 有机化学 | 有机推断题 |

 +OH-→Br-+SO
+OH-→Br-+SO +H2O中,转移的电子数可能是
+H2O中,转移的电子数可能是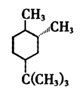 最稳定的构象
最稳定的构象

