2020高三下·辽宁·学业考试
1 . 宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料,其主要成分为CuCO3•Cu(OH)2,下列说法中错误的是
| A.孔雀石颜料中含有重金属离子,使用时勿入口中 |
| B.孔雀石颜料耐酸和碱腐蚀 |
| C.孔雀石颜料不易被空气氧化 |
| D.保存《千里江山图》需控制温度和湿度 |
您最近一年使用:0次
2022-07-10更新
|
650次组卷
|
6卷引用:2022年江苏卷高考真题变式题1-13
(已下线)2022年江苏卷高考真题变式题1-132020年辽宁省普通高中合格性考试(7月份 ) 化学试题(已下线)易错点02 化学与STSE-备战2023年高考化学考试易错题(已下线)专题十 金属材料(已下线)合格考真题汇编8金属元素及其化合物二宁夏六盘山高级中学2022-2023学年高一下学期学业水平合格性考试化学模拟试题
2 . 实验室以合成氨(低温变换的)废催化剂(主要含Zn、Cu的单质和氧化物)为原料制取ZnCO3·2Zn(OH)2和Cu2O,其实验流程如图:
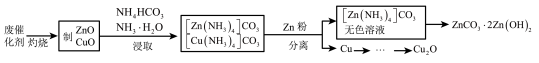
(1)“灼烧”时,需用的硅酸盐质仪器除玻璃棒、酒精灯外,还有___ 和___ 。
(2)“浸取”时,生成[Zn(NH3)4]CO3的离子方程式为___ 。
(3)加“Zn粉”时,为使Zn粉不过量太多{已知:溶液中[Cu(NH3)4]2+呈深蓝色},合适的操作方法及依据的现象是___ ;分离出的铜粉中混有少量Zn,提纯铜粉的方案是__ 。
(4)已知反应:[Zn(NH3)4]2+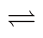 Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是
Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是___ (填字母)。
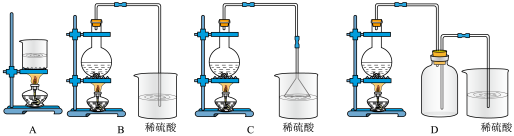
(5)设计以提纯后的铜粉为原料制取Cu2O的实验方案:向烧杯中加入计量的铜粉,__ ,静置、冷却、过滤、水洗及干燥[已知在约50℃时,发生反应:Cu+H2O2+H2SO4=CuSO4+2H2O。实验中必须使用的试剂:稀硫酸、葡萄糖溶液、10%的NaOH溶液和15%的H2O2溶液]。

(1)“灼烧”时,需用的硅酸盐质仪器除玻璃棒、酒精灯外,还有
(2)“浸取”时,生成[Zn(NH3)4]CO3的离子方程式为
(3)加“Zn粉”时,为使Zn粉不过量太多{已知:溶液中[Cu(NH3)4]2+呈深蓝色},合适的操作方法及依据的现象是
(4)已知反应:[Zn(NH3)4]2+
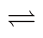 Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是
Zn2++4NH3,K=3.5×10-10,由[Zn(NH3)4]CO3溶液制取ZnCO3·2Zn(OH)2,可采用的装置是
(5)设计以提纯后的铜粉为原料制取Cu2O的实验方案:向烧杯中加入计量的铜粉,
您最近一年使用:0次
名校
解题方法
3 . 已知酸性条件下有如下反应:2Cu+=Cu2++Cu。由于反应温度不同,用氢气还原氧化铜时,可能产生Cu或Cu2O,两者都是红色固体。某同学对氢气还原氧化铜实验所得的红色固体产物进行验证,每一次实验操作和实验现象记录如下,由此推出氢气还原氧化铜实验的产物是( ).
| 加入试剂 | 稀硫酸 | 浓硫酸 | 稀硝酸 | 浓硝酸 |
| 实验现象 | 产生红色固体,溶液呈蓝色 | 加热,产生无色气体 | 产生无色气体,溶液呈蓝色 | 产生红棕色气体,溶液呈绿色 |
| A.只有Cu |
| B.只有Cu2O |
| C.一定有Cu,可能有Cu2O |
| D.一定有Cu2O,可能有Cu |
您最近一年使用:0次
2020-03-06更新
|
281次组卷
|
8卷引用:江苏省启东中学2020年人教版高中化学必修1期末复习第二章 化学物质及其变化(三)
江苏省启东中学2020年人教版高中化学必修1期末复习第二章 化学物质及其变化(三)(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)(已下线)2019年1月17日 《每日一题》高考二轮复习-铜及其化合物2017届新疆生产建设兵团二中高三上第一次月考化学试卷2018届高三一轮复习化学:考点21-铜及其化合物性质探究福建省厦门双十中学2016-2017学年高一下学期第一次月考化学试题(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练
4 . CuSO4是一种重要的化工原料,其有关制备途径及性质如下图所示。下列说法正确的是


| A.相对于途径②,途径①更好地体现了绿色化学思想 |
| B.Y可以是葡萄糖溶液 |
| C.X可能是SO2和SO3的混合气体 |
| D.将CuSO4溶液蒸发,利用余热蒸干,可制得胆矾晶体 |
您最近一年使用:0次
2017-08-19更新
|
570次组卷
|
6卷引用:2018版化学(苏教版)高考总复习课时跟踪训练:铁、铜的获取及应用
2018版化学(苏教版)高考总复习课时跟踪训练:铁、铜的获取及应用(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)2017届湖北省沙市中学高三上学期第二次考试化学试卷广东省揭阳市第三中学2020届高三上学期第三次月考理综化学试题(已下线)课时18 铜及其化合物 合金-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题04 金属材料及金属矿物的开发利用一题多问
名校
5 . 下列说法中正确的是
| A.Cu→CuO→Cu(OH)2每步转化均能通过一步反应实现 |
| B.铝合金是一种混合物,它比纯铝的熔点高 |
| C.金属铜放置在潮湿的空气中会被腐蚀,生成绿色的铜锈——碱式碳酸铜 |
| D.金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜,阻止反应的进一步进行 |
您最近一年使用:0次
2017-08-19更新
|
574次组卷
|
5卷引用:2018版化学(苏教版)高考总复习课时跟踪训练:铁、铜的获取及应用
2018版化学(苏教版)高考总复习课时跟踪训练:铁、铜的获取及应用(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第4讲 用途广泛的金属材料及开发利用金属矿物【押题专练】(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第4讲 金属材料与矿物 铜及其化合物 (题型专练)【校级联考】辽宁省重点六校协作体2019届高三上学期期中考试化学试题【全国百强校】山西省实验中学2018-2019学年高一上学期12月月考化学试题
2010高三·江苏南通·专题练习
6 . 孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4·5H2O及纳米材料G,步骤如下:
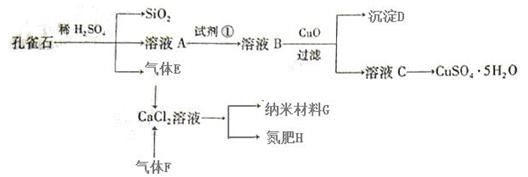
已知:
请回答下列问题:
(1)溶液A中含有Cu2+、Fe2+、Fe3+。根据上述实验过程,可作为试剂①的最合理的是 ▲ (填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)向溶液B中加入CuO的作用是 ▲ 。
(3)由溶液C获得CuSO4·5H2O,需要经过 ▲ 操作。
(4)制备纳米材料G时,应向CaCl2溶液中先通入 ▲ (填化学式)。写出该反应的化学方程式 ▲ 。
(5)欲测定溶液A中Fe2+的浓度,可取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,滴定时盛放待测液A的玻璃仪器是 ▲ (填名称);滴定达到终点的现象为 ▲ 。

已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.7 | 6.7 |
请回答下列问题:
(1)溶液A中含有Cu2+、Fe2+、Fe3+。根据上述实验过程,可作为试剂①的最合理的是 ▲ (填代号)。
a.KMnO4 b.(NH4)2S c.H2O2 d.KSCN
(2)向溶液B中加入CuO的作用是 ▲ 。
(3)由溶液C获得CuSO4·5H2O,需要经过 ▲ 操作。
(4)制备纳米材料G时,应向CaCl2溶液中先通入 ▲ (填化学式)。写出该反应的化学方程式 ▲ 。
(5)欲测定溶液A中Fe2+的浓度,可取A溶液稀释一定倍数后,用KMnO4标准溶液滴定,滴定时盛放待测液A的玻璃仪器是 ▲ (填名称);滴定达到终点的现象为 ▲ 。
您最近一年使用:0次
名校
7 . 铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是______________ ;Y与过量浓硝酸反应后溶液中含有的盐的化学式为___________ 。
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___ 。
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
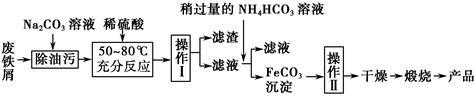
回答下列问题:
①操作Ⅰ的名称是________ ;操作Ⅱ的名称是________ ;操作Ⅱ的方法为_____________________ 。
②请写出生成FeCO3沉淀的离子方程式:____________________________ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后溶液中大量存在的阳离子是
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧,并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是
A.Mg2+B.Fe2+C.Al3+D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:

回答下列问题:
①操作Ⅰ的名称是
②请写出生成FeCO3沉淀的离子方程式:
您最近一年使用:0次
2016-12-08更新
|
535次组卷
|
5卷引用:2018版化学(苏教版)高考总复习课时跟踪训练:铁、铜的获取及应用



