名校
解题方法
1 . 把3.0 mol·L−1 CuSO4溶液和1.0 mol·L−1 Fe2(SO4)3溶液等体积混合(假设混合后液体的体积等于混合前两种溶液的体积之和),向溶液中加入足量铁粉,经足够长的时间后,铁粉有剩余。此时溶液中Fe2+的物质的量浓度为
| A.3.0 mol· L −1 | B.2.5 mol· L −1 | C.2.0mol· L −1 | D.1.0 mol· L −1 |
您最近半年使用:0次
解题方法
2 . 将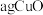 和铜粉的混合物样品加入到体积为1L的
和铜粉的混合物样品加入到体积为1L的 和
和 的混合溶液中,样品完全溶解,反应后溶液中只有
的混合溶液中,样品完全溶解,反应后溶液中只有 、
、 、
、 三种离子,且测得
三种离子,且测得 、
、 的物质的量之比:
的物质的量之比: ,
, (不考虑
(不考虑 、
、 与水反应及溶液体积的变化)。下列说法正确的是
与水反应及溶液体积的变化)。下列说法正确的是
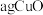 和铜粉的混合物样品加入到体积为1L的
和铜粉的混合物样品加入到体积为1L的 和
和 的混合溶液中,样品完全溶解,反应后溶液中只有
的混合溶液中,样品完全溶解,反应后溶液中只有 、
、 、
、 三种离子,且测得
三种离子,且测得 、
、 的物质的量之比:
的物质的量之比: ,
, (不考虑
(不考虑 、
、 与水反应及溶液体积的变化)。下列说法正确的是
与水反应及溶液体积的变化)。下列说法正确的是A.原溶液中 |
| B.上述反应过程中转移电子的物质的量为0.4mol |
C.混合物中 与Cu的质量之比: 与Cu的质量之比: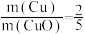 |
D.将足量的 通入灼热a g的混合物中,反应结束后,混合物的质量减少了3.2g 通入灼热a g的混合物中,反应结束后,混合物的质量减少了3.2g |
您最近半年使用:0次
名校
解题方法
3 . 在硫酸铁溶液中同时加入铁粉和铜粉,充分反应后不会出现的结果是
| A.铁铜均有 | B.铁铜均无 | C.有铜无铁 | D.有铁无铜 |
您最近半年使用:0次
2024-02-04更新
|
118次组卷
|
10卷引用:山东省泰安市新泰市第一中学北校2020-2021学年高一上学期第二次考试化学试题
山东省泰安市新泰市第一中学北校2020-2021学年高一上学期第二次考试化学试题浙江省金华市金华十校2020-2021学年高一上学期调研考试化学试题(已下线)【浙江新东方】双师134河南省郑州市第四十七高级中学2021-2022学年高一上学期第二次月考化学试题福建省连城县第一中学2021-2022学年高一上学期第二次月考化学试题2019版鲁科化学必修第一册第3章第1节 铁的多样性课后习题山东省枣庄市2022-2023学年高一上学期期末考试化学试题山东省枣庄市薛城区2022-2023学年高一上学期学科素养诊断化学试题河南省实验中学2023-2024学年高一上学期月考 化学试卷山东省济南市2023-2024学年高一上学期1月期末考试化学试题
名校
4 . 电子工业中,人们常用FeCl3溶液腐蚀附在绝缘板上的铜箔,制造印刷电路板。
(1)请用化学方程式表示制造印刷电路板的反应原理_________________ 。
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:
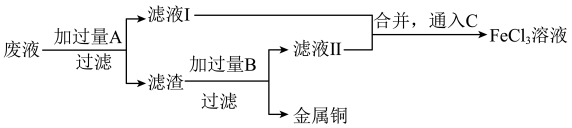
(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A________ ,B________ ,C________ 。
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是_________________ 。为检验该金属阳离子,可设计的实验操作及实验现象为_________________ (可选择的试剂为“锌片”、KSCN溶液、“酸性H2O2”、“酸性KMnO4溶液”或“NaOH溶液”),且该过程发生的氧化还原反应离子方程式为_______________ 。
(4)上述步骤中,通入C发生反应的离子方程式为___________________ 。
(1)请用化学方程式表示制造印刷电路板的反应原理
为了从腐蚀废液中回收铜并重新获得FeCl3溶液,可采用以下步骤:

(2)写出回收铜并重新获得FeCl3溶液的过程中加入的有关物质的化学式:
A
(3)滤液Ⅰ中的阳离子既有氧化性又有还原性,判断的依据是
(4)上述步骤中,通入C发生反应的离子方程式为
您最近半年使用:0次
2024-01-09更新
|
63次组卷
|
2卷引用:广东省珠海市广东实验中学金湾学校2023-2024学年高一上学期12月月考化学试题
名校
5 . 部分被氧化的 合金样品(氧化产物为
合金样品(氧化产物为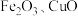 )共5.76g,经如下处理:
)共5.76g,经如下处理:

下列说法不正确的是
 合金样品(氧化产物为
合金样品(氧化产物为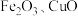 )共5.76g,经如下处理:
)共5.76g,经如下处理:
下列说法不正确的是
A.滤液A中的阳离子为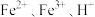 |
| B.样品中氧原子的物质的量为0.02mol |
| C.溶解样品的过程中消耗硫酸的总物质的量为0.04mol |
D.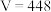 |
您最近半年使用:0次
2023-04-22更新
|
404次组卷
|
2卷引用:浙江省嘉兴市2022-2023学年高一上学期2月期末化学试题
解题方法
6 . 根据下列框图回答问题(答题时,方程式中的M、E用所对应的元素符号表示):
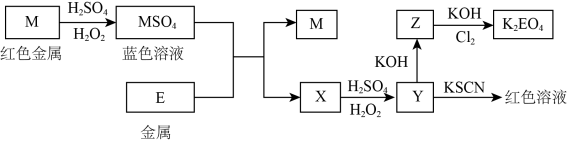
(1)写出下列物质的化学式:M__________ ,E__________ 。
(2)写出M溶于稀 和
和 混合液的化学方程式:
混合液的化学方程式:_____________________________ 。
(3)写出Y和 溶液反应的离子方程式:
溶液反应的离子方程式:________________ 。
(4)写出 将Z氧化为
将Z氧化为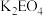 的离子方程式:
的离子方程式:____________________ 。

(1)写出下列物质的化学式:M
(2)写出M溶于稀
 和
和 混合液的化学方程式:
混合液的化学方程式:(3)写出Y和
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)写出
 将Z氧化为
将Z氧化为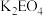 的离子方程式:
的离子方程式:
您最近半年使用:0次
名校
解题方法
7 . 某学生探究小组将 FeCl 溶液腐蚀铜箔制作电路板后的酸性废液“再生”,同时回收铜,实验流程如下:
溶液腐蚀铜箔制作电路板后的酸性废液“再生”,同时回收铜,实验流程如下:
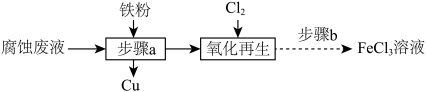
“步骤a”中包含的操作有
 溶液腐蚀铜箔制作电路板后的酸性废液“再生”,同时回收铜,实验流程如下:
溶液腐蚀铜箔制作电路板后的酸性废液“再生”,同时回收铜,实验流程如下:
“步骤a”中包含的操作有
| A.搅拌 | B.过滤 | C.蒸馏 | D.结晶 |
您最近半年使用:0次
2023-04-19更新
|
206次组卷
|
3卷引用:广东省开平市忠源纪念中学2022-2023学年高一下学期4月期中考试(合格考)化学试题
名校
8 . 某兴趣小组用油性笔在一小块覆铜板上写上“化学”,然后浸入盛有 溶液的小烧杯中。一段时间后取出覆铜板,用水洗净并晾干,制作流程如下。该小组继续对反应后的溶液进行定量分析,测得溶液中
溶液的小烧杯中。一段时间后取出覆铜板,用水洗净并晾干,制作流程如下。该小组继续对反应后的溶液进行定量分析,测得溶液中 与
与 之比为
之比为 。下列说法错误的是
。下列说法错误的是

 溶液的小烧杯中。一段时间后取出覆铜板,用水洗净并晾干,制作流程如下。该小组继续对反应后的溶液进行定量分析,测得溶液中
溶液的小烧杯中。一段时间后取出覆铜板,用水洗净并晾干,制作流程如下。该小组继续对反应后的溶液进行定量分析,测得溶液中 与
与 之比为
之比为 。下列说法错误的是
。下列说法错误的是
A.小烧杯中发生反应的离子方程式为: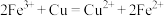 |
B.反应后的溶液再生为 溶液的步骤:加入足量铁粉,过滤,向滤液中通入氯气 溶液的步骤:加入足量铁粉,过滤,向滤液中通入氯气 |
C.反应后的溶液中: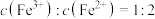 |
D.反应后的溶液中: |
您最近半年使用:0次
2023-02-11更新
|
145次组卷
|
2卷引用:山东省滨州市2022-2023学年高一上学期期末统考化学试题
解题方法
9 . 离子方程式更能体现反应的本质。下列反应的离子方程式书写正确的是
A. 溶液腐蚀铜箔: 溶液腐蚀铜箔: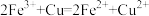 |
B.碳酸钙与稀盐酸反应: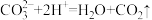 |
C.铜和稀硝酸反应: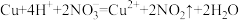 |
D.将金属钠加入到 溶液中: 溶液中: |
您最近半年使用:0次
名校
解题方法
10 . 从古至今,铁及其化合物在人类的生产生活中都起到了巨大的作用。
(1)①在现代半导体工业生产中,常利用 腐蚀铜的原理制作印刷线路板,该原理的化学方程式为:
腐蚀铜的原理制作印刷线路板,该原理的化学方程式为:_______ 。
②氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是_______
A.有铁无铜 B.有铜无铁 C.有铁有铜 D.无铁无铜
(2)某同学在 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入1滴
煤油,再于液面下依次加入1滴 溶液和几滴氯水,溶液变红,煤油的作用是
溶液和几滴氯水,溶液变红,煤油的作用是_______ 。
(3)某同学取 溶液,加入
溶液,加入 溶液混合。分别取此溶液于3支试管中进行如下实验:
溶液混合。分别取此溶液于3支试管中进行如下实验:
①第一支试管中加入1滴淀粉溶液,溶液显蓝色;
②第二支试管中加入1滴 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;
③第三支试管中加入1滴溶液,溶液变红。
i.实验②检验的离子可能是_______ (填离子符号);
ii.写出 与
与 反应的离子方程式
反应的离子方程式_______ 。
iii.上述 和
和 溶充分反应后,溶液中
溶充分反应后,溶液中 浓度为
浓度为_______ 。
(4)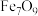 中铁元素形式为
中铁元素形式为 和
和 ,则
,则 和
和 离子质量之比为:
离子质量之比为:_______ 。
(1)①在现代半导体工业生产中,常利用
 腐蚀铜的原理制作印刷线路板,该原理的化学方程式为:
腐蚀铜的原理制作印刷线路板,该原理的化学方程式为:②氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是
A.有铁无铜 B.有铜无铁 C.有铁有铜 D.无铁无铜
(2)某同学在
 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入1滴
煤油,再于液面下依次加入1滴 溶液和几滴氯水,溶液变红,煤油的作用是
溶液和几滴氯水,溶液变红,煤油的作用是(3)某同学取
 溶液,加入
溶液,加入 溶液混合。分别取此溶液于3支试管中进行如下实验:
溶液混合。分别取此溶液于3支试管中进行如下实验:①第一支试管中加入1滴淀粉溶液,溶液显蓝色;
②第二支试管中加入1滴
 溶液,生成蓝色沉淀;
溶液,生成蓝色沉淀;③第三支试管中加入1滴溶液,溶液变红。
i.实验②检验的离子可能是
ii.写出
 与
与 反应的离子方程式
反应的离子方程式iii.上述
 和
和 溶充分反应后,溶液中
溶充分反应后,溶液中 浓度为
浓度为(4)
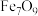 中铁元素形式为
中铁元素形式为 和
和 ,则
,则 和
和 离子质量之比为:
离子质量之比为:
您最近半年使用:0次



