名校
解题方法
1 . 下列关于各图象的解释或结论正确的是


A.由甲可知:热化学方程式是H2(g)+ O2(g)=H2O(g) ΔH=-241.8kJ/mol O2(g)=H2O(g) ΔH=-241.8kJ/mol |
B.由乙可知:对于恒温恒容条件下的反应2NO2(g) N2O4(g),A点为平衡状态 N2O4(g),A点为平衡状态 |
| C.由丙可知:相同pH的盐酸和醋酸溶液分别加水稀释,b点溶液的导电性比c点溶液的导电性强 |
| D.由丁可知:同温度、同物质的量浓度的HA溶液与HB溶液相比,其pH前者小于后者 |
您最近一年使用:0次
2020-01-17更新
|
633次组卷
|
2卷引用:海南省海南中学2019-2020学年高二上学期期末考试化学试题
名校
解题方法
2 . I.甲醛在木材加工、医药等方面有重要用途。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程涉及的主要反应如下:
反应I:CH3OH(g) HCHO(g)+H2(g) △H1=+85.2kJ/mol
HCHO(g)+H2(g) △H1=+85.2kJ/mol
反应II:CH3OH(g)+ O2(g)⇌HCHO(g)+H2O(g) △H2
O2(g)⇌HCHO(g)+H2O(g) △H2
反应III:2H2(g)+O2(g)⇌2H2O(g) △H3=-483.6kJ/mol
(1)计算反应Ⅱ的反应热△H2=_____________________________ 。
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g)⇌HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________ (用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________ kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
II.CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(3)CO2用于生产乙烯,已知:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g) △H=QkJ/mol。一定条件下,按不同的投料比X[X= ]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
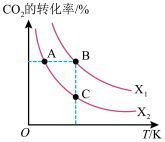
①X1_____ X2(填“>”或“<”,后同),Q_____ 0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为_____ 。
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=_____ [常温下K1(H2CO3)=4.4×10﹣7、K2(H2CO3)=5×10﹣11]。
②欲用5L Na2CO3溶液将23.3g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为__________ 。[已知:常温下Ksp(BaSO4)=1×10﹣7、Ksp(BaCO3)=2.5×10﹣6]。(忽略溶液体积积的变化)
反应I:CH3OH(g)
 HCHO(g)+H2(g) △H1=+85.2kJ/mol
HCHO(g)+H2(g) △H1=+85.2kJ/mol反应II:CH3OH(g)+
 O2(g)⇌HCHO(g)+H2O(g) △H2
O2(g)⇌HCHO(g)+H2O(g) △H2反应III:2H2(g)+O2(g)⇌2H2O(g) △H3=-483.6kJ/mol
(1)计算反应Ⅱ的反应热△H2=
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g)⇌HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=
II.CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(3)CO2用于生产乙烯,已知:2CO2(g)+6H2(g)⇌CH2=CH2(g)+4H2O(g) △H=QkJ/mol。一定条件下,按不同的投料比X[X=
 ]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
]向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
①X1
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为
(4)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
①若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=
②欲用5L Na2CO3溶液将23.3g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为
您最近一年使用:0次
2019-03-14更新
|
741次组卷
|
5卷引用:海南省琼海市嘉积第三中学2021-2022学年高三下学期第三次月考化学科试题
海南省琼海市嘉积第三中学2021-2022学年高三下学期第三次月考化学科试题 【校级联考】江西省重点中学盟校2019届高三上学期第一次联考化学试题(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(三)山东省济南市大学城实验高级中学2021届高三1月阶段性考试化学试题云南民族大学附属中学2019-2020学年高二下学期期中考试化学试题
名校
解题方法
3 . 碳及其化合物与人类的生活、生产紧密联系。
(1)已知2g甲烷完全燃烧生成稳定的氧化物时放出Q kJ的热量,写出表示甲烷燃烧热的热化学方程式:___________
(2)已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+130 kJ·mol-1,2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1。断开1 mol H—H键、O===O键分别需要吸收436 kJ、496 kJ的热量,则断开1 mol O—H键需要吸收的热量为___________
A.332 kJ B.462 kJ C.118 kJ D.360 kJ
(3)以CO2和H2O为原料制备HCOOH和O2的原电池原理如图.

电极a为_____ (填“正”或“负”)极,电极b发生的电极反应式是:___________________ .
(1)已知2g甲烷完全燃烧生成稳定的氧化物时放出Q kJ的热量,写出表示甲烷燃烧热的热化学方程式:
(2)已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+130 kJ·mol-1,2C(s)+O2(g)=2CO(g) ΔH=-220 kJ·mol-1。断开1 mol H—H键、O===O键分别需要吸收436 kJ、496 kJ的热量,则断开1 mol O—H键需要吸收的热量为
A.332 kJ B.462 kJ C.118 kJ D.360 kJ
(3)以CO2和H2O为原料制备HCOOH和O2的原电池原理如图.

电极a为
您最近一年使用:0次



