1 . 水煤合成气的生产和应用在化学工业中有极为重要的地位。回答下列问题:
(1)利用合成气(主要成分CO、CO2和H2)在催化剂作用下合成甲醇,可能发生的反应有:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-63 kJ•mol-1
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2
③CH3OH(g)=CO(g)+2H2(g) ΔH3
已知部分化学键键能数据如下表:
则ΔH3=_______ kJ•mol-1。
(2)CO2和CH4在一定条件下反应也可制得合成水煤气。在1.0 L密闭容器中充入1.0 mol CH4和1.0 mol CO2,在一定条件下发生反应CH4(g)+CO2(g) 2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
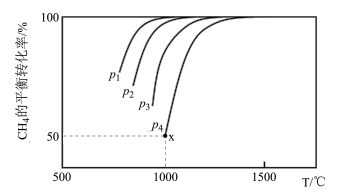
①比较压强大小:p1_______ p3(选填“>”、“<”或“=”)。
②若要提高CH4的平衡转化率,可采取的措施有_______ ,_______ 。(任写两条)
③若p4=2.0 MPa,则x点的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)化学家利用电化学原理回收CO2达到节能减排的目的,有一种实验设计的装置如下图所示。
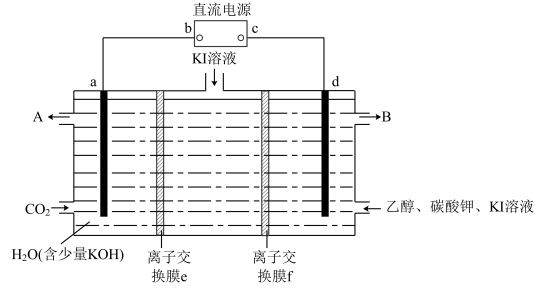
已知在碱性条件下,卤素单质可以将乙醇氧化为乙醛。实验一段时间后,测得a电极周围有甲酸根离子HCOO-生成。回答:
①电极b为_______ 极;
②电解时a电极附近溶液的pH_______ (选填“降低”、“升高”、“不变”);
③e为_______ 交换膜;
④d电极周围除了发生电极反应外,还有_______ (用离子方程式表示)。
(1)利用合成气(主要成分CO、CO2和H2)在催化剂作用下合成甲醇,可能发生的反应有:
①CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH1=-63 kJ•mol-1
②CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2
③CH3OH(g)=CO(g)+2H2(g) ΔH3
已知部分化学键键能数据如下表:
| 化学键 | H-H | C=O | C≡O | O-H |
| 键能(kJ•mol-1) | 436 | 803 | 1076 | 465 |
(2)CO2和CH4在一定条件下反应也可制得合成水煤气。在1.0 L密闭容器中充入1.0 mol CH4和1.0 mol CO2,在一定条件下发生反应CH4(g)+CO2(g)
 2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
2CO(g)+2H2,测得CH4的平衡转化率与温度及压强的关系如下图所示。
①比较压强大小:p1
②若要提高CH4的平衡转化率,可采取的措施有
③若p4=2.0 MPa,则x点的平衡常数Kp=
(3)化学家利用电化学原理回收CO2达到节能减排的目的,有一种实验设计的装置如下图所示。

已知在碱性条件下,卤素单质可以将乙醇氧化为乙醛。实验一段时间后,测得a电极周围有甲酸根离子HCOO-生成。回答:
①电极b为
②电解时a电极附近溶液的pH
③e为
④d电极周围除了发生电极反应外,还有
您最近一年使用:0次
2022-11-05更新
|
141次组卷
|
2卷引用:海南省海口中学2023-2024学年高二上学期12月月考化学试题
2 . “水煤气(CO和 )”是化学工业常用的原料气,请回答:
)”是化学工业常用的原料气,请回答:
I.已知:焦炭、CO的标准燃烧热分别为 、
、 ,氢气燃烧的热化学反应方程式:
,氢气燃烧的热化学反应方程式: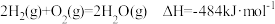
(1)试写出由焦炭和水蒸气生成水煤气的热化学反应方程式:___________
(2)下列说法正确的是___________
II.合成氨工厂以“水煤气”为原料,采用两段间接换热式绝热反应器(反应器中的催化剂对原料气的吸附时间长短,对原料气的转化率会造成一定影响)在常压下进行转换合成氨,装置如图。
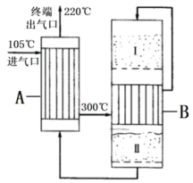
A反应器中主要发生的反应为: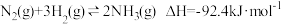
B反应器中主要发生的反应为:
主反应: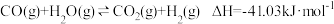
副反应:
由进气口充入一定量含CO、 、
、 、
、 的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、
的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、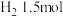 、
、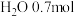 、
、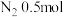 、
、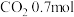 和
和 。
。
已知标准平衡常数: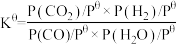 ,其中
,其中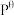 表示标准压强(
表示标准压强( )
)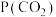 、
、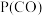 、
、 、
、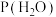 表示各组分的分压,如
表示各组分的分压,如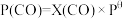 ,
, 为体系中CO的物质的量分数
为体系中CO的物质的量分数
(3)T℃时,主反应的压强平衡常数
___________
(4)平衡时CO的转化率为___________
(5)进气空速对反应产品的收率有一定的影响,实验测得在不同进气空速下,测得平衡时 的收率如下图所示
的收率如下图所示
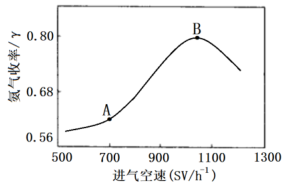
①曲线中A点到B点变化的原因是:___________
②若将绝热转换反应器改为恒温转换反应器,试在图中画出随进气空速变化的 收率曲线
收率曲线___ 。
 )”是化学工业常用的原料气,请回答:
)”是化学工业常用的原料气,请回答:I.已知:焦炭、CO的标准燃烧热分别为
 、
、 ,氢气燃烧的热化学反应方程式:
,氢气燃烧的热化学反应方程式: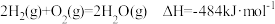
(1)试写出由焦炭和水蒸气生成水煤气的热化学反应方程式:
(2)下列说法正确的是___________
| A.将煤炭在空气中直接加强热进行干馏,制备生成水煤气的原料焦炭 |
| B.水煤气可经过催化合成获得液体燃料、碳氢化合物和含氧有机物 |
| C.水煤气也可采用高温下煤和水蒸气直接作用制得 |
| D.在恒压反应釜中,利用焦炭与水蒸气高温制备水煤气时,适当加快通入水蒸气的流速,有利于水煤气的生成 |
II.合成氨工厂以“水煤气”为原料,采用两段间接换热式绝热反应器(反应器中的催化剂对原料气的吸附时间长短,对原料气的转化率会造成一定影响)在常压下进行转换合成氨,装置如图。

A反应器中主要发生的反应为:
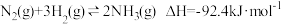
B反应器中主要发生的反应为:
主反应:
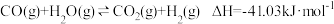
副反应:

由进气口充入一定量含CO、
 、
、 、
、 的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、
的混合气体,在B中充分反应,在T℃下,反应达到平衡后,测得混合气体各组分的物质的量分别为CO0.2mol、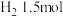 、
、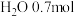 、
、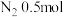 、
、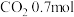 和
和 。
。已知标准平衡常数:
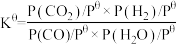 ,其中
,其中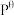 表示标准压强(
表示标准压强( )
)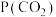 、
、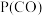 、
、 、
、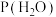 表示各组分的分压,如
表示各组分的分压,如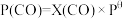 ,
, 为体系中CO的物质的量分数
为体系中CO的物质的量分数(3)T℃时,主反应的压强平衡常数

(4)平衡时CO的转化率为
(5)进气空速对反应产品的收率有一定的影响,实验测得在不同进气空速下,测得平衡时
 的收率如下图所示
的收率如下图所示
①曲线中A点到B点变化的原因是:
②若将绝热转换反应器改为恒温转换反应器,试在图中画出随进气空速变化的
 收率曲线
收率曲线
您最近一年使用:0次
2021-10-20更新
|
637次组卷
|
3卷引用:2021年海南高考化学试题变式题11-19
名校
解题方法
3 . Ⅰ.铁及铁的氧化物广泛应于生产、生活、航天、科研领域。
(1)铁的氧化物循环分解水制H2
已知:H2O(l)=H2(g)+1/2 O2(g) ΔH1=a kJ•mol-1
6FeO(s)+O2(g)=2Fe3O4(s) ΔH2=b kJ•mol-1
则:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH3=_______
(2)Fe2O3与CH4反应可制备“纳米级”金属铁。已知,恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+Fe2O3(s)⇌2Fe(s)+6H2(g)+3CO(g)
①此反应的化学平衡常数表达式为_______
②下列条件能判断该反应达到平衡状态的是_______
a.消耗1molFe2O3的同时,消耗3molCO
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2)
Ⅱ.用CH4还原NO2的反应为CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),向两个容积均为2L温度分别为T1、T2的恒温恒容密闭容器中分别加入1mol CH4和2mol NO2,测得各容器中n(NO2)随反应时间t的变化如图所示:
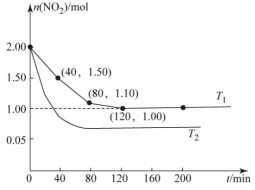
①T1_______ T2(填“>”或“<”)。
②T1时,40~80 min内,用N2的浓度变化表示的平均反应速率为v(N2)=_______
③T1下,200 min时,向容器中再加入CH4、NO2和H2O(g)各l mol,化学平衡_______ 移动(填“正向”“逆向”或“不”)。
Ⅲ.CaSO4微溶于水和酸,可加入氢氧化钠并通入CO2使其转化为CaCO3,然后加酸浸泡除去,反应的离子方程式为CaSO4+CO =CaCO3+SO
=CaCO3+SO ,室温下,该反应的化学平衡常数为
,室温下,该反应的化学平衡常数为_______ (室温下,Ksp(CaCO3)=3×10-9,Ksp(CaSO4)=9×10-6)。
(1)铁的氧化物循环分解水制H2
已知:H2O(l)=H2(g)+1/2 O2(g) ΔH1=a kJ•mol-1
6FeO(s)+O2(g)=2Fe3O4(s) ΔH2=b kJ•mol-1
则:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH3=
(2)Fe2O3与CH4反应可制备“纳米级”金属铁。已知,恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+Fe2O3(s)⇌2Fe(s)+6H2(g)+3CO(g)
①此反应的化学平衡常数表达式为
②下列条件能判断该反应达到平衡状态的是
a.消耗1molFe2O3的同时,消耗3molCO
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2)
Ⅱ.用CH4还原NO2的反应为CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),向两个容积均为2L温度分别为T1、T2的恒温恒容密闭容器中分别加入1mol CH4和2mol NO2,测得各容器中n(NO2)随反应时间t的变化如图所示:

①T1
②T1时,40~80 min内,用N2的浓度变化表示的平均反应速率为v(N2)=
③T1下,200 min时,向容器中再加入CH4、NO2和H2O(g)各l mol,化学平衡
Ⅲ.CaSO4微溶于水和酸,可加入氢氧化钠并通入CO2使其转化为CaCO3,然后加酸浸泡除去,反应的离子方程式为CaSO4+CO
 =CaCO3+SO
=CaCO3+SO ,室温下,该反应的化学平衡常数为
,室温下,该反应的化学平衡常数为
您最近一年使用:0次
2021-06-27更新
|
1003次组卷
|
8卷引用:2021年海南高考化学试题变式题11-19
2021年海南高考化学试题变式题11-19四川省广安市2019-2020学年高二下学期期末(零诊)化学试题(已下线)理综化学-2021年秋季高三开学摸底考试卷01(课标全国专用)(已下线)备战2022年高考化学精准检测卷【全国卷】08广东省湛江市第二十一中学2021—2022学年高三上学期11月月考化学试题四川省资中县球溪高级中学2022-2023学年高三上学期10月月考化学试题湖北省天门外国语学校2022-2023学年高二上学期12月月考化学试题四川省内江市威远中学校2022-2023学年高二下学期第二次阶段性考试理综化学试题
名校
4 . 下列图示与对应的叙述相符合的是
A. 表示对某化学平衡体系改变温度后反应速率随时间的变化 表示对某化学平衡体系改变温度后反应速率随时间的变化 |
B. 表示反应物断键吸收的总能量大于生成物成键放出的总能量 表示反应物断键吸收的总能量大于生成物成键放出的总能量 |
C.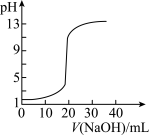 表示0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化 表示0.1 mol·L-1 NaOH溶液滴定20 mL 0.1 mol·L-1硫酸时溶液pH的变化 |
D. 表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况 表示向Ba(OH)2溶液中滴加稀H2SO4至过量,溶液的导电性变化情况 |
您最近一年使用:0次
2018-02-07更新
|
693次组卷
|
7卷引用:【全国百强校】海南省海南中学2018届高三下学期第二次模拟考试化学试题
名校
解题方法
5 . 臭氧是一种强氧化剂,常用于消毒、灭菌等。
(1)O3与KI溶液反应生成的两种单质是____ 和____ (填分子式)。
(2)已知①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=+571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=+131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=+206.1kJ·mol–1
则反应CH4(g)=C(s)+2H2(g)的ΔH=_______________ kJ·mol–1
(3)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。已知:O3的起始浓度为 0.021 6 mol/L。
①pH增大能加速O3分解,表明对O3分解起催化作用的微粒是____ 。
②在30 ℃、pH=4.0条件下,O3的分解速率为_____ mol/(L·min)。
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为_____ (填字母)。
a.40 ℃、pH=3.0 b.10 ℃、pH=4.0 c.30 ℃、pH=7.0
(4)O3可由臭氧发生器(原理如图)电解稀硫酸制得。

①图中阴极为____ (填“A”或“B”),其电极反应式为_________________________ 。
②若C处通入O2,则A极的电极反应式为_________ ,右室pH变化___________ (填升高、降低、不变)
(1)O3与KI溶液反应生成的两种单质是
(2)已知①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=+571.6kJ·mol–1
②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=+131.3kJ·mol–1
③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=+206.1kJ·mol–1
则反应CH4(g)=C(s)+2H2(g)的ΔH=
(3)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。已知:O3的起始浓度为 0.021 6 mol/L。
| pH t /min T/℃ | 3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
①pH增大能加速O3分解,表明对O3分解起催化作用的微粒是
②在30 ℃、pH=4.0条件下,O3的分解速率为
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为
a.40 ℃、pH=3.0 b.10 ℃、pH=4.0 c.30 ℃、pH=7.0
(4)O3可由臭氧发生器(原理如图)电解稀硫酸制得。

①图中阴极为
②若C处通入O2,则A极的电极反应式为
您最近一年使用:0次
12-13高一上·海南·期末
6 . 硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用。试回答下列问题:
(1) 向大气中排放NOx可能导致的环境问题有_______ 。(答两点)已知足量NaOH溶液能完全吸收NO2生成氮的两种含氧酸盐(氮为+3、+5价)。试写出该反应的离子方程式_______ 。
(2) 光导纤维的作用,让人们的生活更加丰富精彩,_______ 是制备光导纤维的基本原料。
(3) 氮化硅陶瓷是一种新型无机非金属材料,其化学式为_______ , 可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成,氮气在反应中既是反应物,同时又起了_______ 作用。由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉。在烧结过程中,二氧化硅、碳、氮气以物质的量之比3∶6∶2反应生成两 种化合物,该反应的化学方程式为_______ 。
(4) 硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源。与“氢能源”比较“硅能源”具有_______ 等更加优越的特点,从而得到全球的关注和期待。
(1) 向大气中排放NOx可能导致的环境问题有
(2) 光导纤维的作用,让人们的生活更加丰富精彩,
(3) 氮化硅陶瓷是一种新型无机非金属材料,其化学式为
(4) 硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源。与“氢能源”比较“硅能源”具有
您最近一年使用:0次



