解题方法
1 . 下列关于热化学反应的描述中正确的是
A. 和 和 反应的中和热 反应的中和热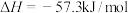 ,则 ,则 和 和 反应的中和热 反应的中和热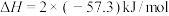 |
B.甲烷的标准燃烧热 ,则 ,则 |
C.已知: 、 、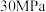 下, 下,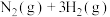 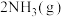 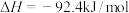 ;将 ;将 和过量的 和过量的 在此条件下充分反应,放出热量 在此条件下充分反应,放出热量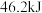 |
D. 的燃烧热是 的燃烧热是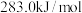 ,则 ,则 反应的 反应的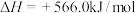 |
您最近一年使用:0次
名校
2 . 化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语错误的是
A.相同条件下,等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应 |
B.在稀溶液中,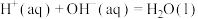  ,若将含0.5mol硫酸的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ ,若将含0.5mol硫酸的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ |
C.热化学方程式为: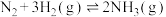  ,一定条件下,将 ,一定条件下,将 和 和 置于密闭的容器中反应生成 置于密闭的容器中反应生成 ,则放热46.2kJ ,则放热46.2kJ |
D.CO(g)的燃烧热是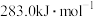 ,则 ,则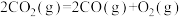  |
您最近一年使用:0次
2024-04-04更新
|
355次组卷
|
2卷引用:四川省内江市2025届第三中学高二上学期化学试卷
名校
3 . 能源是人类生存和发展的重要支柱。研究和有效地开发新能源有重要意义。已知CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的燃烧过程如图所示:

已知:H2O(g)=H2O(l) ΔH=-41kJ·mol-1.请根据以上信息,回答下列有关问题:
(1)图形中E表示CH3CH2CH2CH3(g)燃烧反应逆反应的___________ 。
(2)CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的热稳定性___________ 更高。
(3)表示CH3CH(CH3)CH3(g)燃烧热的热化学方程式为___________ 。
(4)CH3CH2CH2CH3(g)转化为CH3CH(CH3)CH3(g)的热化学反应方程式为___________ 。
(5)如表所示是部分化学键的键能参数:
合成气(CO和H2的混合气体)可以合成CH3CH2CH2CH3(g),同时生成H2O(g),则合成1molCH3CH2CH2CH3(g)的ΔH=___________ 。
(6)标准状况,CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的混合气体11.2L,充分燃烧后,生成H2O(g)和CO2(g),共放出1333.8kJ热量,则混合气体中CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的物质的量之比为___________ 。

已知:H2O(g)=H2O(l) ΔH=-41kJ·mol-1.请根据以上信息,回答下列有关问题:
(1)图形中E表示CH3CH2CH2CH3(g)燃烧反应逆反应的
(2)CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的热稳定性
(3)表示CH3CH(CH3)CH3(g)燃烧热的热化学方程式为
(4)CH3CH2CH2CH3(g)转化为CH3CH(CH3)CH3(g)的热化学反应方程式为
(5)如表所示是部分化学键的键能参数:
| 化学键 | C≡O | C—H | H—H | C—C | H—O |
| 键能/(kJ·mol-1) | a | b | d | e | f |
(6)标准状况,CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的混合气体11.2L,充分燃烧后,生成H2O(g)和CO2(g),共放出1333.8kJ热量,则混合气体中CH3CH2CH2CH3(g)与CH3CH(CH3)CH3(g)的物质的量之比为
您最近一年使用:0次
名校
4 . 依据如下反应可知某纯物质的燃烧热的是(燃烧热数值正确)
A.2C(s)+O2(g)=2CO(g)  =﹣221kJ•mol-1 =﹣221kJ•mol-1 |
B.CH4(g)+2O2(g)=2CO2(g)+2H2O(g)  =﹣890.3kJ•mol-1 =﹣890.3kJ•mol-1 |
C.4NH3(g)+3O2(g)=2N2(g)+6H2O(l)  =﹣1265.2kJ•mol-1 =﹣1265.2kJ•mol-1 |
D.2H2S(g)+O2(g)=2H2O(l)+2S(s)  =-632kJ•mol-1 =-632kJ•mol-1 |
您最近一年使用:0次
5 . 能由下表所列的“依据”推导出后面的“结论”的是
| 依据 | 结论 | |
| A | 稀溶液中: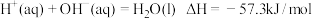 | 中和热为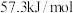 |
| B | C(s,石墨) C(s,金刚石) 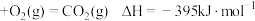 | 石墨转化为金刚石的过程中会放出热量 |
| C |  时, 时, ; ; | 非金属性: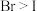 |
| D |  |  的燃烧热为 的燃烧热为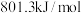 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 大气中的二氧化碳主要来自于煤、石油及其他含碳化合物的燃烧。已知25℃时,相关物质的燃烧热数据如下表:
则25℃时,6C(石墨,s)+3H2(g)=C6H6(l) △H=
| 物质 | H2(g) | C(石墨,s) | C6H6(l) |
| 燃烧热△H(kJ•mol-1) | -285.8 | -393.5 | -3267.5 |
| A.-30.9kJ/mol | B.+49.1kJ/mol | C.+104.7kJ/mol | D.-2588.2kJ/mol |
您最近一年使用:0次
7 . 已知①
 kJ⋅mol-1
kJ⋅mol-1  ;
;
②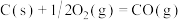
 kJ⋅mol-1
kJ⋅mol-1  ;
;
③
 kJ⋅mol-1
kJ⋅mol-1 
下列说法正确的是

 kJ⋅mol-1
kJ⋅mol-1  ;
;②
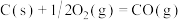
 kJ⋅mol-1
kJ⋅mol-1  ;
;③

 kJ⋅mol-1
kJ⋅mol-1 
下列说法正确的是
A.C的燃烧热 kJ kJ |
B.2g 完全燃烧生成液态水放出的热量为241.8kJ 完全燃烧生成液态水放出的热量为241.8kJ |
C.反应 的反应热为+41.2kJ⋅mol-1 的反应热为+41.2kJ⋅mol-1 |
D.反应 的平衡常数 的平衡常数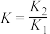 |
您最近一年使用:0次
8 . 已知热化学反应方程式:
①

②

下列说法正确的是
①


②


下列说法正确的是
A.反应①: | B.CO的燃烧热是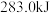 |
C.C生成 需要吸收热量 需要吸收热量 | D.盖斯定律可间接获得不方便测量的反应热 |
您最近一年使用:0次
名校
9 . 下列热化学方程式中,与反应描述对应且书写正确的是
A.已知: 。稀 。稀 溶液与稀硫酸中和: 溶液与稀硫酸中和: |
B.在25℃、101kPa下,1g辛烷燃烧生成二氧化碳和液态水时放出48.4kJ热量: |
C.查表知葡萄糖固体颗粒的燃烧热为2800kJ/mol,则葡萄糖固体燃烧可表示为: |
D.6.4g硫粉与12.8g铜粉混合高温下充分反应,放热19.12kJ: |
您最近一年使用:0次
名校
10 . I.50mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液在图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题:
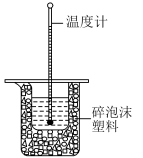
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________ 。
(2)实验中改用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”、“不相等”),所求中和热______ 。(填“相等”、“不相等”)
(3)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是_____ (填序号)。
a.Ba(OH)2·8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(4)已知N2(g)+2O2(g)=2 NO2(g) ΔH =+67.7 kJ·mol-1
N2H4(g)+O2(g)= N2(g)+2H2O (l) ΔH =-534 kJ·mol-1
根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式___________ 。
Ⅱ.CO、SO2、NO均为大气污染物,通过下列反应可以实现可持续发展。已知:
①2CO(g)+SO2(g)=S(g)+2CO2(g) ΔH=+8.0kJ/mol-1
②2H2(g)+SO2(g)=S(g)+2H2O(g) ΔH=+90.4kJ·mol -1
③2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.5kJ·mol -1
请回答:
(5)反应①属于______  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
(6)反应②生成0.5mol S(g)时,ΔH=________ 。
(7)反应③消耗30g NO(g)时,ΔH=________ 。

(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)实验中改用60mL0.50mol·L-1盐酸与50mL0.55mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
(3)化学反应中的能量变化,通常主要表现为热量的变化。下列反应中,属于放热反应的是
a.Ba(OH)2·8H2O与NH4Cl混合搅拌 b.高温煅烧石灰石 c.铝与盐酸反应
(4)已知N2(g)+2O2(g)=2 NO2(g) ΔH =+67.7 kJ·mol-1
N2H4(g)+O2(g)= N2(g)+2H2O (l) ΔH =-534 kJ·mol-1
根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式
Ⅱ.CO、SO2、NO均为大气污染物,通过下列反应可以实现可持续发展。已知:
①2CO(g)+SO2(g)=S(g)+2CO2(g) ΔH=+8.0kJ/mol-1
②2H2(g)+SO2(g)=S(g)+2H2O(g) ΔH=+90.4kJ·mol -1
③2NO(g)+2CO(g)=N2(g)+2CO2(g) ΔH=-746.5kJ·mol -1
请回答:
(5)反应①属于
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。(6)反应②生成0.5mol S(g)时,ΔH=
(7)反应③消耗30g NO(g)时,ΔH=
您最近一年使用:0次
2024-02-02更新
|
107次组卷
|
2卷引用:四川省眉山市仁寿第一中学校(北校区)2023-2024学年高二上学期11月期中化学试题



