1 . 假定反应体系的始态为s,终态为l,它们之间变化如图所示:s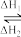 l,则下列说法不正确的是
l,则下列说法不正确的是
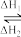 l,则下列说法不正确的是
l,则下列说法不正确的是| A.若ΔH1<0,则ΔH2>0 | B.若ΔH1<0,则ΔH2<0 |
| C.ΔH1和ΔH2的绝对值相等 | D.ΔH1+ΔH2=0 |
您最近一年使用:0次
20-21高二上·浙江金华·期中
2 . H2与ICl的反应分两步完成,其能量曲线如图所示。反应①:H2(g)+2ICl(g)=HCl(g)+HI(g)+ICl(g),反应②:HCl(g)+HI(g)+ICl(g)=I2(g)+2HCl(g),下列有关说法不正确 的是
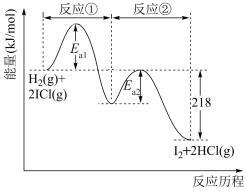

| A.总反应的活化能为(Ea1+Ea2)kJ·mol-1 |
| B.反应①、②均是反应物总能量高于生成物总能量 |
| C.H2(g)+2ICl(g)=I2(g)+2HCl(g) ∆H=-218kJ·mol-1 |
| D.温度升高,活化分子百分数增大,反应碰撞概率增大,反应速率加快 |
您最近一年使用:0次
解题方法
3 . 已知2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,则下列关于方程式2H2O(l)=2H2(g)+O2(g)的ΔH的说法中正确的是
| A.方程式中的化学计量数表示分子数 |
| B.该反应ΔH大于零 |
| C.该反应ΔH=-571.6 kJ·mol-1 |
| D.该反应可表示36 g水分解时的热效应 |
您最近一年使用:0次
2022-07-26更新
|
478次组卷
|
5卷引用:第2课时 化学反应的内能变化与焓变
第2课时 化学反应的内能变化与焓变(已下线)第24练 反应热-2023年高考化学一轮复习小题多维练(全国通用)河北省唐山市迁西县职业技术教育中心2021-2022学年高二(普职融通部)上学期9月月考化学试题(已下线)【知识图鉴】单元讲练测选择性必修1第1单元02基础练(已下线)BBWYhjhx1102
名校
4 . 煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaSO4(s)+4CO(g) CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
下列有关说法正确的是
CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)
CaO(s)+SO2(g)+CO2(g) △H1=+218.4 kJ/mol(反应I)CaSO4(s)+4CO(g)
 CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)
CaS(s)+4CO2(g) △H2=-175.6 kJ/mol (反应II)下列有关说法正确的是
| A.反应I在较低的温度下可自发进行 |
| B.反应II在较低的温度下可自发进行 |
C.用生石灰固硫的反应为:4CaO(s)+4SO2(g)  3CaSO4(s)+CaS(s) △H3,则△H3>△H2 3CaSO4(s)+CaS(s) △H3,则△H3>△H2 |
D.由反应I和反应II可计算出反应CaSO4(s)  CaO(s)+SO3(g)的焓变 CaO(s)+SO3(g)的焓变 |
您最近一年使用:0次
2018-10-24更新
|
617次组卷
|
6卷引用:鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第1节 化学反应的方向



