1 . 利用 制甲醇具有重要意义。其过程可能发生的反应如下:
制甲醇具有重要意义。其过程可能发生的反应如下:
反应1: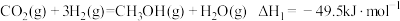
反应2:
反应3: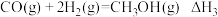
(1)
_______ 
(2)恒容条件下,下列有利于提高 平衡产率的条件是_______。
平衡产率的条件是_______。
(3)控制一定压强,通入 和
和 ,反应
,反应 后,
后, 转化率
转化率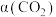 、
、 产率
产率 及
及 产率
产率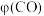 随温度变化曲线如图。
随温度变化曲线如图。
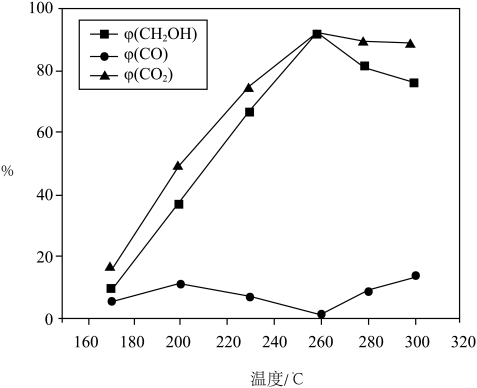
①温度升高, 先升高后降低的原因是
先升高后降低的原因是_______ 。
②260℃时,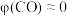 (认为此时只发生反应1),
(认为此时只发生反应1),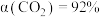 ,气体总体积为
,气体总体积为 ,则该温度下反应1的平衡常数
,则该温度下反应1的平衡常数
_______ (列出代数式即可),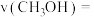
_______ (列出代数式即可)。
③280℃时, ,
, ,则反应2的平衡常数
,则反应2的平衡常数
_______ (列出代数式即可)。
(4)学界关于反应2产生的 能否发生反应3存在争议。科学家利用
能否发生反应3存在争议。科学家利用 模拟
模拟 催化剂表面合成
催化剂表面合成 的两种不同路径,其决速步及活化能
的两种不同路径,其决速步及活化能 分别如下。
分别如下。
路径1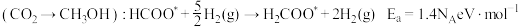
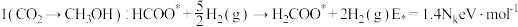 路径2
路径2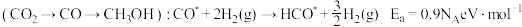
由此分析,200~260℃时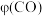 降低的原因是
降低的原因是_______ 。
 制甲醇具有重要意义。其过程可能发生的反应如下:
制甲醇具有重要意义。其过程可能发生的反应如下:反应1:
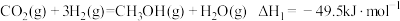
反应2:

反应3:
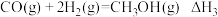
(1)


(2)恒容条件下,下列有利于提高
 平衡产率的条件是_______。
平衡产率的条件是_______。| A.使用催化剂 | B.调整 和 和 的投料比由1∶1至1∶3 的投料比由1∶1至1∶3 |
| C.增大反应物总压 | D.通入稀有气体 |
 和
和 ,反应
,反应 后,
后, 转化率
转化率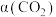 、
、 产率
产率 及
及 产率
产率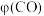 随温度变化曲线如图。
随温度变化曲线如图。
①温度升高,
 先升高后降低的原因是
先升高后降低的原因是②260℃时,
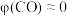 (认为此时只发生反应1),
(认为此时只发生反应1),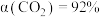 ,气体总体积为
,气体总体积为 ,则该温度下反应1的平衡常数
,则该温度下反应1的平衡常数
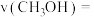
③280℃时,
 ,
, ,则反应2的平衡常数
,则反应2的平衡常数
(4)学界关于反应2产生的
 能否发生反应3存在争议。科学家利用
能否发生反应3存在争议。科学家利用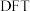 模拟
模拟 催化剂表面合成
催化剂表面合成 的两种不同路径,其决速步及活化能
的两种不同路径,其决速步及活化能 分别如下。
分别如下。路径1
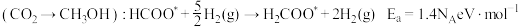
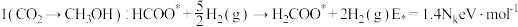 路径2
路径2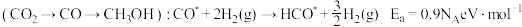
由此分析,200~260℃时
 降低的原因是
降低的原因是
您最近一年使用:0次
2 . 在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g) 2NH3(g) ∆H=-92.4kJ/mol)
2NH3(g) ∆H=-92.4kJ/mol)
下列说法正确的是
 2NH3(g) ∆H=-92.4kJ/mol)
2NH3(g) ∆H=-92.4kJ/mol)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1 mol N2、3 mol H2 | 2 mol NH3 | 4 mol NH3 |
| NH3浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强 | p1 | p2 | p3 |
| 反应物转化率 | a1 | a2 | a3 |
| A.2c1>c3 | B.a+b=92.4 | C.2p1<p3 | D.a2+a3>1 |
您最近一年使用:0次
2021-10-20更新
|
1982次组卷
|
25卷引用:福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题
福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)2011-2012学年江西省上饶县中学高二第一次月考化学试卷2015-2016学年四川省新津中学高二10月月考化学试卷2016-2017学年黑龙江省铁人中学高二上开学测化学卷湖北省沙市中学2017-2018学年高二上学期期中考试化学试题安徽省淮南市第二中学2017-2018学年高二上学期第二次月考化学试题内蒙古北京八中乌兰察布分校2017-2018学年高二下学期第二次调研考试化学试题【全国百强校】宁夏回族自治区银川市第一中学2018-2019学年高二上学期期末考试化学试题新疆乌鲁木齐市二十三中学2018-2019学年高二10月月考化学试题步步为赢 高二化学寒假作业:作业六 化学平衡中的模型构建与等效平衡云南省楚雄市楚雄实验中学2018—2019学年高二上学期9月月考化学试题鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 第4节 化学反应条件的优化—工业合成氨山东省临沂市沂水一中2020-2021学年高二9月月考化学试题江西省赣州市会昌县会昌中学2020-2021学年高二上学期第一次月考化学试题河南省安阳市第一中学2020-2021学年高二上学期第一次阶段考试化学试题山西省运城市景胜中学2020-2021学年高二10月月考化学试题黑吉两省十校2020-2021学年高二上学期期中联考(吉雅2校用)化学试题天津市咸水沽第二中学2021-2022学年高二上学期第一次月考化学试题江西省吉安市峡江中学2021-2022学年高二上学期开学考试化学(理科)试题百所名校联考-选修四模块综合检测夯基提能2020届高三化学选择题对题专练——选修四化学反应原理—— 转化率与产率的相关计算2020届高三化学选修4二轮专题练——等效平衡专练【精编23题】(已下线)第23讲 化学平衡状态 化学平衡的移动 (精讲)——2021年高考化学一轮复习讲练测(已下线)第七单元 化学反应速率与化学平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省宁波市镇海中学2022-2023学年高三上学期(10月)选考模拟一化学试题
3 . 燃煤烟气的脱硫脱硝是目前研究的热点。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ•mol-1
③H2O(g)=H2O(l) △H=-44 kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l) 的热化学方程式_________ 。
(2)某科研小组研究臭氧氧化--碱吸收法同时脱除SO2和NO工艺,氧化过程反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+ O3(g) ⇌NO2(g)+O2(g) △H1 = -200.9 kJ•mol-1 Ea1 = 3.2 kJ•mol-1
反应Ⅱ:SO2(g)+ O3(g) ⇌SO3(g)+O2(g) △H2 = -241.6 kJ•mol-1 Ea2 = 58 kJ•mol-1
已知该体系中臭氧发生分解反应:2O3(g) ⇌3O2(g)。请回答:
其它条件不变,每次向容积为2L的反应器中充入含1.0 mol NO、1.0 mol SO2的模拟烟气和2.0 mol O3,改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示:
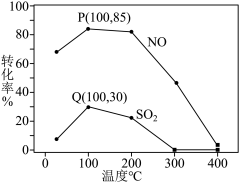
①由图可知相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因_______ 。
②下列说法正确的是____________ 。
A.P点一定为平衡状态点
B.温度高于200℃后,NO和SO2的转化率随温度升高显著下降、最后几乎为零
C.其它条件不变,若缩小反应器的容积可提高NO和SO2的转化率
③假设100℃时P(NO转化率为85%)、Q(SO2转化率为30%)均为平衡点,此时反应时间为10分钟,发生分解反应的臭氧占充入臭氧总量的10%,则体系中剩余O3的物质的量是_______ mol;NO的平均反应速率为_______________ ;反应Ⅱ在此时的平衡常数为_______________ 。
(3)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:
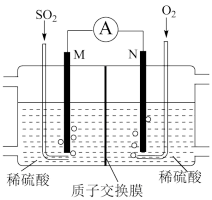
①M极发生的电极反应式为____________ 。
②当外电路通过0.2 mol电子时,质子交换膜左侧的溶液质量_____ (填“增大”或“减小”)_______ 克。
(1)用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574 kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ•mol-1
③H2O(g)=H2O(l) △H=-44 kJ•mol-1
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(l) 的热化学方程式
(2)某科研小组研究臭氧氧化--碱吸收法同时脱除SO2和NO工艺,氧化过程反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+ O3(g) ⇌NO2(g)+O2(g) △H1 = -200.9 kJ•mol-1 Ea1 = 3.2 kJ•mol-1
反应Ⅱ:SO2(g)+ O3(g) ⇌SO3(g)+O2(g) △H2 = -241.6 kJ•mol-1 Ea2 = 58 kJ•mol-1
已知该体系中臭氧发生分解反应:2O3(g) ⇌3O2(g)。请回答:
其它条件不变,每次向容积为2L的反应器中充入含1.0 mol NO、1.0 mol SO2的模拟烟气和2.0 mol O3,改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示:

①由图可知相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因
②下列说法正确的是
A.P点一定为平衡状态点
B.温度高于200℃后,NO和SO2的转化率随温度升高显著下降、最后几乎为零
C.其它条件不变,若缩小反应器的容积可提高NO和SO2的转化率
③假设100℃时P(NO转化率为85%)、Q(SO2转化率为30%)均为平衡点,此时反应时间为10分钟,发生分解反应的臭氧占充入臭氧总量的10%,则体系中剩余O3的物质的量是
(3)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能:

①M极发生的电极反应式为
②当外电路通过0.2 mol电子时,质子交换膜左侧的溶液质量
您最近一年使用:0次
2019-11-20更新
|
662次组卷
|
2卷引用:福建省平和一中、南靖一中等五校2019-2020学年高二年上学期期中联考化学试题
解题方法
4 . 能源是人类生存与发展必不可缺的物质,对传统能源进行脱硫、脱硝处理,能提高能源在能源消费中的比例是改变目前我国频发的雾霾天气的有效措施。
(1)肼(N2H4)和化合物甲是一种重要的火箭推进剂,甲分子与肼分子具有相同的电子数,二者反应的生成物中有10e-分子,另一种生成物为极稳定的单质,写出该反应的化学方程式__________________ 。
(2)对燃煤产生的尾气进行回收处理,有助于空气质量的改善,还能变废为宝,尾气处理过程中涉及到的主要反应如下:
①2CO(g)+SO2(g)=S(g)+2CO2(g) △H=十8.0 kJ·mol-1
②2H2 (g)+SO2(g)=S(g)+2H2O(g) △H=+90.4 kJ·mol-1
③2CO(g)+O2 (g) =2CO2 (g) △H= -566.0 kJ·mol-1
④2H2 (g)+O2 (g) =2H2O(g) △H =-483.6 kJ·mol-1
S(g)与O2(g)反应生成SO2(g)的热化学方程式为__________________ 。
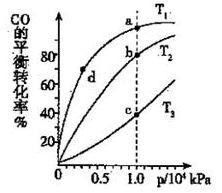
(3)煤炭液化也有助于减少雾霾天气的发生,液化反应之一为:CO(g)+2H2(g) CH3OH(g)(正反应放热);按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为
CH3OH(g)(正反应放热);按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为__________ ;实际生产条件控制在T 1°C、1×106Pa左右,选择此压强的理由是________ 。
(4)工业上生产新能源二甲醚(CH3OCH3)的原理之一为:2CO(g)+6H2(g) CH3OCH3(g)+3H2O(g),相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol/L)及正逆反应速率之间的关系如下表所示:
CH3OCH3(g)+3H2O(g),相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol/L)及正逆反应速率之间的关系如下表所示:
填写表中空白处,并写出其推测过程___________ 。
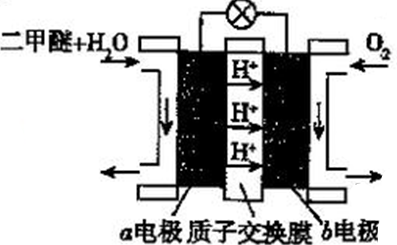
(5)二甲醚(燃烧热为1455kJ/mol)燃料电池是一种绿色电池,其工作原理如图所示,a、b均为惰性电极,a极的电极反应式为________________________ ;当消耗1molO2时,通过质子交换膜的质子数为_________ NA;若电池工作时消耗1mol二甲醚所能产生的最大电能为1320kJ,则该燃料电池的工作效率为________ (燃烧电池的工作效率是指电池所能产生的最大电能与燃料燃烧时所能释放的全部热能之比)。
(1)肼(N2H4)和化合物甲是一种重要的火箭推进剂,甲分子与肼分子具有相同的电子数,二者反应的生成物中有10e-分子,另一种生成物为极稳定的单质,写出该反应的化学方程式
(2)对燃煤产生的尾气进行回收处理,有助于空气质量的改善,还能变废为宝,尾气处理过程中涉及到的主要反应如下:
①2CO(g)+SO2(g)=S(g)+2CO2(g) △H=十8.0 kJ·mol-1
②2H2 (g)+SO2(g)=S(g)+2H2O(g) △H=+90.4 kJ·mol-1
③2CO(g)+O2 (g) =2CO2 (g) △H= -566.0 kJ·mol-1
④2H2 (g)+O2 (g) =2H2O(g) △H =-483.6 kJ·mol-1
S(g)与O2(g)反应生成SO2(g)的热化学方程式为
(3)煤炭液化也有助于减少雾霾天气的发生,液化反应之一为:CO(g)+2H2(g)
 CH3OH(g)(正反应放热);按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为
CH3OH(g)(正反应放热);按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示,则正反应速率:v(a)、v(b)、v(c)、v(d)由小到大的顺序为
(4)工业上生产新能源二甲醚(CH3OCH3)的原理之一为:2CO(g)+6H2(g)
 CH3OCH3(g)+3H2O(g),相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol/L)及正逆反应速率之间的关系如下表所示:
CH3OCH3(g)+3H2O(g),相同温度下,在两个容器中进行上述反应,某时刻两容器中各气态物质的浓度(mol/L)及正逆反应速率之间的关系如下表所示:容器 | c(CO) | c(H2) | c(CH3OCH3) | c(H2O) | v(正)与v(逆)大小比较 |
I | 1.0×10-2 | 1.0×10-2 | 1.0×10-4 | 1.0×10-4 | v(正)= v(逆) |
II | 2.0×10-2 | 1.0×10-2 | 1.0×10-4 | 2.0×10-4 | v(正) |
(5)二甲醚(燃烧热为1455kJ/mol)燃料电池是一种绿色电池,其工作原理如图所示,a、b均为惰性电极,a极的电极反应式为

您最近一年使用:0次



