23-24高二上·全国·期末
1 . 研究碳、氮、硫等元素化合物的性质或转化对建设生态文明,美丽中国具有重要意义。
(1)基态硫原子的价层电子轨道表示式为:___________ 。
(2) 加速臭氧层被破坏,其反应过程如下图所示:
加速臭氧层被破坏,其反应过程如下图所示:
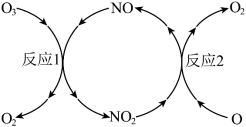
已知: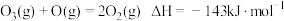
反应1: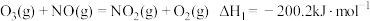 。
。
反应2的热化学方程式为___________ 。
(3)工业上以 和
和 为原料合成甲醇的反应:
为原料合成甲醇的反应: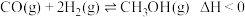 ,在容积为
,在容积为 的恒容容器中,分别在
的恒容容器中,分别在 温度下合成甲醇。如图是不同温度下
温度下合成甲醇。如图是不同温度下 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为 )与
)与 平衡转化率的关系。
平衡转化率的关系。

①判断
___________  (选填“<”、“>”或“=”);
(选填“<”、“>”或“=”);
②若a点达到平衡的时间是5分钟,从反应开始到平衡用 表示的反应速率为
表示的反应速率为
_______ ;
③d点的平衡常数的值为___________ ;
④a点状态下再通入 和
和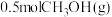 ,平衡
,平衡______ 移动(选填“正向”、“逆向”或“不”);
⑤a、b、c三点 转化率由大到小的顺序是
转化率由大到小的顺序是___________ 。
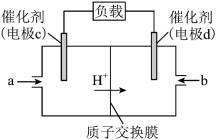
(4)CH3OH和O2组合形成的燃料电池的结构如图所示,质子(H+)交换膜左右两侧的溶液均为1L2mol/L的H2SO4溶液。电极c是___________ (填“正”或“负”)极,写出物质a在电极c上发生的反应式为___________ 。
(1)基态硫原子的价层电子轨道表示式为:
(2)
 加速臭氧层被破坏,其反应过程如下图所示:
加速臭氧层被破坏,其反应过程如下图所示:
已知:
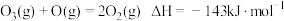
反应1:
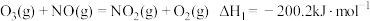 。
。反应2的热化学方程式为
(3)工业上以
 和
和 为原料合成甲醇的反应:
为原料合成甲醇的反应: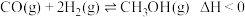 ,在容积为
,在容积为 的恒容容器中,分别在
的恒容容器中,分别在 温度下合成甲醇。如图是不同温度下
温度下合成甲醇。如图是不同温度下 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为 )与
)与 平衡转化率的关系。
平衡转化率的关系。
①判断

 (选填“<”、“>”或“=”);
(选填“<”、“>”或“=”);②若a点达到平衡的时间是5分钟,从反应开始到平衡用
 表示的反应速率为
表示的反应速率为
③d点的平衡常数的值为
④a点状态下再通入
 和
和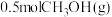 ,平衡
,平衡⑤a、b、c三点
 转化率由大到小的顺序是
转化率由大到小的顺序是(4)CH3OH和O2组合形成的燃料电池的结构如图所示,质子(H+)交换膜左右两侧的溶液均为1L2mol/L的H2SO4溶液。电极c是

您最近一年使用:0次
名校
2 . 研究碳、氮、硫等元素化合物的性质或转化对建设生态文明,美丽中国具有重要意义。
(1)基态硫原子的价层电子轨道表示式为:___________ 。
(2) 加速臭氧层被破坏,其反应过程如下图所示:
加速臭氧层被破坏,其反应过程如下图所示:
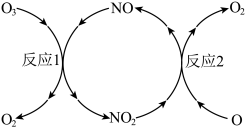
已知: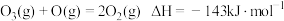
反应1: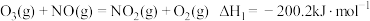 。
。
反应2的热化学方程式为___________ 。
(3)工业上以 和
和 为原料合成甲醇的反应:
为原料合成甲醇的反应: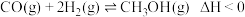 ,在容积为
,在容积为 的恒容容器中,分别在
的恒容容器中,分别在 温度下合成甲醇。如图是不同温度下
温度下合成甲醇。如图是不同温度下 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为 )与
)与 平衡转化率的关系。
平衡转化率的关系。

①判断
___________  (选填“<”、“>”或“=”);
(选填“<”、“>”或“=”);
②若a点达到平衡的时间是5分钟,从反应开始到平衡用 表示的反应速率为
表示的反应速率为
___________ ;
③d点的平衡常数的值为___________ ;
④a点状态下再通入 和
和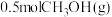 ,平衡
,平衡___________ 移动(选填“正向”、“逆向”或“不”);
⑤a、b、c三点 转化率由大到小的顺序是
转化率由大到小的顺序是___________ 。
(1)基态硫原子的价层电子轨道表示式为:
(2)
 加速臭氧层被破坏,其反应过程如下图所示:
加速臭氧层被破坏,其反应过程如下图所示:
已知:
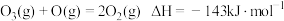
反应1:
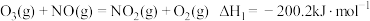 。
。反应2的热化学方程式为
(3)工业上以
 和
和 为原料合成甲醇的反应:
为原料合成甲醇的反应: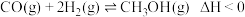 ,在容积为
,在容积为 的恒容容器中,分别在
的恒容容器中,分别在 温度下合成甲醇。如图是不同温度下
温度下合成甲醇。如图是不同温度下 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为 )与
)与 平衡转化率的关系。
平衡转化率的关系。
①判断

 (选填“<”、“>”或“=”);
(选填“<”、“>”或“=”);②若a点达到平衡的时间是5分钟,从反应开始到平衡用
 表示的反应速率为
表示的反应速率为
③d点的平衡常数的值为
④a点状态下再通入
 和
和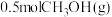 ,平衡
,平衡⑤a、b、c三点
 转化率由大到小的顺序是
转化率由大到小的顺序是
您最近一年使用:0次
解题方法
3 . 碳中和作为一种新型环保形式,目前已经被越来越多的大型活动和会议采用。回答下列有关问题:
(1)利用 合成二甲醚有两种工艺。
合成二甲醚有两种工艺。
工艺1:涉及以下主要反应:
Ⅰ.甲醇的合成:
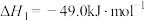
Ⅱ.逆水汽变换:
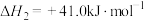
Ⅲ.甲醇脱水:

工艺2:利用 直接加氢合成
直接加氢合成 (反应Ⅳ)
(反应Ⅳ)
①据上述信息可知反应Ⅳ的热化学方程式为___________ ,反应Ⅰ低温___________ 自发进行(填“能”、“不能”)。
②恒温恒容情况下,下列说法能判断反应Ⅳ达到平衡的是___________ 。
A.气体物质中碳元素与氧元素的质量比不变
B.容器内 浓度保持不变
浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)工艺1需先合成甲醇。在不同压强下,按照 投料合成甲醇,实验测定
投料合成甲醇,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图甲、乙所示。
的平衡产率随温度的变化关系如下图甲、乙所示。
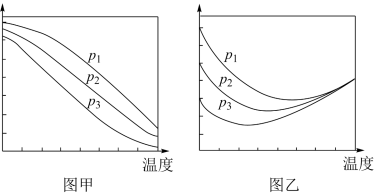
①下列说法正确的是___________ 。
A.图甲纵坐标表示 的平衡产率
的平衡产率
B.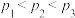
C.为了同时提高 的平衡转化率和
的平衡转化率和 的平衡产率,应选择低温、高压条件
的平衡产率,应选择低温、高压条件
D.一定温度压强下,提高 的平衡转化率的主要方向是寻找活性更高的催化剂
的平衡转化率的主要方向是寻找活性更高的催化剂
②图乙中,某温度时,三条曲线几乎交于一点的原因是___________ 。
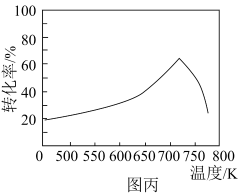
(3)对于合成甲醇的反应:
 ,一定条件下,单位时间内不同温度下测定的
,一定条件下,单位时间内不同温度下测定的 转化率如图丙所示。温度高于
转化率如图丙所示。温度高于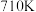 时,随温度的升高
时,随温度的升高 转化率降低的原因可能是
转化率降低的原因可能是___________ 。
(4) 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
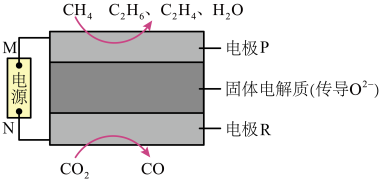
图丁
①电极M为电源的___________ 极;
②电极R上发生的电极反应为___________ 。
(1)利用
 合成二甲醚有两种工艺。
合成二甲醚有两种工艺。工艺1:涉及以下主要反应:
Ⅰ.甲醇的合成:

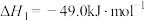
Ⅱ.逆水汽变换:

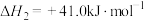
Ⅲ.甲醇脱水:


工艺2:利用
 直接加氢合成
直接加氢合成 (反应Ⅳ)
(反应Ⅳ)①据上述信息可知反应Ⅳ的热化学方程式为
②恒温恒容情况下,下列说法能判断反应Ⅳ达到平衡的是
A.气体物质中碳元素与氧元素的质量比不变
B.容器内
 浓度保持不变
浓度保持不变C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)工艺1需先合成甲醇。在不同压强下,按照
 投料合成甲醇,实验测定
投料合成甲醇,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图甲、乙所示。
的平衡产率随温度的变化关系如下图甲、乙所示。
①下列说法正确的是
A.图甲纵坐标表示
 的平衡产率
的平衡产率B.
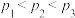
C.为了同时提高
 的平衡转化率和
的平衡转化率和 的平衡产率,应选择低温、高压条件
的平衡产率,应选择低温、高压条件D.一定温度压强下,提高
 的平衡转化率的主要方向是寻找活性更高的催化剂
的平衡转化率的主要方向是寻找活性更高的催化剂②图乙中,某温度时,三条曲线几乎交于一点的原因是
(3)对于合成甲醇的反应:

 ,一定条件下,单位时间内不同温度下测定的
,一定条件下,单位时间内不同温度下测定的 转化率如图丙所示。温度高于
转化率如图丙所示。温度高于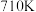 时,随温度的升高
时,随温度的升高 转化率降低的原因可能是
转化率降低的原因可能是
(4)
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
图丁
①电极M为电源的
②电极R上发生的电极反应为
您最近一年使用:0次
4 . 研究碳、氮、硫等元素化合物的性质或转化对建设生态文明,美丽中国具有重要意义。
(1)基态氮原子的价层电子轨道表示式为:______ 。
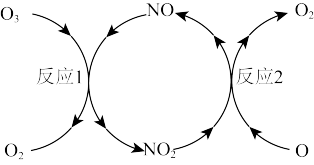
(2)NO加速臭氧层被破坏,其反应过程如下图所示:
已知: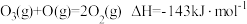
反应1: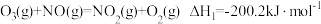 。
。
反应2的热化学方程式为___________ 。
(3)工业上以CO和 为原料合成甲醇的反应:
为原料合成甲醇的反应: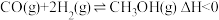 ,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
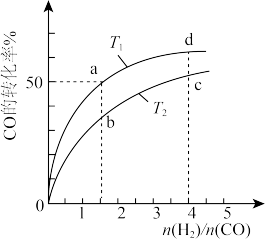
①判断T1___________ T2 (选填“<”、“>”或“=”);
②若a点达到平衡的时间是10分钟,从反应开始到平衡用H2表示的反应速率为
___________ ;
③该反应平衡常数的表达式为K=___________ ,d点的平衡常数的值为___________ ;
④a点状态下再通入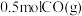 和
和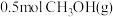 ,平衡
,平衡____ 移动(选填“正向”、“逆向”或“不”);
⑤a、b、c三点H2转化率由大到小的顺序是___________ 。
(1)基态氮原子的价层电子轨道表示式为:
(2)NO加速臭氧层被破坏,其反应过程如下图所示:

已知:
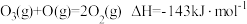
反应1:
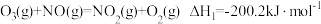 。
。反应2的热化学方程式为
(3)工业上以CO和
 为原料合成甲醇的反应:
为原料合成甲醇的反应: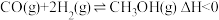 ,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
,在容积为1L的恒容容器中,分别在T1、T2温度下合成甲醇。如图是不同温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。
①判断T1
②若a点达到平衡的时间是10分钟,从反应开始到平衡用H2表示的反应速率为

③该反应平衡常数的表达式为K=
④a点状态下再通入
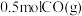 和
和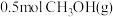 ,平衡
,平衡⑤a、b、c三点H2转化率由大到小的顺序是
您最近一年使用:0次
2022-02-16更新
|
302次组卷
|
2卷引用:江西省吉安市第三中学2022-2023学年高二上学期1月期末考试化学试题



