研究碳、氮、硫等元素化合物的性质或转化对建设生态文明,美丽中国具有重要意义。
(1)基态硫原子的价层电子轨道表示式为:___________ 。
(2) 加速臭氧层被破坏,其反应过程如下图所示:
加速臭氧层被破坏,其反应过程如下图所示:
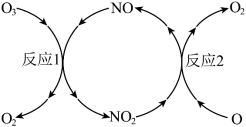
已知: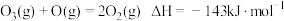
反应1: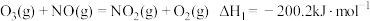 。
。
反应2的热化学方程式为___________ 。
(3)工业上以 和
和 为原料合成甲醇的反应:
为原料合成甲醇的反应: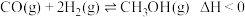 ,在容积为
,在容积为 的恒容容器中,分别在
的恒容容器中,分别在 温度下合成甲醇。如图是不同温度下
温度下合成甲醇。如图是不同温度下 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为 )与
)与 平衡转化率的关系。
平衡转化率的关系。

①判断
___________  (选填“<”、“>”或“=”);
(选填“<”、“>”或“=”);
②若a点达到平衡的时间是5分钟,从反应开始到平衡用 表示的反应速率为
表示的反应速率为
_______ ;
③d点的平衡常数的值为___________ ;
④a点状态下再通入 和
和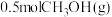 ,平衡
,平衡______ 移动(选填“正向”、“逆向”或“不”);
⑤a、b、c三点 转化率由大到小的顺序是
转化率由大到小的顺序是___________ 。
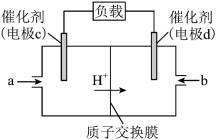
(4)CH3OH和O2组合形成的燃料电池的结构如图所示,质子(H+)交换膜左右两侧的溶液均为1L2mol/L的H2SO4溶液。电极c是___________ (填“正”或“负”)极,写出物质a在电极c上发生的反应式为___________ 。
(1)基态硫原子的价层电子轨道表示式为:
(2)
 加速臭氧层被破坏,其反应过程如下图所示:
加速臭氧层被破坏,其反应过程如下图所示:
已知:
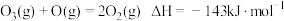
反应1:
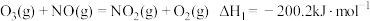 。
。反应2的热化学方程式为
(3)工业上以
 和
和 为原料合成甲醇的反应:
为原料合成甲醇的反应: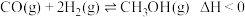 ,在容积为
,在容积为 的恒容容器中,分别在
的恒容容器中,分别在 温度下合成甲醇。如图是不同温度下
温度下合成甲醇。如图是不同温度下 和
和 的起始组成比(起始时
的起始组成比(起始时 的物质的量均为
的物质的量均为 )与
)与 平衡转化率的关系。
平衡转化率的关系。
①判断

 (选填“<”、“>”或“=”);
(选填“<”、“>”或“=”);②若a点达到平衡的时间是5分钟,从反应开始到平衡用
 表示的反应速率为
表示的反应速率为
③d点的平衡常数的值为
④a点状态下再通入
 和
和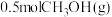 ,平衡
,平衡⑤a、b、c三点
 转化率由大到小的顺序是
转化率由大到小的顺序是(4)CH3OH和O2组合形成的燃料电池的结构如图所示,质子(H+)交换膜左右两侧的溶液均为1L2mol/L的H2SO4溶液。电极c是

23-24高二上·全国·期末 查看更多[1]
(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
更新时间:2023-12-30 22:49:17
|
相似题推荐
【推荐1】近年来我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年头现“碳达峰”,2060年实现“碳中和”。因此将 转化为高附加值化学品成为科学家研究的重要课题。
转化为高附加值化学品成为科学家研究的重要课题。
工业上在Cu-ZnO催化下利用 发生如下反应ⅰ来生产甲醇,同时伴有反应ⅱ发生。
发生如下反应ⅰ来生产甲醇,同时伴有反应ⅱ发生。
反应ⅰ:

反应ⅱ:
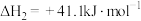
(1)反应 的
的
_______  。
。
(2)恒温下, 和
和 在恒容密闭容器发生反应ⅰ、ⅱ,下列能表明上述反应已达到平衡状态的有_______(填标号)。
在恒容密闭容器发生反应ⅰ、ⅱ,下列能表明上述反应已达到平衡状态的有_______(填标号)。
(3)不同条件下,按照 投料,
投料, 的平衡转化率如下图所示。
的平衡转化率如下图所示。
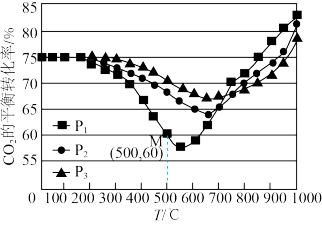
①压强P1、P2、P3由大到小的顺序是_______ 。压强为P1时,温度高于570℃之后,随着温度升高 平衡转化率增大的原因是
平衡转化率增大的原因是_______ 。
②图中点M(500,60),此时压强P1为0.2MPa, 的选择性为
的选择性为 (选择性:生成
(选择性:生成 所消耗的
所消耗的 占全部转化的
占全部转化的 的比)。则该温度时反应ⅰ的平衡常数
的比)。则该温度时反应ⅰ的平衡常数
_______  (分压=总压×物质的量分数)。
(分压=总压×物质的量分数)。
Ⅱ.电化学法还原二氧化碳制乙烯
(4)在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示,阴极电极反应式为_______ ,该装置中使用的是_______ (填“阴”或“阳”)离子交换膜。
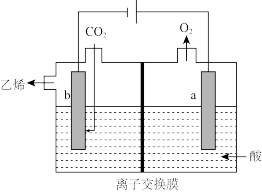
 转化为高附加值化学品成为科学家研究的重要课题。
转化为高附加值化学品成为科学家研究的重要课题。工业上在Cu-ZnO催化下利用
 发生如下反应ⅰ来生产甲醇,同时伴有反应ⅱ发生。
发生如下反应ⅰ来生产甲醇,同时伴有反应ⅱ发生。反应ⅰ:


反应ⅱ:

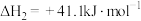
(1)反应
 的
的
 。
。(2)恒温下,
 和
和 在恒容密闭容器发生反应ⅰ、ⅱ,下列能表明上述反应已达到平衡状态的有_______(填标号)。
在恒容密闭容器发生反应ⅰ、ⅱ,下列能表明上述反应已达到平衡状态的有_______(填标号)。| A.每断裂1mol H-H键,同时生成1mol O-H键 |
B.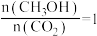 |
| C.混合气体的平均相对分子质量不变 |
| D.混合气体的压强不变 |
 投料,
投料, 的平衡转化率如下图所示。
的平衡转化率如下图所示。
①压强P1、P2、P3由大到小的顺序是
 平衡转化率增大的原因是
平衡转化率增大的原因是②图中点M(500,60),此时压强P1为0.2MPa,
 的选择性为
的选择性为 (选择性:生成
(选择性:生成 所消耗的
所消耗的 占全部转化的
占全部转化的 的比)。则该温度时反应ⅰ的平衡常数
的比)。则该温度时反应ⅰ的平衡常数
 (分压=总压×物质的量分数)。
(分压=总压×物质的量分数)。Ⅱ.电化学法还原二氧化碳制乙烯
(4)在强酸性溶液中通入二氧化碳,用惰性电极进行电解可制得乙烯,其原理如图所示,阴极电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,可能发生的反应如下:
ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-63 kJ·mol-1
ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2
ⅲ.CH3OH(g)⇌CO(g)+2H2(g) ΔH3=+99kJ·mol-1
回答下列问题:
(1)反应ⅰ的平衡常数表达式K=__ ;计算ΔH2=__ kJ·mol-1。
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。
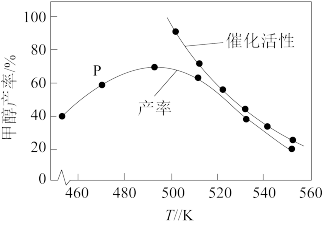
温度为470K时,图中P点__ (填“是”或“不是”)处于平衡状态。在490K之前,甲醇产率随着温度升高而增大的原因是__ ;490K之后,甲醇产率下降的可能原因是__ 。 (答一条即可)
(3)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在__ 极,该电极反应式是__ 。
ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-63 kJ·mol-1
ⅱ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH2
ⅲ.CH3OH(g)⇌CO(g)+2H2(g) ΔH3=+99kJ·mol-1
回答下列问题:
(1)反应ⅰ的平衡常数表达式K=
(2)一定比例的合成气在装有催化剂的反应器中反应12小时。体系中甲醇的产率和催化剂的催化活性与温度的关系如图所示。

温度为470K时,图中P点
(3)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】将二氧化碳还原转化为有用的化学物质是目前研究的热点之一。
(1)1945年Ipatieff等首次提出可在铜铝催化剂上用CO2加氢合成甲醇。已知发生的主要反应的热化学方程式如下:
CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41.17 kJ/mol
CO(g)+H2O(g) △H1=+41.17 kJ/mol
CO2+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
CO(g)+2H2(g) CH3OH(g) △H3=-90.64 kJ/mol
CH3OH(g) △H3=-90.64 kJ/mol
则:①△H2= 1 kJ/mol。
②如图1所示,关闭K,向A中充入1 mol CO2、3 mol H2,向B中充入2 mol CO2、6 mol H2,起始时VA=VB=aL。在相同条件下,两容器中只发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),达到平衡时VB=0.8a L,则B中CO2的转化率为
CH3OH(g)+H2O(g),达到平衡时VB=0.8a L,则B中CO2的转化率为 2 。打开K,过一段时间重新达平衡,此时B的体积为 3 L(用含a的代数式表示,连通管中气体体积不计)。
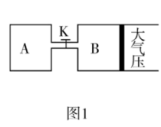
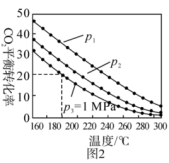
③CO2和H2以物质的量之比为1:3通入某密闭容器中,只发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),CO2的平衡转化率与温度、气体的总压强的关系如图2所示,则p1
CH3OH(g)+H2O(g),CO2的平衡转化率与温度、气体的总压强的关系如图2所示,则p1 4 p2(填“>”、“<”或“=”)。已知p3=1 MPa,则a点压强平衡常数Kp= 5 (Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
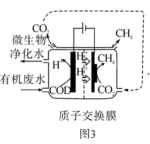
(2)利用微生物燃料电池技术可将CO2转化为甲烷(如图3所示),则阴极的电极反应式为 6 。该技术将有机废水中的碳元素最终转化为 7 (填分子式)。
(1)1945年Ipatieff等首次提出可在铜铝催化剂上用CO2加氢合成甲醇。已知发生的主要反应的热化学方程式如下:
CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41.17 kJ/mol
CO(g)+H2O(g) △H1=+41.17 kJ/molCO2+3H2(g)
 CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2CO(g)+2H2(g)
 CH3OH(g) △H3=-90.64 kJ/mol
CH3OH(g) △H3=-90.64 kJ/mol则:①△H2=
②如图1所示,关闭K,向A中充入1 mol CO2、3 mol H2,向B中充入2 mol CO2、6 mol H2,起始时VA=VB=aL。在相同条件下,两容器中只发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),达到平衡时VB=0.8a L,则B中CO2的转化率为
CH3OH(g)+H2O(g),达到平衡时VB=0.8a L,则B中CO2的转化率为
③CO2和H2以物质的量之比为1:3通入某密闭容器中,只发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),CO2的平衡转化率与温度、气体的总压强的关系如图2所示,则p1
CH3OH(g)+H2O(g),CO2的平衡转化率与温度、气体的总压强的关系如图2所示,则p1
(2)利用微生物燃料电池技术可将CO2转化为甲烷(如图3所示),则阴极的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应N2+3H2 2NH3的平衡常数K值和温度的关系如下:
2NH3的平衡常数K值和温度的关系如下:
I(1)①由表中数据可知该反应为放热反应,理由是________________ 。
②理论上,为了增大平衡时H2的转化率,可采取的措施是______________ (填字母序号)。
a.增大压强 b.使用合适的催化剂 c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2还可通过反应CO(g)+H2O(g) CO2(g)+H2(g)获取。T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为
CO2(g)+H2(g)获取。T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为________ 该温度下反应的平衡常数K值为________ 。
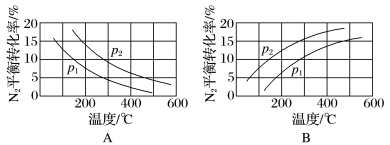
Ⅱ、(1)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,下图所示的图示中,正确的是________ (填“A”或“B”);比较p1、p2的大小关系:________ 。
(2)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8 mol。已知平衡时,容器压强为8 MPa,则平衡常数Kp=________ (用平衡分压代替浓度计算,分压=总压×物质的量分数)。
 2NH3的平衡常数K值和温度的关系如下:
2NH3的平衡常数K值和温度的关系如下:| 温度/℃ | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
I(1)①由表中数据可知该反应为放热反应,理由是
②理论上,为了增大平衡时H2的转化率,可采取的措施是
a.增大压强 b.使用合适的催化剂 c.升高温度 d.及时分离出产物中的NH3
(2)原料气H2还可通过反应CO(g)+H2O(g)
 CO2(g)+H2(g)获取。T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为
CO2(g)+H2(g)获取。T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为Ⅱ、(1)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(p1、p2)下随温度变化的曲线,下图所示的图示中,正确的是

(2)在一定温度下,将1 mol N2和3 mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8 mol。已知平衡时,容器压强为8 MPa,则平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】利用反应I可用于在国际空间站中处理二氧化碳,同时伴有副反应II发生。
主反应I:
副反应II:
1.几种化学键的键能如表所示:
表中
___________ 。
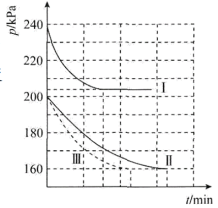
为了进一步研究上述两个反应,某小组在三个10L的刚性容器中,分别充入1mol 和4mol
和4mol ,在三种不同实验条件(见下表)下进行两个反应,反应体系的总压强(p)随时间变化情况如图所示:
,在三种不同实验条件(见下表)下进行两个反应,反应体系的总压强(p)随时间变化情况如图所示:
 ___________
___________ 。
。
3.曲线III对应的实验编号是___________。
4.若在曲线II条件下,10min达到平衡时生成1.2mol ,则10min内反应的平均速率
,则10min内反应的平均速率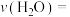
___________  。
。
5.该温度下反应II的平衡常数 ___________。
___________。
6.一定条件下反应I存在: 或
或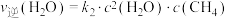 ,反应I的平衡常数
,反应I的平衡常数
___________ (用含 、
、 的代数式表示)。
的代数式表示)。
主反应I:

副反应II:

1.几种化学键的键能如表所示:
| 化学键 |  |  |  |  |
键能/( ) ) | 413 | 436 | 463 | a |

为了进一步研究上述两个反应,某小组在三个10L的刚性容器中,分别充入1mol
 和4mol
和4mol ,在三种不同实验条件(见下表)下进行两个反应,反应体系的总压强(p)随时间变化情况如图所示:
,在三种不同实验条件(见下表)下进行两个反应,反应体系的总压强(p)随时间变化情况如图所示:| 实验编号 | a | b | c |
| 温度/K |  |  |  |
催化剂的比表面积/(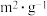 ) ) | 80 | 120 | 120 |
 ___________
___________ 。
。| A.大于 | B.等于 | C.小于 | D.无法确定 |
| A.a | B.b | C.c | D.无法确定 |
 ,则10min内反应的平均速率
,则10min内反应的平均速率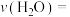
 。
。5.该温度下反应II的平衡常数
 ___________。
___________。| A.1.44 | B.0.44 | C.2.55 | D.0.55 |
 或
或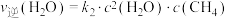 ,反应I的平衡常数
,反应I的平衡常数
 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
【推荐3】研究碳及其化合物的相互转化对能源的充分利用、低碳经济有着重要的作用。
(1)已知:①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+206.1kJ·mol−1
CO(g)+3H2(g) ΔH1=+206.1kJ·mol−1
②2H2(g)+CO(g) CH3OH(g) ΔH2=-128.3kJ·mol−1
CH3OH(g) ΔH2=-128.3kJ·mol−1
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6kJ·mol−1
若某反应的平衡常数表达式为:K=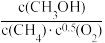 ,则此反应ΔH=
,则此反应ΔH=___________ kJ·mol−1。
(2)CH4-CO2催化重整对温室气体的减排具有重要意义。催化重整反应为:CH4(g)+CO2(g) 2CO(g)+2H2(g)ΔH=+247kJ·mol−1,平衡时CH4的转化率与温度和压强的关系如图所示。
2CO(g)+2H2(g)ΔH=+247kJ·mol−1,平衡时CH4的转化率与温度和压强的关系如图所示。___________ 。
②压强为P4时,在Y点:v正___________ v逆(填“>”、“<”或“=”)。
③图中W、X、Y、Z四点对应的反应的平衡常数K1、K2、K3、K4由大到小的顺序为___________ 。
(3)CO2加氢制备甲酸(HCOOH)可回收利用CO2,温度为T1时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) ΔH>0,化学平衡常数K=1,实验测得:v正=k正·c(CO2)·c(H2),v逆=k逆·c(HCOOH),k正、k逆为速率常数。
HCOOH(g) ΔH>0,化学平衡常数K=1,实验测得:v正=k正·c(CO2)·c(H2),v逆=k逆·c(HCOOH),k正、k逆为速率常数。
①当HCOOH的体积分数为25%时,CO2的转化率为___________ 。
②温度为T1,反应达到平衡时,k逆=___________ (用k正表示)。改变温度至T2,若k逆=0.9k正,则T1___________ T2(填“>”、“<”或“=”)。
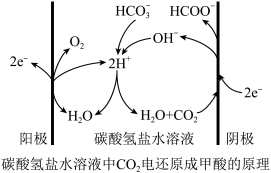
(4)采用电还原法也可将CO2转化为甲酸,在碳酸氢盐的水溶液中,CO2被还原成甲酸的原理如图所示。阴极的电极反应式是___________ 。
(1)已知:①CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1=+206.1kJ·mol−1
CO(g)+3H2(g) ΔH1=+206.1kJ·mol−1②2H2(g)+CO(g)
 CH3OH(g) ΔH2=-128.3kJ·mol−1
CH3OH(g) ΔH2=-128.3kJ·mol−1③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6kJ·mol−1
若某反应的平衡常数表达式为:K=
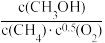 ,则此反应ΔH=
,则此反应ΔH=(2)CH4-CO2催化重整对温室气体的减排具有重要意义。催化重整反应为:CH4(g)+CO2(g)
 2CO(g)+2H2(g)ΔH=+247kJ·mol−1,平衡时CH4的转化率与温度和压强的关系如图所示。
2CO(g)+2H2(g)ΔH=+247kJ·mol−1,平衡时CH4的转化率与温度和压强的关系如图所示。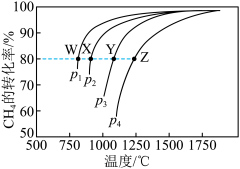
②压强为P4时,在Y点:v正
③图中W、X、Y、Z四点对应的反应的平衡常数K1、K2、K3、K4由大到小的顺序为
(3)CO2加氢制备甲酸(HCOOH)可回收利用CO2,温度为T1时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) ΔH>0,化学平衡常数K=1,实验测得:v正=k正·c(CO2)·c(H2),v逆=k逆·c(HCOOH),k正、k逆为速率常数。
HCOOH(g) ΔH>0,化学平衡常数K=1,实验测得:v正=k正·c(CO2)·c(H2),v逆=k逆·c(HCOOH),k正、k逆为速率常数。①当HCOOH的体积分数为25%时,CO2的转化率为
②温度为T1,反应达到平衡时,k逆=
(4)采用电还原法也可将CO2转化为甲酸,在碳酸氢盐的水溶液中,CO2被还原成甲酸的原理如图所示。阴极的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】将制得的锰粉碎后加入到SnCl2溶液中使其浸出(假定杂质不反应,溶液体积不变),发生反应Mn(s)+ Sn2+(aq) Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)。
Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)。
(1)为加快反应速率可以采取的措施有____________ 、____________ ;
(2)不考虑温度因素,一段时间后Mn的溶解速率加快,可能的原因是____________ 。
(3)下列能说明反应已达平衡的有____________ (填编号)。
A.溶液的颜色不发生变化 B.溶液中c(Mn2+)=c( Sn2+)
C.体系中固体的质量不变 D.Mn2+与Sn2+浓度的比值保持不变
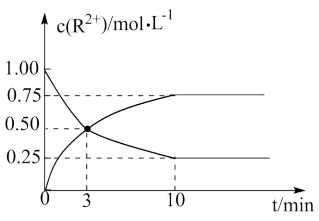
(4)室温下,测得溶液中阳离子浓度c(R2+)随时间的变化情况如下图所示,则上述反应的平衡常数K=____________ 。若其他条件不变,10min后向容器中迅速加入蒸馏水至溶液体积变为原来的2倍,则再次平衡时c(Mn2+) =____________ (不考虑离子水解的影响)。
(5)MnO2也可在MnSO4-H2SO4-H2O为体系的电解液中电解获得,其阳极反应式为______ 。
 Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)。
Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)。(1)为加快反应速率可以采取的措施有
(2)不考虑温度因素,一段时间后Mn的溶解速率加快,可能的原因是
(3)下列能说明反应已达平衡的有
A.溶液的颜色不发生变化 B.溶液中c(Mn2+)=c( Sn2+)
C.体系中固体的质量不变 D.Mn2+与Sn2+浓度的比值保持不变
(4)室温下,测得溶液中阳离子浓度c(R2+)随时间的变化情况如下图所示,则上述反应的平衡常数K=

(5)MnO2也可在MnSO4-H2SO4-H2O为体系的电解液中电解获得,其阳极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】“废气”的综合处理与应用技术是科研人员的重要研究课题,CO、SO2、NO2是重要的大气污染气体。
(1)捕集处理后的CO是制取新型能源二甲醚(CH3OCH3)的原料,已知:①CO(g)+H2O(g) CO2(g)+H2(g),△H1=-41.0kJ•mol-1,②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2=-49.0kJ•mol-1,③CH3OCH2(g)+H2O(g)
CO2(g)+H2(g),△H1=-41.0kJ•mol-1,②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2=-49.0kJ•mol-1,③CH3OCH2(g)+H2O(g)  2CH3OH(g)△H3=+23.5kJ•mol-1,则反应2CO(g)+4H2(g)
2CH3OH(g)△H3=+23.5kJ•mol-1,则反应2CO(g)+4H2(g)  CH3OCH2(g)+H2O(g)的△H=
CH3OCH2(g)+H2O(g)的△H=______ 。
(2)采用NaClO2溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性NaClO2溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表,依据表中数据,写出NaClO2溶液脱硝过程中发生的总反应的离子方程式:______ 。
(3)已知973K时,SO2与NO2反应生成SO3和NO,混合气体经冷凝分离出的SO3可用于制备硫酸。
①973K时测得:NO2(g) NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)⇌SO3(g)K3=20.则反应SO2(g)+NO2(g)
NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)⇌SO3(g)K3=20.则反应SO2(g)+NO2(g) SO3(g)+NO(g)的K3=
SO3(g)+NO(g)的K3=______ 。
②973K时,向体积为1L的恒容密闭容器中充入SO2、NO2各aml,平衡时SO2的转化率为______ 。
③恒压下SO2的分压p(SO2)随温度的变化如图所示。当温度升高时,SO2(g)+NO2(g) SO2(g)+NO(g)的化学平衡常数
SO2(g)+NO(g)的化学平衡常数______ (填“增大”或”减小”),判断理由是______ 。
(4)用纳米铁可去除污水中的NO ,反应的离子方程式为4Fe+NO
,反应的离子方程式为4Fe+NO +10H+=4Fe2++NH
+10H+=4Fe2++NH +3H2O;相同温度下,纳米铁粉去除不同水样中的NO
+3H2O;相同温度下,纳米铁粉去除不同水样中的NO 的速率有较大差异,下表中Ⅰ和Ⅱ产生差异的原因可能是
的速率有较大差异,下表中Ⅰ和Ⅱ产生差异的原因可能是______ ;II中0~20min内用NO 表示的平均反应速率为
表示的平均反应速率为______ mol•L-1•min-1。
(1)捕集处理后的CO是制取新型能源二甲醚(CH3OCH3)的原料,已知:①CO(g)+H2O(g)
 CO2(g)+H2(g),△H1=-41.0kJ•mol-1,②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2=-49.0kJ•mol-1,③CH3OCH2(g)+H2O(g)
CO2(g)+H2(g),△H1=-41.0kJ•mol-1,②CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H2=-49.0kJ•mol-1,③CH3OCH2(g)+H2O(g)  2CH3OH(g)△H3=+23.5kJ•mol-1,则反应2CO(g)+4H2(g)
2CH3OH(g)△H3=+23.5kJ•mol-1,则反应2CO(g)+4H2(g)  CH3OCH2(g)+H2O(g)的△H=
CH3OCH2(g)+H2O(g)的△H=(2)采用NaClO2溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性NaClO2溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表,依据表中数据,写出NaClO2溶液脱硝过程中发生的总反应的离子方程式:
离子 | NO | NO | Cl- |
c/(mol•L-1) | 2.0×10-4 | 1.0×10-4 | 1.75×10-4 |
①973K时测得:NO2(g)
 NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)⇌SO3(g)K3=20.则反应SO2(g)+NO2(g)
NO(g)+1/2O2(g)K1=0.018;SO2(g)1/2+O2(g)⇌SO3(g)K3=20.则反应SO2(g)+NO2(g) SO3(g)+NO(g)的K3=
SO3(g)+NO(g)的K3=②973K时,向体积为1L的恒容密闭容器中充入SO2、NO2各aml,平衡时SO2的转化率为
③恒压下SO2的分压p(SO2)随温度的变化如图所示。当温度升高时,SO2(g)+NO2(g)
 SO2(g)+NO(g)的化学平衡常数
SO2(g)+NO(g)的化学平衡常数(4)用纳米铁可去除污水中的NO
 ,反应的离子方程式为4Fe+NO
,反应的离子方程式为4Fe+NO +10H+=4Fe2++NH
+10H+=4Fe2++NH +3H2O;相同温度下,纳米铁粉去除不同水样中的NO
+3H2O;相同温度下,纳米铁粉去除不同水样中的NO 的速率有较大差异,下表中Ⅰ和Ⅱ产生差异的原因可能是
的速率有较大差异,下表中Ⅰ和Ⅱ产生差异的原因可能是 表示的平均反应速率为
表示的平均反应速率为反应时间/min | 0 | 10 | 20 | 30 | 40 | |
| I | c(NO | 8 | 3.2 | 1.6 | 0.8 | 0.64 |
| II | c(NO | 8 | 0.48 | 0.32 | 0.32 | 0.32 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】 还原重整
还原重整 既能减少二氧化碳排放,又能生产增值化学品,是实现“双碳”经济的有效途径之一、
既能减少二氧化碳排放,又能生产增值化学品,是实现“双碳”经济的有效途径之一、
(1)甲烷干法重整(1000℃)
ⅰ.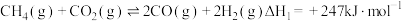
ⅱ.
①反应ⅰ的平衡常数表达式为______ 。
②对于反应ⅰ,既能加快反应速率又能提高 平衡转化率的措施是
平衡转化率的措施是_______ 。(写2条)反应ⅱ为副反应,生产中要尽可能控制该反应,减少水的生成。
(2)甲烷超干重整(750℃)


①
_______  。
。
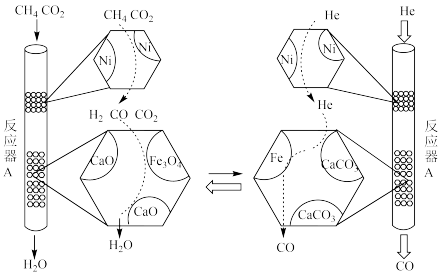
② 的转化原理如下图所示:恒压、750℃时,将混合气
的转化原理如下图所示:恒压、750℃时,将混合气 通入反应器
通入反应器 ,充分反应;待反应平衡后,改通
,充分反应;待反应平衡后,改通 气,吹出反应器
气,吹出反应器 内气体;如此往复切换通入的气体,实现
内气体;如此往复切换通入的气体,实现 的高效转化。
的高效转化。
ⅰ.基态 原子
原子 轨道能活化
轨道能活化 的简化电子排布式是
的简化电子排布式是________ 。
ⅱ.结合有关反应方程式,说明 对
对 氧化
氧化 反应的影响
反应的影响________ 。
ⅲ.反应达平衡后,改通 气,测得一段时间内
气,测得一段时间内 物质的量上升,解释
物质的量上升,解释 物质的量上升的原因
物质的量上升的原因___________ 。
(3)从能源利用的角度,分析甲烷超干重整法的优点:_______ 。
 还原重整
还原重整 既能减少二氧化碳排放,又能生产增值化学品,是实现“双碳”经济的有效途径之一、
既能减少二氧化碳排放,又能生产增值化学品,是实现“双碳”经济的有效途径之一、(1)甲烷干法重整(1000℃)
ⅰ.
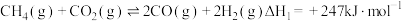
ⅱ.

①反应ⅰ的平衡常数表达式为
②对于反应ⅰ,既能加快反应速率又能提高
 平衡转化率的措施是
平衡转化率的措施是(2)甲烷超干重整(750℃)


①

 。
。②
 的转化原理如下图所示:恒压、750℃时,将混合气
的转化原理如下图所示:恒压、750℃时,将混合气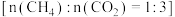 通入反应器
通入反应器 ,充分反应;待反应平衡后,改通
,充分反应;待反应平衡后,改通 气,吹出反应器
气,吹出反应器 内气体;如此往复切换通入的气体,实现
内气体;如此往复切换通入的气体,实现 的高效转化。
的高效转化。
ⅰ.基态
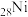 原子
原子 轨道能活化
轨道能活化 的简化电子排布式是
的简化电子排布式是ⅱ.结合有关反应方程式,说明
 对
对 氧化
氧化 反应的影响
反应的影响ⅲ.反应达平衡后,改通
 气,测得一段时间内
气,测得一段时间内 物质的量上升,解释
物质的量上升,解释 物质的量上升的原因
物质的量上升的原因(3)从能源利用的角度,分析甲烷超干重整法的优点:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】甲醇是性能优良的能源和车用燃料。
(1)工业上可用一氧化碳和氢气在催化剂作用下合成甲醇,研究该反应可能的历程,其中吸附在催化剂表面上的物种用*标注,该历程能量变化如图所示:

可知该历程的
_______ 0(填“大于”“等于”或“小于”),其中决速步骤的能垒为_______ eV,虚线框内最有可能发生的反应的化学方程式为_______ 。
(2)已知 (g)、CO(g)的燃烧热分别是
(g)、CO(g)的燃烧热分别是 和
和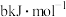 (a、b均小于0),
(a、b均小于0),
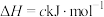 。则反应
。则反应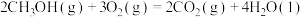 的
的
_______  。
。
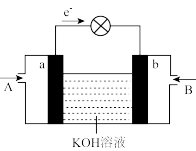
(3)如图是碱性甲醇燃料电池。a电极发生的电极反应式是_______ 。标准状况下,当电路中累计有2mol电子通过时,消耗的氧气体积至少为_______ L。
(1)工业上可用一氧化碳和氢气在催化剂作用下合成甲醇,研究该反应可能的历程,其中吸附在催化剂表面上的物种用*标注,该历程能量变化如图所示:

可知该历程的

(2)已知
 (g)、CO(g)的燃烧热分别是
(g)、CO(g)的燃烧热分别是 和
和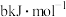 (a、b均小于0),
(a、b均小于0),
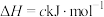 。则反应
。则反应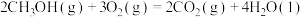 的
的
 。
。(3)如图是碱性甲醇燃料电池。a电极发生的电极反应式是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7 kJ·mol-1
CH3OH(g) △H1=-90.7 kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2 kJ·mol-1
CO2(g)+H2(g) △H3=-41.2 kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g) CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=___________ kJ·mol-1。
(2)反应②达平衡后采取下列措施,能提高CH3OCH3产率的有___________ (填字母,下同)。
(3)以下说法能说明反应3H2(g)+3CO(g)  CH3OCH3(g)+CO2(g)达到平衡状态的有
CH3OCH3(g)+CO2(g)达到平衡状态的有___________ 。
A.H2和CO2的浓度之比为3:1
B.单位时间内断裂3个H-H同时断裂1个C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(4)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g) 2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:
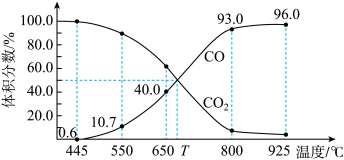
已知:气体分压(p分)=气体总压(p总)×体积分数。
①该反应△H___________ (填“>”“<”或“=”)0,550℃时,平衡后若充入惰性气体,平衡___________ (填“正移”“逆移”或“不移动”)。
②650℃时,反应达平衡后CO2的转化率为___________ (保留2位有效数字)。
③T℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=___________ p总。
(5)一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。图中b电极是___________ (填“正”或“负”)极,写出a电极反应式为___________ 。

①CO(g)+2H2(g)
 CH3OH(g) △H1=-90.7 kJ·mol-1
CH3OH(g) △H1=-90.7 kJ·mol-1②2CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5 kJ·mol-1③CO(g)+H2O(g)
 CO2(g)+H2(g) △H3=-41.2 kJ·mol-1
CO2(g)+H2(g) △H3=-41.2 kJ·mol-1回答下列问题:
(1)则反应3H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g)的△H=
CH3OCH3(g)+CO2(g)的△H=(2)反应②达平衡后采取下列措施,能提高CH3OCH3产率的有___________ (填字母,下同)。
| A.使用催化剂 | B.升高温度 | C.增大压强 | D.移出H2O |
 CH3OCH3(g)+CO2(g)达到平衡状态的有
CH3OCH3(g)+CO2(g)达到平衡状态的有A.H2和CO2的浓度之比为3:1
B.单位时间内断裂3个H-H同时断裂1个C=O
C.恒温恒容条件下,气体的密度保持不变
D.恒温恒压条件下,气体的平均摩尔质量保持不变
E.绝热体系中,体系的温度保持不变
(4)一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)
 2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如图所示:
已知:气体分压(p分)=气体总压(p总)×体积分数。
①该反应△H
②650℃时,反应达平衡后CO2的转化率为
③T℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=
(5)一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。图中b电极是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】工厂烟气(主要污染物 、NO)直接排放会造成空气污染,需处理后才能排放。
、NO)直接排放会造成空气污染,需处理后才能排放。
(1) 氧化。反应物断键吸收的能量越少,反应速率越快,
氧化。反应物断键吸收的能量越少,反应速率越快, 氧化
氧化 、NO反应的能量变化如图1和如图2所示。
、NO反应的能量变化如图1和如图2所示。
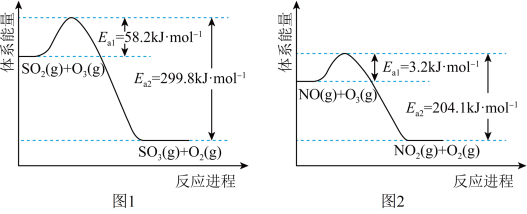
 氧化
氧化 、NO的反应为:
、NO的反应为:
A.
B.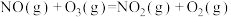
反应A_____ (填”放热”或“吸热”)_____  。
。
(2)某化学兴趣小组构想将NO转化为 脱除,装置如图3,电极为多孔惰性材料。则负极的电极反应式是
脱除,装置如图3,电极为多孔惰性材料。则负极的电极反应式是_____ 。
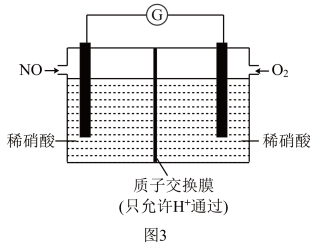
(3)“纳米零价铁— ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。
在一定温度下,将 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。

① 催化
催化 分解产生
分解产生 ,
, 将NO氧化为
将NO氧化为 的机理如图4所示,Y的化学式为
的机理如图4所示,Y的化学式为_____ 。
②NO与 反应生成
反应生成 的化学方程式为
的化学方程式为_____ 。
③纳米零价铁的作用是_____ 。
④NO脱除率随温度的变化如图5所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是_____ 。
 、NO)直接排放会造成空气污染,需处理后才能排放。
、NO)直接排放会造成空气污染,需处理后才能排放。(1)
 氧化。反应物断键吸收的能量越少,反应速率越快,
氧化。反应物断键吸收的能量越少,反应速率越快, 氧化
氧化 、NO反应的能量变化如图1和如图2所示。
、NO反应的能量变化如图1和如图2所示。
 氧化
氧化 、NO的反应为:
、NO的反应为:A.

B.
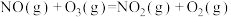
反应A
 。
。(2)某化学兴趣小组构想将NO转化为
 脱除,装置如图3,电极为多孔惰性材料。则负极的电极反应式是
脱除,装置如图3,电极为多孔惰性材料。则负极的电极反应式是
(3)“纳米零价铁—
 ”体系可将烟气中难溶的NO氧化为可溶的
”体系可将烟气中难溶的NO氧化为可溶的 。
。在一定温度下,将
 溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①
 催化
催化 分解产生
分解产生 ,
, 将NO氧化为
将NO氧化为 的机理如图4所示,Y的化学式为
的机理如图4所示,Y的化学式为②NO与
 反应生成
反应生成 的化学方程式为
的化学方程式为③纳米零价铁的作用是
④NO脱除率随温度的变化如图5所示。温度高于120℃时,NO脱除率随温度升高呈现下降趋势的主要原因是
您最近一年使用:0次




