1 . 认识化学反应的本质
化学反应的本质是旧化学键断裂和新化学键形成的过程。在反应中常伴有发光、发热、变色、生成沉淀物等。判断一个反应是否为化学反应的依据是反应是否生成新的物质。认识一个化学反应,不仅要着眼于物质的变化与能量的转化,更要从化学反应的程度与快慢来综合认识一个化学反应。
(1)下列属吸热反应的是___________。
(2)原电池能够实现化学能与电能的转化,下列反应一定不能设计成原电池的是___________。
(3)对于可逆反应 ,决定反应速率的主要因素是___________。
,决定反应速率的主要因素是___________。
(4)下列方法对于可逆反应 的反应速率没有影响的是___________。
的反应速率没有影响的是___________。
(5)一定条件下,在密闭容器中进行合成氨反应: ,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。
,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。
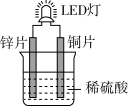
(6)某活动小组设计用如图装置使LED灯发光。下列有关该装置的说法正确的是___________。
(7)恒温恒容密闭容器中充入1mol 和3mol
和3mol ,一定条件下发生下列放热反应:
,一定条件下发生下列放热反应: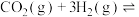
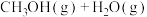 ,测得其中
,测得其中 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
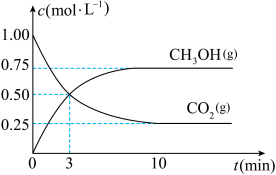
①由图可知,反应从开始至少需要___________ min,反应才达到化学平衡状态。达到化学平衡状态时容器中 的浓度为
的浓度为___________  。
。
②反应达到平衡状态过程中, 的平均反应速率为
的平均反应速率为___________  ,
, 的平均反应速率为
的平均反应速率为___________  。
。
③下列措施能使得该反应化学平衡向逆反应方向移动的是___________ 。
A.升高温度 B.降低温度 C.增大压强 D.分离出产物
化学反应的本质是旧化学键断裂和新化学键形成的过程。在反应中常伴有发光、发热、变色、生成沉淀物等。判断一个反应是否为化学反应的依据是反应是否生成新的物质。认识一个化学反应,不仅要着眼于物质的变化与能量的转化,更要从化学反应的程度与快慢来综合认识一个化学反应。
(1)下列属吸热反应的是___________。
| A.液态水汽化 | B.生石灰与水反应 | C.碳酸钙分解 | D.铝热反应 |
| A.化合反应 | B.分解反应 | C.置换反应 | D.复分解反应 |
 ,决定反应速率的主要因素是___________。
,决定反应速率的主要因素是___________。| A.温度 | B.压强 | C. 和 和 的性质 的性质 | D.催化剂 |
 的反应速率没有影响的是___________。
的反应速率没有影响的是___________。A.加入 | B.压强不变充入He | C.容积不变充入 | D.降低温度 |
 ,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。
,当正、逆反应速率相等且不等于0时,下列说法不正确的是___________。A. 、 、 、 、 的浓度相等 的浓度相等 |
B. 、 、 、 、 在容器中共存 在容器中共存 |
| C.反应已经达到化学平衡状态 |
D. 、 、 、 、 浓度不再改变 浓度不再改变 |

A.铜片是负极,其附近溶液变蓝,溶液中有 产生 产生 |
| B.如果将锌片换成铁片,电路中的电流方向将改变 |
| C.上述能量转化形式主要是“化学能-电能-光能” |
| D.如果将稀硫酸换成柠檬汁,LED灯将不会发光 |
 和3mol
和3mol ,一定条件下发生下列放热反应:
,一定条件下发生下列放热反应: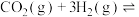
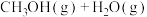 ,测得其中
,测得其中 和
和 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
①由图可知,反应从开始至少需要
 的浓度为
的浓度为 。
。②反应达到平衡状态过程中,
 的平均反应速率为
的平均反应速率为 ,
, 的平均反应速率为
的平均反应速率为 。
。③下列措施能使得该反应化学平衡向逆反应方向移动的是
A.升高温度 B.降低温度 C.增大压强 D.分离出产物

您最近一年使用:0次
2 . 水凝结成冰的过程中,下列分析不正确 的是
| A.该过程属于物理变化 | B.  |
| C.等质量水和冰所具有的内能不同 | D.该过程是熵减的过程 |
您最近一年使用:0次
2023-01-14更新
|
178次组卷
|
2卷引用:上海市宜川中学2022-2023学年高二下学期3月阶段测试化学试题
3 . 298K时,部分物质的相对能量如图所示。该温度下有关能量变化的说法正确的是


| A.热稳定性:C2H4(g)>C2H6(g) |
| B.CO(g)+H2O(g)=CO2(g)+H2(g)+QkJ,Q<0 |
| C.H2O(g)→H2O(l)是吸热过程 |
| D.CO完全燃烧的热化学方程式为:2CO(g)+O2(g)=2CO2(g)+566kJ |
您最近一年使用:0次
名校
解题方法
4 . 人类利用化学反应不仅可以创造新物质,还可以实现不同形式能量之间的转化。
(1)开发利用可再生能源受到世界各国的广泛关注。下列不属于可再生能源的是_______。
(2)下列反应中,生成物总能量低于反应物总能量的是_______。
(3)下列有关化学变化中能量变化的说法中,正确的是_______。
(4)图是有关反应过程与能量变化的示意图,由此可以推知:
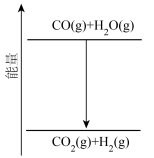
CO(g)+H2O(g)=CO2(g)+H2(g)是_______ 反应(填“吸热”或“放热”)
(1)开发利用可再生能源受到世界各国的广泛关注。下列不属于可再生能源的是_______。
| A.沼气 | B.水力发电 | C.太阳能 | D.清洁煤 |
| A.碳酸钙受热分解 | B.灼热的碳与二氧化碳反应 |
| C.酒精燃烧 | D.煤与高温下的水蒸气反应 |
| A.需要加热才能发生的反应一定是吸热反应 |
| B.放热反应在常温条件下一定能自发进行 |
| C.化学键断裂时会放出能量 |
| D.反应物和生成物所具有总能量的相对大小决定了化学反应是放热还是吸热 |

CO(g)+H2O(g)=CO2(g)+H2(g)是
您最近一年使用:0次
5 . 合成氨反应不具备的特征是
| A.放热 | B.熵增 | C.可逆 | D.气态 |
您最近一年使用:0次
6 . 下列反应形成新化学键释放的能量大于破坏旧化学键吸收的能量的是
| A.锌和盐酸反应生成氢气 | B.柠檬酸与碳酸氢钠溶液反应 |
| C.碳与二氧化碳共热生成一氧化碳 | D.碳酸钙受热分解 |
您最近一年使用:0次
2022-09-10更新
|
268次组卷
|
3卷引用:上海市位育中学2022-2023学年高二上学期9月阶段性练习化学试题
2022高二·上海·专题练习
解题方法
7 . 切开的金属Na暴露在空气中,其变化过程如图所示:
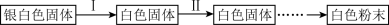
反应I的反应过程与能量变化的关系如图所示,请回答下列问题:
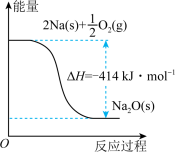
(1)反应I是_______ 反应(填“放热”或“吸热”),判断依_______ 。
(2)1molNa(s)被氧化成 molNa2O(s)的热化学方程式是
molNa2O(s)的热化学方程式是_______ 。
反应I的反应过程与能量变化的关系如图所示,请回答下列问题:

(1)反应I是
(2)1molNa(s)被氧化成
 molNa2O(s)的热化学方程式是
molNa2O(s)的热化学方程式是
您最近一年使用:0次
名校
8 . 下列应用涉及的核心化学反应中 的是
的是
 的是
的是| A.利用铝粉与氧化铁焊接铁轨 | B.用“水果电池”驱动时钟 |
C.硝酸工业中催化氧化 | D.工业冶炼金属镁 |
您最近一年使用:0次
名校
9 . 煤是重要能源。燃煤会释放 、
、 等有毒气体。消除有毒气体的研究和实践从未停止。用
等有毒气体。消除有毒气体的研究和实践从未停止。用 可消除
可消除 。
。
反应①: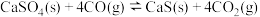 (放热反应)
(放热反应)
反应②: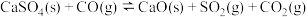 (吸热反应)
(吸热反应)
(1)其他条件不变,增加 的用量(质量),反应①的速率_______
的用量(质量),反应①的速率_______
(2)若在容积为1L的密闭装置中仅发生反应①,20分钟后,固体的质量减少了3.2g,则 的反应速率为_______,不能说明反应①一定达到平衡状态的是。
的反应速率为_______,不能说明反应①一定达到平衡状态的是。
(3)为了提高反应②的 的吸收率,可行的措施是
的吸收率,可行的措施是_______ 、_______ (2条)。
(4)补全图中反应②的能量变化示意图_____ (即注明生成物能量的大致位置)

(5)若反应①、②同时发生,一段时间后均到达了平衡,升高温度,均再次达到平衡,发现 的吸收率减小,分析可能的原因是
的吸收率减小,分析可能的原因是_______ 。
 、
、 等有毒气体。消除有毒气体的研究和实践从未停止。用
等有毒气体。消除有毒气体的研究和实践从未停止。用 可消除
可消除 。
。反应①:
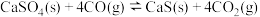 (放热反应)
(放热反应)反应②:
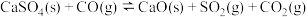 (吸热反应)
(吸热反应)(1)其他条件不变,增加
 的用量(质量),反应①的速率_______
的用量(质量),反应①的速率_______| A.增大 | B.减小 | C.不变 | D.无法判断 |
 的反应速率为_______,不能说明反应①一定达到平衡状态的是。
的反应速率为_______,不能说明反应①一定达到平衡状态的是。| A.压强不变 | B.气体的密度不变 |
C.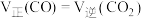 | D. 、 、 浓度相等 浓度相等 |
 的吸收率,可行的措施是
的吸收率,可行的措施是(4)补全图中反应②的能量变化示意图

(5)若反应①、②同时发生,一段时间后均到达了平衡,升高温度,均再次达到平衡,发现
 的吸收率减小,分析可能的原因是
的吸收率减小,分析可能的原因是
您最近一年使用:0次
10 . 在牙膏和一些药品中,常用轻质碳酸钙粉末作填充剂或载体。该轻质碳酸钙粉末的工业生产流程如图。

(1)化学反应还伴随着能量的变化,在第①、②步反应中,存在放热现象的是_______ (填序号);第①、②步反应的基本类型分别是_______ 、_______ 。
(2)使用轻质碳酸钙粉末作填充剂或载体的牙膏和一些药品有利于人体补钙,老年人缺钙会_______ 。
(3)用石灰乳可制取烧碱,写出反应的化学方程式_______ 。

(1)化学反应还伴随着能量的变化,在第①、②步反应中,存在放热现象的是
(2)使用轻质碳酸钙粉末作填充剂或载体的牙膏和一些药品有利于人体补钙,老年人缺钙会
(3)用石灰乳可制取烧碱,写出反应的化学方程式
您最近一年使用:0次



