1 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ/mol
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ/mol
总反应的△H=_______ kJ/mol;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是_______ (填标号),判断的理由是_______ 。
A.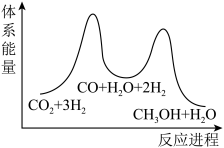 B.
B.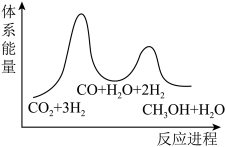
C.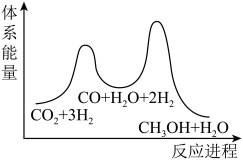 D.
D.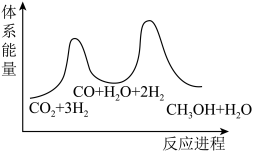
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
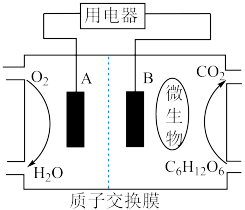
①B为生物燃料电池的_______ (填“正”或“负”)极。
②正极反应式为_______ 。
③电池工作过程中,H+将移向_______ (填“正”或“负”)极。
④在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是_______ 。
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ/mol
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ/mol
总反应的△H=
A.
 B.
B.
C.
 D.
D.
(2)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

①B为生物燃料电池的
②正极反应式为
③电池工作过程中,H+将移向
④在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是
您最近一年使用:0次
名校
2 . 为了研究反应 能量变化情况,某同学设计了如图所示装置。当向盛有
能量变化情况,某同学设计了如图所示装置。当向盛有 的试管中滴加试剂
的试管中滴加试剂 时,看到
时,看到 形管中甲处液面下降乙处液面上升。试回答下列问题:
形管中甲处液面下降乙处液面上升。试回答下列问题:
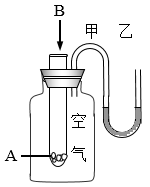
(1)该反应为___________ 反应(填“放热”或“吸热”)。
(2)物质中的化学能通过化学反应转化成___________ 释放出来。
(3)若甲烷的燃烧热为 ,写出表示甲烷燃烧热的热化学方程式
,写出表示甲烷燃烧热的热化学方程式___________ 。
(4)已知
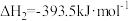
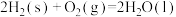
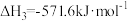 。
。
则高温下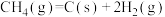

___________  。
。
 能量变化情况,某同学设计了如图所示装置。当向盛有
能量变化情况,某同学设计了如图所示装置。当向盛有 的试管中滴加试剂
的试管中滴加试剂 时,看到
时,看到 形管中甲处液面下降乙处液面上升。试回答下列问题:
形管中甲处液面下降乙处液面上升。试回答下列问题:
(1)该反应为
(2)物质中的化学能通过化学反应转化成
(3)若甲烷的燃烧热为
 ,写出表示甲烷燃烧热的热化学方程式
,写出表示甲烷燃烧热的热化学方程式(4)已知

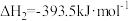
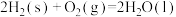
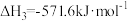 。
。则高温下
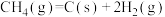

 。
。
您最近一年使用:0次
2021-11-01更新
|
220次组卷
|
3卷引用:西藏林芝市第二高级中学2021-2022学年高三下学期第四次月考理综化学试题
18-19高三·西藏拉萨·阶段练习
解题方法
3 . 空气质量评价的主要污染物为PM10、PM2.5、SO2、NO2、O3、CO等物质。脱硝(除NOx)技术和脱硫(除SO2)技术都是环境科学研究的热点,对于消除环境污染有重要意义。
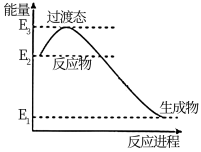
(1)已知在催化剂存在的条件下,H2可以将NO还原为N2。如图是一定条件下H2还原NO生成N2和1mol水蒸气的能量变化示意图。由图可看出此反应为:__________ 反应(填“放热”或“吸热”),写出该反应的热化学方程式:__________ (ΔH用E1、E2、E3表示)
(2)升高温度绝大多数反应的化学反应速率增大,但是2NO(g)+O2(g) 2NO2(g)的速率却随着温度的升高而减小。某化学小组为研究该特殊现象的实质原因,查阅资料知2NO(g)+O2(g)
2NO2(g)的速率却随着温度的升高而减小。某化学小组为研究该特殊现象的实质原因,查阅资料知2NO(g)+O2(g)  2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:
Ⅰ.2NO(g) N2O2(g)(快) ΔH1 < 0 ;v1正=k1正·c2(NO);v1逆=k1逆·c(N2O2)
N2O2(g)(快) ΔH1 < 0 ;v1正=k1正·c2(NO);v1逆=k1逆·c(N2O2)
Ⅱ.N2O2(g)+O2(g) 2NO2(g)(慢) ΔH2 < 0 ;v2正=k2正·c(N2O2)·c(O2); v2逆=k2逆·c2(NO2)
2NO2(g)(慢) ΔH2 < 0 ;v2正=k2正·c(N2O2)·c(O2); v2逆=k2逆·c2(NO2)
请回答下列问题:
① 一定温度下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,请写出此反应的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出此反应的平衡常数表达式K=__________ 。
② 决定2NO(g)+O2(g) 2NO2(g)反应速率的是反应Ⅱ,反应Ⅰ的活化能E1与反应Ⅱ的活化能E2的大小关系为E1
2NO2(g)反应速率的是反应Ⅱ,反应Ⅰ的活化能E1与反应Ⅱ的活化能E2的大小关系为E1__________ E2(填“ >”“<”或“=”)。根据速率方程分析,升高温度该反应速率减小的原因是__________ (填序号)。
A k2正增大,c(N2O2)增大 B k2正减小,c(N2O2)减小
C k2正增大,c(N2O2)减小 D k2正减小,c(N2O2)增大
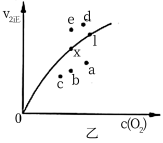
③ 由实验数据得到v2正~c(O2)的关系可如图表示。当X点升高到某一温度时,反应重新达到平衡,则变为相应的点为__________ (填字母)。
(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓,已知甲池中发生的反应为:
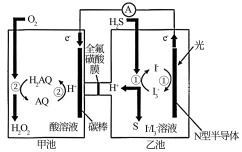
① 装置中H+从__________ 移向__________ (填“甲池”或“乙池”)。
(1)已知在催化剂存在的条件下,H2可以将NO还原为N2。如图是一定条件下H2还原NO生成N2和1mol水蒸气的能量变化示意图。由图可看出此反应为:

(2)升高温度绝大多数反应的化学反应速率增大,但是2NO(g)+O2(g)
 2NO2(g)的速率却随着温度的升高而减小。某化学小组为研究该特殊现象的实质原因,查阅资料知2NO(g)+O2(g)
2NO2(g)的速率却随着温度的升高而减小。某化学小组为研究该特殊现象的实质原因,查阅资料知2NO(g)+O2(g)  2NO2(g)的反应历程分两步:
2NO2(g)的反应历程分两步:Ⅰ.2NO(g)
 N2O2(g)(快) ΔH1 < 0 ;v1正=k1正·c2(NO);v1逆=k1逆·c(N2O2)
N2O2(g)(快) ΔH1 < 0 ;v1正=k1正·c2(NO);v1逆=k1逆·c(N2O2)Ⅱ.N2O2(g)+O2(g)
 2NO2(g)(慢) ΔH2 < 0 ;v2正=k2正·c(N2O2)·c(O2); v2逆=k2逆·c2(NO2)
2NO2(g)(慢) ΔH2 < 0 ;v2正=k2正·c(N2O2)·c(O2); v2逆=k2逆·c2(NO2)请回答下列问题:
① 一定温度下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,请写出此反应的平衡常数表达式K=
2NO2(g)达到平衡状态,请写出此反应的平衡常数表达式K=② 决定2NO(g)+O2(g)
 2NO2(g)反应速率的是反应Ⅱ,反应Ⅰ的活化能E1与反应Ⅱ的活化能E2的大小关系为E1
2NO2(g)反应速率的是反应Ⅱ,反应Ⅰ的活化能E1与反应Ⅱ的活化能E2的大小关系为E1A k2正增大,c(N2O2)增大 B k2正减小,c(N2O2)减小
C k2正增大,c(N2O2)减小 D k2正减小,c(N2O2)增大
③ 由实验数据得到v2正~c(O2)的关系可如图表示。当X点升高到某一温度时,反应重新达到平衡,则变为相应的点为

(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓,已知甲池中发生的反应为:


① 装置中H+从
您最近一年使用:0次
4 . 下列说法正确的是
②C(s,金刚石)+O2(g)=CO2 (g) △H="-" 395.0 kJ·mol-1,
则C(s,石墨)=C(s,金刚石)△H="+1.5" kJ.mol。1
②C(s,金刚石)+O2(g)=CO2 (g) △H="-" 395.0 kJ·mol-1,
则C(s,石墨)=C(s,金刚石)△H="+1.5" kJ.mol。1
| A.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 |
| B.同温同压下,H2 (g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H不同 |
| C.已知:①2H2(g) +O2(g) =2H2O(g) △H="-a" kJ·mol-1,②2H2(g)+O2 (g)= 2H2O(1)△H="-b" kJ·mol-1,则a>b |
| D.已知:①C(s,石墨)+O2 (g)=CO2(g)△H="-" 393.5kJ·mol-1, |
您最近一年使用:0次



