名校
1 . 二维锑片(Sb)是一种新型的CO2电化学还原催化剂。酸性条件下,人工固碳装置中的CO2气体在二维锑片表面发生三种催化竞争反应,其反应历程如下图所示(*表示吸附态中间体)。下列说法不正确 的是
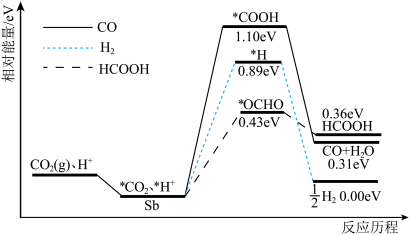

| A.三种催化竞争的总反应中,生成HCOOH吸收的能量最多 |
| B.在二维锑片表面生成CO的反应可表示为*CO2+*H++2e−=CO+H2O |
| C.使用二维锑片可以改变反应的路径 |
| D.生成各种不同的产物时,有极性键和非极性键形成 |
您最近一年使用:0次
名校
解题方法
2 . 先进的甲醇蒸气重整—变压吸附技术可得到高浓度CO2和H2混合气,化学反应原理是CH3OH+H2O CO2+3H2,其能量变化如图所示。下列说法错误的是
CO2+3H2,其能量变化如图所示。下列说法错误的是
 CO2+3H2,其能量变化如图所示。下列说法错误的是
CO2+3H2,其能量变化如图所示。下列说法错误的是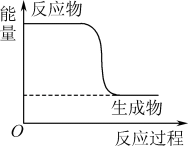
| A.CH3OH转变成H2的过程是一个吸收能量的过程 |
| B.反应物的总能量大于生成物的总能量 |
| C.形成H—H键放出能量 |
| D.断开H—C键吸收能量 |
您最近一年使用:0次
2024-01-24更新
|
153次组卷
|
2卷引用:江苏省南通市如皋中学2024届高三下学期第三次适应性考试化学试题
名校
3 . 一种由 和
和 转化为高附加值产品
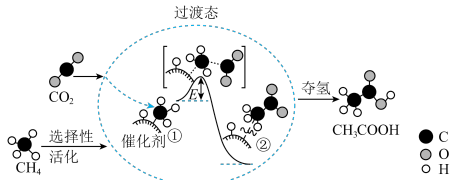
转化为高附加值产品 的催化反应历程如图所示。下列说法正确的是
的催化反应历程如图所示。下列说法正确的是
 和
和 转化为高附加值产品
转化为高附加值产品 的催化反应历程如图所示。下列说法正确的是
的催化反应历程如图所示。下列说法正确的是
| A.①→②放出能量并形成了C=C键 |
B.该反应的平衡常数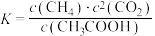 |
| C.该催化剂能提高反应物的平衡转化率 |
D.该反应中每生成1mol  转移电子的数目约为4×6.02×1023 转移电子的数目约为4×6.02×1023 |
您最近一年使用:0次
名校
4 . 将 嵌于聚苯胺表面制成催化剂(
嵌于聚苯胺表面制成催化剂( 为催化剂、聚苯胺为催化剂载体),碱性条件下,催化氧化含
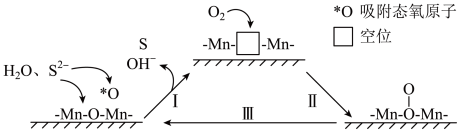
为催化剂、聚苯胺为催化剂载体),碱性条件下,催化氧化含 废水的机理如图所示。下列说法不正确的是
废水的机理如图所示。下列说法不正确的是
 嵌于聚苯胺表面制成催化剂(
嵌于聚苯胺表面制成催化剂( 为催化剂、聚苯胺为催化剂载体),碱性条件下,催化氧化含
为催化剂、聚苯胺为催化剂载体),碱性条件下,催化氧化含 废水的机理如图所示。下列说法不正确的是
废水的机理如图所示。下列说法不正确的是
| A.催化剂因S覆盖表面或进入空位而失活 |
B.该反应过程的总方程式为 |
| C.反应过程中锰元素化合价既有升高也有下降 |
D.反应Ⅲ的 |
您最近一年使用:0次
5 .  、
、 、
、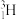 是氢元素的3种核素,基态H原子1s1的核外电子排布,使得H既可以形成H+又可以形成H-,还能形成H2O、H2O2、NH3、N2H4、CaH2等重要化合物;水煤气法、电解水、光催化分解水都能获得H2,如水煤气法制氢反应中,H2O(g)与足量C(s)反应生成1molH2(g)和1molCO(g)吸收131.3kJ的热量。H2在金属冶炼、新能源开发、碳中和等方面具有重要应用,如HCO
是氢元素的3种核素,基态H原子1s1的核外电子排布,使得H既可以形成H+又可以形成H-,还能形成H2O、H2O2、NH3、N2H4、CaH2等重要化合物;水煤气法、电解水、光催化分解水都能获得H2,如水煤气法制氢反应中,H2O(g)与足量C(s)反应生成1molH2(g)和1molCO(g)吸收131.3kJ的热量。H2在金属冶炼、新能源开发、碳中和等方面具有重要应用,如HCO 在催化剂作用下与H2反应可得到HCOO-。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
在催化剂作用下与H2反应可得到HCOO-。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
 、
、 、
、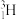 是氢元素的3种核素,基态H原子1s1的核外电子排布,使得H既可以形成H+又可以形成H-,还能形成H2O、H2O2、NH3、N2H4、CaH2等重要化合物;水煤气法、电解水、光催化分解水都能获得H2,如水煤气法制氢反应中,H2O(g)与足量C(s)反应生成1molH2(g)和1molCO(g)吸收131.3kJ的热量。H2在金属冶炼、新能源开发、碳中和等方面具有重要应用,如HCO
是氢元素的3种核素,基态H原子1s1的核外电子排布,使得H既可以形成H+又可以形成H-,还能形成H2O、H2O2、NH3、N2H4、CaH2等重要化合物;水煤气法、电解水、光催化分解水都能获得H2,如水煤气法制氢反应中,H2O(g)与足量C(s)反应生成1molH2(g)和1molCO(g)吸收131.3kJ的热量。H2在金属冶炼、新能源开发、碳中和等方面具有重要应用,如HCO 在催化剂作用下与H2反应可得到HCOO-。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是
在催化剂作用下与H2反应可得到HCOO-。我国科学家在氢气的制备和应用等方面都取得了重大成果。下列化学反应表示正确的是| A.C(s)+H2O(g)=H2(g)+CO(g)中,反应物的总键能小于生成物的总键能 |
B.HCO 催化加氢生成HCOO-的反应:HCO 催化加氢生成HCOO-的反应:HCO +H2 +H2 HCOO-+H2O HCOO-+H2O |
| C.电解水制氢的阳极反应:2H2O+2e-=H2↑+2OH- |
| D.CaH2与水反应:CaH2+2H2O=Ca(OH)2+H2↑ |
您最近一年使用:0次
2023-12-25更新
|
106次组卷
|
2卷引用:江苏省如皋中学2023-2024学年高三上学期阶段考试(二) 化学试题
6 . 已知: (1) 血红蛋白可与 O2结合,血红蛋白更易与CO配位,血红蛋白与O2配位示意如图所示。 (2) 血红蛋白(Hb)与O2 、CO结合的反应可表示为
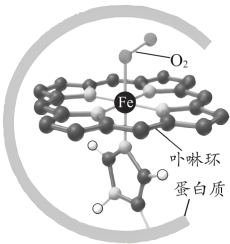
①Hb+O2⇌Hb(O2) K1;
②Hb+CO⇌Hb(CO) K2。
下列说法不正确的是

①Hb+O2⇌Hb(O2) K1;
②Hb+CO⇌Hb(CO) K2。
下列说法不正确的是
| A.相同温度下, K1>K2 |
| B.反应①②的ΔH均小于0 |
| C.CO中的C原子提供孤电子对与Fe2⁺配位 |
| D.用高压氧舱治疗CO中毒时,平衡②逆向移动 |
您最近一年使用:0次
解题方法
7 . 甲烷催化氧化为合成气的主要反应有:
I、
Ⅱ、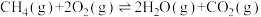
将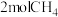 与
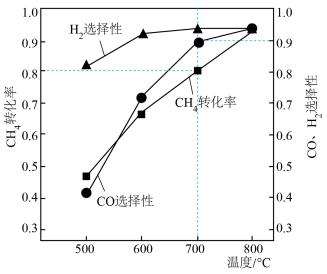
与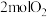 投入密闭容器中反应,不同温度下,相同时间内CH4转化率、H2选择性
投入密闭容器中反应,不同温度下,相同时间内CH4转化率、H2选择性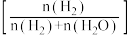 与CO的选择性
与CO的选择性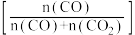 随温度的变化如图所示,下列说法正确的是
随温度的变化如图所示,下列说法正确的是
I、

Ⅱ、
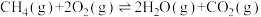
将
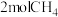 与
与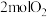 投入密闭容器中反应,不同温度下,相同时间内CH4转化率、H2选择性
投入密闭容器中反应,不同温度下,相同时间内CH4转化率、H2选择性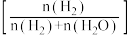 与CO的选择性
与CO的选择性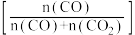 随温度的变化如图所示,下列说法正确的是
随温度的变化如图所示,下列说法正确的是
| A.由题可知,反应I为吸热反应 |
| B.在700℃时,容器中生成的CO2的物质的量为1.44mol |
C.在500℃、600℃、700℃时都可能发生 |
| D.该过程中,低温有利于合成气的生成 |
您最近一年使用:0次
2023-10-07更新
|
614次组卷
|
2卷引用:江苏省南通市海门区2023-2024学年高三上学期第一次调研考试化学试题
8 . 周期表中VIA族元素及其化合物应用广泛。 、
、 、
、 是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯
是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯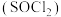 为黄色液体,其结构式为(
为黄色液体,其结构式为(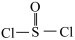 ),遇水发生水解。工业上可电解H2SO4与
),遇水发生水解。工业上可电解H2SO4与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵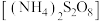 ,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
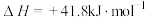 。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列有关
。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列有关
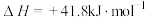 ,下列说法正确的
,下列说法正确的
 、
、 、
、 是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯
是氧元素的3种核素,可以形成多种重要的化合物。亚硫酰氯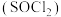 为黄色液体,其结构式为(
为黄色液体,其结构式为(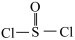 ),遇水发生水解。工业上可电解H2SO4与
),遇水发生水解。工业上可电解H2SO4与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵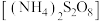 ,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
,过二硫酸铵与双氧水中都含有过氧键(-O-O-)。硝化法制硫酸的主要反应为:
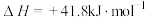 。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列有关
。SO2和SO3都是酸性氧化物,是制备硫酸的中间产物。下列有关
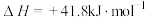 ,下列说法正确的
,下列说法正确的| A.该反应中反应物的总能量低于生成物的总能量 |
| B.反应达平衡后,分离出少量SO3,正反应速率加快 |
| C.其他条件不变,平衡后继续充入NO2,平衡常数将减小 |
| D.该反应中消耗22.4LNO2,转移电子的数目为2×6.02×1023 |
您最近一年使用:0次
解题方法
9 . 在Fe+催化作用下CO可将N2O转化为N2,反应的能量变化及反应历程如图所示:
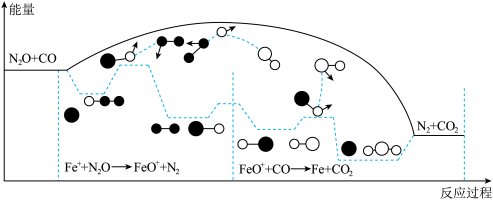
①N2O+Fe+=N2+FeO+(慢)②FeO++CO=CO2+Fe+(快)
下列叙述不 正确的是

①N2O+Fe+=N2+FeO+(慢)②FeO++CO=CO2+Fe+(快)
下列叙述
| A.反应①为放热反应 |
| B.FeO+为反应①的氧化产物,也是总反应的中间产物 |
| C.反应②的活化能Ea2比反应①的活化能Ea2要大 |
| D.每生成1molN2,转移电子数目为2×6.02×1023 |
您最近一年使用:0次
10 . 根据侯氏制碱原理(NaCl+NH3+H2O+CO2=NH4Cl+NaHCO3↓),某学习小组制备少量Na2CO3流程如图:

工业合成氨反应为:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ•mol-1。对于反应N2(g)+3H2(g)
2NH3(g) △H=-92.4kJ•mol-1。对于反应N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ•mol-1,下列说法正确的是
2NH3(g) △H=-92.4kJ•mol-1,下列说法正确的是

工业合成氨反应为:N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ•mol-1。对于反应N2(g)+3H2(g)
2NH3(g) △H=-92.4kJ•mol-1。对于反应N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ•mol-1,下列说法正确的是
2NH3(g) △H=-92.4kJ•mol-1,下列说法正确的是| A.该反应的△S>0 |
| B.1molN2与3molH2充分反应,放出92.4kJ的热量 |
| C.升高温度,该反应v(逆)增大,v(正)减小,平衡向逆反应方向移动 |
| D.断裂3molH-H键的同时,有6molH-N键断裂,说明该反应达到平衡状态 |
您最近一年使用:0次



