名校
解题方法
1 . 下列说法或表示方法正确的是( )
| A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B.由C(石墨)=C(金刚石)ΔH=+1.90kJ/mol可知,金刚石比石墨稳定 |
| C.在稀溶液中,H+(aq)+OH-(aq)=H2O(1)ΔH=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH溶液混合,放出的热量大于57.3kJ |
| D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)ΔH=-285.8kJ/mol |
您最近一年使用:0次
2020-10-26更新
|
278次组卷
|
20卷引用:2015-2016学年山西太原五中高二上第一周考理科化学试卷
2015-2016学年山西太原五中高二上第一周考理科化学试卷山西省朔州市怀仁一中2019-2020学年高二上学期第一次月考化学试卷2015-2016学年陕西西安第一中学高二上期中考试化学试卷2017届陕西省西安中学高三上学期月考二化学试卷重庆市第十八中学2016-2017学年高一下学期期中考试化学试题【全国校级联考】新疆伊宁生产建设兵团五校联考2017-2018学年高二下学期期末考试化学试题辽宁省阜新市海州高级中学2019届高三上学期第一次月考化学试题【全国百强校】江西省南昌市第二中学2018-2019学年高二上学期第一次月考化学试题(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点第2章《化学键 化学反应规律》单元测试——鲁科版(2019)必修第二册新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高一下学期期中考试化学试题黑龙江省哈尔滨师范大学青冈实验中学校2019届高三12月月考化学试题河北省保定市唐县第一中学2020-2021学年高二9月月考化学试题山东省惠民县第二中学致远部2020-2021学年高二上学期10月月考化学试题广东省广州市第一一三中学22020-2021学年高二上学期第一阶段考试化学(选考)试题湖南省中方一中2020-2021学年高二上学期期中考试化学试题福建省永安市第一中学2020-2021学年高二上学期期中考试化学试题广东省清远市凤霞中学2020-2021学年高二上学期期中考试化学(选科)试题辽宁省丹东市凤城市第一中学2021-2022学年高二上学期10月份月考化学试题辽宁省鞍山市第一中学2023-2024学年高一下学期第一次月考化学试卷
解题方法
2 . 下列说法正确的是
A.甲烷的标准燃烧热为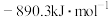 ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为: |
B.已知 ,则在一定条件下向密闭容器中充入 ,则在一定条件下向密闭容器中充入  和 和  充分反应后放出 充分反应后放出 的热量 的热量 |
C. 石墨转化为 石墨转化为 时,放出 时,放出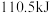 的热量 的热量 (石墨, (石墨, ) ) |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
您最近一年使用:0次
名校
3 . 实验测得H2和C3H8的标准燃烧热分别为285.8 kJ·mol-1和2220 kJ·mol-1,将 H2和C3H8的混合气体1mol完全燃烧生成CO2和液态水时放出1252.5kJ的热量,则混合气体中H2和C3H8的体积之比是
| A.2:1 | B.1:1 | C.1:2 | D.1:4 |
您最近一年使用:0次
2020-04-17更新
|
766次组卷
|
12卷引用:山西省运城市景胜中学2020-2021学年高二9月月考化学试题
山西省运城市景胜中学2020-2021学年高二9月月考化学试题【全国百强校】新疆维吾尔自治区生产建设兵团第一师高级中学2018-2019学年高二上学期第一次月考化学试题天津市静海区四校2019-2020学年高二上学期9月联考化学试题(已下线)【南昌新东方】2019 南大附中 高一下第三次月考黑龙江省七台河市第一中学2019-2020学年高一下学期期末考试化学试题(已下线)1.1.2 热化学方程式(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)1.2 燃烧热 能源(重点练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)(已下线)第一章 化学反应与能量(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版选修4)河南省长葛市第一高级中学2020-2021学年高一上学期阶段性测试试卷化学试题河南省安阳市第一中学2020-2021学年高二上学期第一次阶段考试化学试题四川省成都市金堂县竹篙中学2020-2021学年高二10月月考化学试题甘肃省靖远县第二中学2021-2022学年高二上学期期中考试(二)化学(理)试题
名校
解题方法
4 . 沼气是一种能源,它的主要成分是 ,
, 完全燃烧生成
完全燃烧生成 和液态水时放出445kJ的热最,则下列热化学方程式中正确的是
和液态水时放出445kJ的热最,则下列热化学方程式中正确的是
 ,
, 完全燃烧生成
完全燃烧生成 和液态水时放出445kJ的热最,则下列热化学方程式中正确的是
和液态水时放出445kJ的热最,则下列热化学方程式中正确的是A.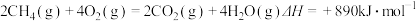 |
B. |
C.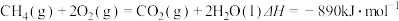 |
D.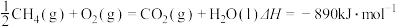 |
您最近一年使用:0次
2020-02-17更新
|
233次组卷
|
19卷引用:山西省应县第一中学校2019-2020学年高二上学期期中考试化学试题
山西省应县第一中学校2019-2020学年高二上学期期中考试化学试题(已下线)2011-2012学年浙江省东阳市南马高中高一下学期期中考试化学试卷(已下线)2011-2012学年浙江省杭州市西湖高级中学高一5月月考化学试卷(已下线)2012-2013学年广东省揭阳一中高二第一阶段考试化学试卷(已下线)2012-2013学年广东陆丰碣石中学高二第二次月考化学试卷(已下线)2013-2014学年江苏省淮安市高中协作体高二下学期期中考试化学试卷2016-2017学年山东省桓台二中高二12月检测化学试卷辽宁省辽源市金鼎高级中学2016-2017学年高二上学期期末考试化学试卷内蒙古翁牛特旗乌丹第二中学2017-2018学年高二上学期期中考试化学试题【校级联考】浙江省台州市联谊五校2018-2019学年高一下学期期中考试化学试题新疆疏勒县八一中学2018-2019学年高二上学期期末化学试题广东省深圳科学高中2019-2020学年高二上学期开学考试化学试题吉林省长春外国语学校2019-2020学年高二上学期第一次月考化学试题宁夏青铜峡市高级中学(吴忠中学分校)2019-2020学年高二上学期第一次月考化学试题海南省临高县临高中学2019-2020学年高二上学期期中考试化学试题(已下线)【新东方】高中化学5029甘肃省古浪县第二中学2019-2020学年高二12月基础知识竞赛化学试题2020届高三化学知识点强化训练—化学能与热能河北省唐山市海港高级中学2019-2020学年高一下学期期中考试化学试题
5 . 甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
(1)甲醇蒸汽完全燃烧的热化学方程式为_____________ 。
(2)反应②中的能量变化如下图所示,则△H2=______ (用E1和E2表示)。

(3)H2(g)的燃烧热为__________ kJ· mol-1。
(4)请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:__________________ (写出一点)
①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1(1)甲醇蒸汽完全燃烧的热化学方程式为
(2)反应②中的能量变化如下图所示,则△H2=

(3)H2(g)的燃烧热为
(4)请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:
您最近一年使用:0次
2020-01-12更新
|
182次组卷
|
8卷引用:2014-2015山西省原平市一中高二上学期期末考试化学试卷
解题方法
6 . “二青会”火炬塔中使用的燃料是天然气,主要成分是甲烷,作为一种洁净环保的优质能源,几乎不含硫、粉尘和其他有害物质。
(1)已知:CH4的燃烧热为ΔH=-890kJ•mol-1,CO的燃烧热为ΔH=-283kJ•mol-1
①深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。常温常压下,甲烷细菌使1mol甲烷生成CO2气体和液态水,放出的能量___ (填“<”“>”或“=”)890kJ。
②写出1molCH4(g)不完全燃烧生成CO(g)和H2O(l)的热化学方程式___ 。
(2)甲烷与CO2可用于制备合成气(主要成分是一氧化碳和氢气):CH4(g)+CO2(g)=2CO(g)+2H2(g),1gCH4(g)参加以上反应可释放15.46kJ的热量,则如图中能表示该反应过程中能量变化的是___ (填字母)。

(3)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0
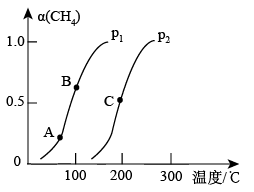
①在一定条件下,CH4的平衡转化率与温度、压强的关系如图所示。则p1___ p2(填“<”“>”或“=”);A、B、C三点处对应的平衡常数(KA、KB、KC)由大到小的顺序为___ 。
②在恒温恒压的密闭容器中,下列各项能作为判断该反应达到化学平衡状态依据的是___ (填字母)。
a.v(CH4)=v(CO)
b.混合气体的密度不发生变化
c.容器内混合气体的总压强不发生变化
d.一段时间内,用CH4表示的平均反应速率等于零
③将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4的转化率为50%,则反应前与平衡后,混合气体的平均相对分子质量之比为___ 。
(4)甲烷可以合成甲醇来代替日益供应紧张的燃油。工业上用甲烷为原料制备甲醇分为两个阶段:
①制备合成气:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。
②合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)。实验室在恒温(500℃)、恒容(1L)密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,10min、40min、50min时分别测得容器中甲醇的浓度为0.60mol•L-1、0.80mol•L-1、0.80mol•L-1。则此条件下该反应开始10min内,H2的平均反应速率为__ ;平衡常数K的数值为___ 。
(1)已知:CH4的燃烧热为ΔH=-890kJ•mol-1,CO的燃烧热为ΔH=-283kJ•mol-1
①深海中存在一种甲烷细菌,它们依靠酶使甲烷与O2作用产生的能量存活。常温常压下,甲烷细菌使1mol甲烷生成CO2气体和液态水,放出的能量
②写出1molCH4(g)不完全燃烧生成CO(g)和H2O(l)的热化学方程式
(2)甲烷与CO2可用于制备合成气(主要成分是一氧化碳和氢气):CH4(g)+CO2(g)=2CO(g)+2H2(g),1gCH4(g)参加以上反应可释放15.46kJ的热量,则如图中能表示该反应过程中能量变化的是

(3)甲烷转化为CO和H2的反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0
①在一定条件下,CH4的平衡转化率与温度、压强的关系如图所示。则p1

②在恒温恒压的密闭容器中,下列各项能作为判断该反应达到化学平衡状态依据的是
a.v(CH4)=v(CO)
b.混合气体的密度不发生变化
c.容器内混合气体的总压强不发生变化
d.一段时间内,用CH4表示的平均反应速率等于零
③将CH4和H2O(g)按等物质的量混合,一定条件下反应达到平衡,CH4的转化率为50%,则反应前与平衡后,混合气体的平均相对分子质量之比为
(4)甲烷可以合成甲醇来代替日益供应紧张的燃油。工业上用甲烷为原料制备甲醇分为两个阶段:
①制备合成气:CH4(g)+H2O(g)⇌CO(g)+3H2(g)。
②合成甲醇:CO(g)+2H2(g)⇌CH3OH(g)。实验室在恒温(500℃)、恒容(1L)密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,10min、40min、50min时分别测得容器中甲醇的浓度为0.60mol•L-1、0.80mol•L-1、0.80mol•L-1。则此条件下该反应开始10min内,H2的平均反应速率为
您最近一年使用:0次
7 . 已知丙烷的燃烧热△H=-2215kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8g水,则放出的热量约为
| A.55 kJ | B.220 kJ | C.550 kJ | D.1108 kJ |
您最近一年使用:0次
2019-01-30更新
|
2546次组卷
|
42卷引用:2017届山西省重点中学协作体高三暑假第一次联考化学试卷
2017届山西省重点中学协作体高三暑假第一次联考化学试卷2015年全国普通高等学校招生统一考试理科综合能力测试化学(海南卷)2015-2016学年江苏省泰州市姜堰区高二上学期期中选修化学试卷2015-2016学年浙江省东阳中学高二上学期12月阶段测化学试卷2015-2016学年浙江省湖州中学高二上学期期中化学试卷2015-2016学年海南文昌中学高一下期末考化学(理)试题2017届陕西省西安中学高三上学期月考二化学试卷2015-2016学年青海省西宁市第五中学高一下学期期末(理)化学试卷河南省郸城县第一高级中学2017-2018学年高二11月月考化学试题【全国百强校】黑龙江省双鸭山市第一中学2017-2018学年高一下学期期末考试化学试题甘肃省岷县二中2018-2019学年高二上学期第一次月考化学试题【全国百强校】河北省武邑中学2018-2019学年高二上学期第二次月考化学试题甘肃省岷县第二中学2018-2019学年高二上学期期中考试化学试题高二人教版选修4 第一章 章末知识测评(一)(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)云南省腾冲市第八中学2018-2019学年高二下学期期中考试化学试题河北安平中学2018-2019学年高二下学期期末考试化学试题(已下线)2019年9月1日《每日一题》人教选修4—— 每周一测安徽省青阳县第一中学2019-2020学年高二9月月考化学试题福建省莆田九中2019-2020学年高二上学期期中考试化学试题2020年春季人教版高中化学选修4第一章《化学反应与能量》测试卷(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训河北省石家庄市第二中学2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分陕西省延安市吴起高级中学2019-2020学年高一下学期第四次质量检测(期末)化学试题(已下线)第01章 化学反应与能量(B卷提升篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)福建省福州市罗源第一中学2020-2021学年高二上学期10月月考化学试题黑龙江省哈尔滨市第六中学2020-2021学年高二10月月考化学试题甘肃省武威市民勤县第一中学2020-2021学年高二上学期12月月考化学试题(理科)(已下线)1.2 反应热的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)浙江省丽水外国语学校高中部2021-2022学年高二上学期第一次月考(10月)化学试题河北省盐山中学2021-2022学年高二上学期9月月考化学试题黑龙江省哈尔滨市第六中学校2021-2022学年高二上学期10月阶段性总结化学试题吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题安徽省六安市新安中学2021-2022学年高二上学期期中考试化学试题(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)云南省文山州第一中学2021-2022学年高二下学期3月份考试化学试题第二节 反应热的计算 第2课时 反应热的计算(已下线)第15讲 化学反应的热效应 (练)-2023年高考化学一轮复习讲练测(新教材新高考)广东省广州大学附属中学2022-2023学年高二上学期期中考试化学试题上海市华东政法大学附属中学2022-2023学年高二下学期期中考试(等级考)化学试题第3课时 反应焓变的计算
8 . 氢气是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为________________
②该反应的热化学方程式为_____________________
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:Mg(s)+H2(g)=MgH2(s)ΔH1=-74.5kJ·mol-1,Mg2Ni(s)+2H2(g)=Mg2NiH4(s)ΔH2,Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1,则ΔH2=____________ kJ·mol-1。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为
②该反应的热化学方程式为
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:Mg(s)+H2(g)=MgH2(s)ΔH1=-74.5kJ·mol-1,Mg2Ni(s)+2H2(g)=Mg2NiH4(s)ΔH2,Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1,则ΔH2=
您最近一年使用:0次
2018-10-02更新
|
274次组卷
|
4卷引用:山西省运城市稷山中学2019-2020学年高二上学期第一次月考化学试题
名校
9 . 氢气在氧气中燃烧产生淡蓝色火焰,在反应中,破坏1 mol H—H键消耗的能量为Q1 kJ,破坏1 mol O===O键消耗的能量为Q2 kJ,形成1 mol H—O键释放的能量为Q3 kJ。下列关系式中正确的是( )
| A.2Q1+Q2<4Q3 | B.2Q1+Q2>4Q3 | C.2Q1+Q2<2Q3 | D.2Q1+Q2>2Q3 |
您最近一年使用:0次
2018-04-19更新
|
631次组卷
|
6卷引用:山西省祁县中学2017-2018学年高一下学期第一次月考化学试题
山西省祁县中学2017-2018学年高一下学期第一次月考化学试题(已下线)2019年3月11日 《每日一题》 必修2 化学键与化学反应中能量变化的关系贵州省遵义市2021 2022学年高二上学期第一次月考化学试题黑龙江省双鸭山市第一中学2022-2023学年高一下学期期中考试化学试题山东省泰安市2022-2023学年高一下学期期末统考化学试题山东省威海市乳山市银滩高级中学2023-2024学年高一下学期3月月考化学试题
11-12高二上·山西太原·期中
名校
10 . 已知:2H2(g)+O2(g)=2 H2O(l) △H= -571.6 kJ·mol-1
H2(g)+1/2O2(g)=H2O(g) ΔH= -241.8 kJ/mol
C3H4(g)+4O2(g) = 3CO2(g) +2H2O(g) △H= -2100.0 kJ·mol-1
根据上面两个热化学方程式回答下列问题:
(1) H2的燃烧热为________________ ;
(2)1mol H2和2mol C3H4 组成的混合气体完全燃烧生成液态水时释放的热量为___ ;
(3)现有H2和C3H4的混合气体共5mol,完全燃烧生成CO2和气态水时,则放出热量(Q)的取值范围是____ ;若生成CO2和H2O的物质的量相等,则放出的热量是_____ 。
H2(g)+1/2O2(g)=H2O(g) ΔH= -241.8 kJ/mol
C3H4(g)+4O2(g) = 3CO2(g) +2H2O(g) △H= -2100.0 kJ·mol-1
根据上面两个热化学方程式回答下列问题:
(1) H2的燃烧热为
(2)1mol H2和2mol C3H4 组成的混合气体完全燃烧生成液态水时释放的热量为
(3)现有H2和C3H4的混合气体共5mol,完全燃烧生成CO2和气态水时,则放出热量(Q)的取值范围是
您最近一年使用:0次



