名校
1 . 硫磺(主要成份:S)和黄铁矿(主要成份: )均是工业制取硫酸的主要原料。
)均是工业制取硫酸的主要原料。
Ⅰ.已知:①单质硫的燃烧热为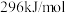
②

(1)写出由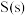 生成
生成 的热化学反应方程式
的热化学反应方程式_______
Ⅱ.黄铁矿因其浅黄铜色和明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。某兴趣小组设计如下实验方案,测定某高纯黄铁矿石中硫元素的含量。
称取 该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
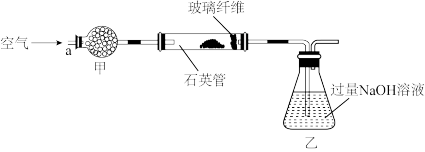
(2)写出石英管中发生反应的化学方程式:_______ 。
(3)上图中,干燥管甲内所盛试剂是_______ 。
(4)有同学提出该实验装置存在安全 隐患,请用简洁的文字说明:_______ 。
反应结束后,将乙瓶中的溶液进行如下处理:
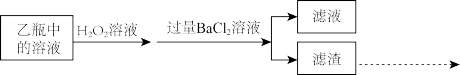
(5)为准确 测定该黄铁矿石中硫元素的质量分数,请将上述步骤补充完整_______ 。
(6)某同学设计如下实验,探究反应后乙瓶中溶液所含的阴离子种类 ,请完成下列表格
 )均是工业制取硫酸的主要原料。
)均是工业制取硫酸的主要原料。Ⅰ.已知:①单质硫的燃烧热为
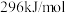
②


(1)写出由
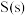 生成
生成 的热化学反应方程式
的热化学反应方程式Ⅱ.黄铁矿因其浅黄铜色和明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。某兴趣小组设计如下实验方案,测定某高纯黄铁矿石中硫元素的含量。
称取
 该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
该黄铁矿样品放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全得到红棕色固体和一种刺激性气味的气体。
(2)写出石英管中发生反应的化学方程式:
(3)上图中,干燥管甲内所盛试剂是
(4)有同学提出该实验装置存在
反应结束后,将乙瓶中的溶液进行如下处理:
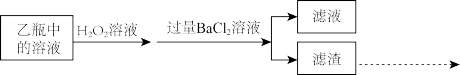
(5)为
(6)某同学设计如下实验,探究反应后乙瓶中溶液所含的
| 步骤 | 实验操作 | 现象及结论 |
| a | 取适量锥形瓶乙中反应后的溶液,滴加足量稀盐酸至不再有气泡产生,将所产生的气体通入到足量 | 红色褪去,说明有 |
| b | 取步骤a所得溶液,滴加 | 有白色沉淀产生,说明有 |
| c | 另取适量锥形瓶乙中反应后的溶液, | 溶液变红,说明有 |
您最近一年使用:0次
2 . 由硫铁矿“烧渣”(主要成分: 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图: (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。
(1)①中加入的酸为___________ 。①中 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为___________ 。
(2)关于制备流程中含铁微粒的描述,错误的是___________。
(3)反应②需在高温高压下进行,且随着反应温度的升高,硫铁矿烧渣酸浸液中 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式___________ 。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、___________ 过滤、洗涤、干燥。
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀 酸化,用
酸化,用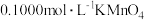 溶液滴定,消耗
溶液滴定,消耗 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为___________ %(保留一位小数)。
(6)长期放置的 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾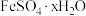 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入___________ ,其原因是___________ (用离子方程式表示)。
(7) 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知
在空气中加热反应可制得铁系氧化物材料。已知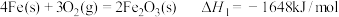
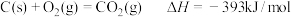

则:4FeCO3(s)+O2(g) 2Fe2O3(s)+4CO2(g) ΔH=
2Fe2O3(s)+4CO2(g) ΔH=___________ 。
(8)用一氧化碳还原氮氧化物,可防止氮氧化物污染。已知:
①2C(s)+O2(g)=2CO(g) ΔH1=-221kJ•mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+181kJ•mol-1
③2CO(g)+2NO(g)=2CO2(g)+N2(g) ΔH3=-747kJ•mol-1
则C(s)的燃烧热为___________ 。
 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图: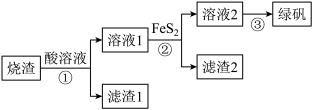
 (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。(1)①中加入的酸为
 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为(2)关于制备流程中含铁微粒的描述,错误的是___________。
A.步骤①,硫酸酸溶后溶液中主要有 、 、 等正离子 等正离子 |
B.步骤①后可依次用KSCN溶液和酸性 溶液来检测溶液中铁元素的价态 溶液来检测溶液中铁元素的价态 |
| C.Fe元素位于周期表的第ⅥB族 |
D.步骤②中加入硫铁矿的目的是将 还原为 还原为 |
(3)反应②需在高温高压下进行,且随着反应温度的升高,硫铁矿烧渣酸浸液中
 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式(4)通过③得到绿矾晶体的实验操作:加热浓缩、
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀
 酸化,用
酸化,用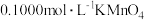 溶液滴定,消耗
溶液滴定,消耗 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为(6)长期放置的
 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾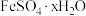 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入(7)
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知
在空气中加热反应可制得铁系氧化物材料。已知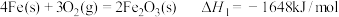
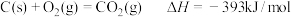

则:4FeCO3(s)+O2(g)
 2Fe2O3(s)+4CO2(g) ΔH=
2Fe2O3(s)+4CO2(g) ΔH=(8)用一氧化碳还原氮氧化物,可防止氮氧化物污染。已知:
①2C(s)+O2(g)=2CO(g) ΔH1=-221kJ•mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+181kJ•mol-1
③2CO(g)+2NO(g)=2CO2(g)+N2(g) ΔH3=-747kJ•mol-1
则C(s)的燃烧热为
您最近一年使用:0次
名校
解题方法
3 . 由硫铁矿“烧渣”(主要成分: 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图:

已知: (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。
(1)①中加入的酸为___________ 。①中 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为___________ 。
(2)关于制备流程中含铁微粒的描述,错误的是___________。
(3)反应②需在高温高压下进行,且随着反应温度的升高,硫铁矿烧渣酸浸液中 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式___________ 。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、___________ 过滤、洗涤、干燥。
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀 酸化,用
酸化,用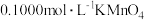 溶液滴定至终点。滴定终点的现象是
溶液滴定至终点。滴定终点的现象是___________ ,滴定至终点时,消耗 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为___________ %(保留一位小数)。
(6)长期放置的 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入___________ ,其原因是___________ (用离子方程式表示)。
(7) 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时:
在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时:
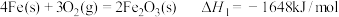
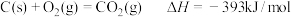

 在空气中加热反应生成
在空气中加热反应生成 的热化学方程式是
的热化学方程式是___________ 。
(8) 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾( ),氧化性比
),氧化性比 、
、 、
、 、
、 更强,制备反应的第一步是:
更强,制备反应的第一步是: 。
。
①上述反应中作还原剂的是___________ (填化学式)。
②简要说明 作为水处理剂时所起的作用
作为水处理剂时所起的作用___________ 。
 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图:
已知:
 (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。(1)①中加入的酸为
 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为(2)关于制备流程中含铁微粒的描述,错误的是___________。
A.步骤①,硫酸酸溶后溶液中主要有 、 、 等正离子 等正离子 |
B.步骤①后可依次用KSCN溶液和酸性 溶液来检测溶液中铁元素的价态 溶液来检测溶液中铁元素的价态 |
| C.Fe元素位于周期表的第VIB族 |
D.步骤②中加入硫铁矿的目的是将 还原为 还原为 |
 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式(4)通过③得到绿矾晶体的实验操作:加热浓缩、
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀
 酸化,用
酸化,用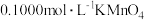 溶液滴定至终点。滴定终点的现象是
溶液滴定至终点。滴定终点的现象是 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为(6)长期放置的
 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入(7)
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时:
在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时: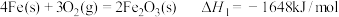
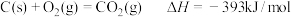

 在空气中加热反应生成
在空气中加热反应生成 的热化学方程式是
的热化学方程式是(8)
 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾( ),氧化性比
),氧化性比 、
、 、
、 、
、 更强,制备反应的第一步是:
更强,制备反应的第一步是: 。
。①上述反应中作还原剂的是
②简要说明
 作为水处理剂时所起的作用
作为水处理剂时所起的作用
您最近一年使用:0次



