由硫铁矿“烧渣”(主要成分: 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图:

已知: (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。
(1)①中加入的酸为___________ 。①中 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为___________ 。
(2)关于制备流程中含铁微粒的描述,错误的是___________。
(3)反应②需在高温高压下进行,且随着反应温度的升高,硫铁矿烧渣酸浸液中 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式___________ 。
(4)通过③得到绿矾晶体的实验操作:加热浓缩、___________ 过滤、洗涤、干燥。
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀 酸化,用
酸化,用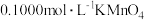 溶液滴定至终点。滴定终点的现象是
溶液滴定至终点。滴定终点的现象是___________ ,滴定至终点时,消耗 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为___________ %(保留一位小数)。
(6)长期放置的 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入___________ ,其原因是___________ (用离子方程式表示)。
(7) 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时:
在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时:
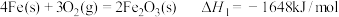
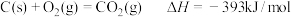

 在空气中加热反应生成
在空气中加热反应生成 的热化学方程式是
的热化学方程式是___________ 。
(8) 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾( ),氧化性比
),氧化性比 、
、 、
、 、
、 更强,制备反应的第一步是:
更强,制备反应的第一步是: 。
。
①上述反应中作还原剂的是___________ (填化学式)。
②简要说明 作为水处理剂时所起的作用
作为水处理剂时所起的作用___________ 。
 、
、 和FeO)制备绿矾(
和FeO)制备绿矾( ))的流程如图:
))的流程如图:
已知:
 (S的化合价为-1)难溶于水。
(S的化合价为-1)难溶于水。(1)①中加入的酸为
 (烧渣的主要成分之一)与酸反应的离子方程式为
(烧渣的主要成分之一)与酸反应的离子方程式为(2)关于制备流程中含铁微粒的描述,错误的是___________。
A.步骤①,硫酸酸溶后溶液中主要有 、 、 等正离子 等正离子 |
B.步骤①后可依次用KSCN溶液和酸性 溶液来检测溶液中铁元素的价态 溶液来检测溶液中铁元素的价态 |
| C.Fe元素位于周期表的第VIB族 |
D.步骤②中加入硫铁矿的目的是将 还原为 还原为 |
 的还原率增加。已知滤渣2的成分中仅有
的还原率增加。已知滤渣2的成分中仅有 ,请你写出反应②的离子方程式
,请你写出反应②的离子方程式(4)通过③得到绿矾晶体的实验操作:加热浓缩、
(5)绿矾纯度测定:称量2.920g样品于锥形瓶中,溶解后加稀
 酸化,用
酸化,用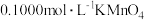 溶液滴定至终点。滴定终点的现象是
溶液滴定至终点。滴定终点的现象是 溶液20.00mL。该样品的纯度为
溶液20.00mL。该样品的纯度为(6)长期放置的
 溶液易被氧化而变质,实验室用绿矾
溶液易被氧化而变质,实验室用绿矾 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入(7)
 可转化为
可转化为 ,
, 在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时:
在空气中加热反应可制得铁系氧化物材料。已知25℃,100kPa时: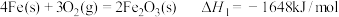
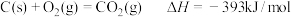

 在空气中加热反应生成
在空气中加热反应生成 的热化学方程式是
的热化学方程式是(8)
 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾(
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钾( ),氧化性比
),氧化性比 、
、 、
、 、
、 更强,制备反应的第一步是:
更强,制备反应的第一步是: 。
。①上述反应中作还原剂的是
②简要说明
 作为水处理剂时所起的作用
作为水处理剂时所起的作用
更新时间:2023-03-29 22:52:48
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】Ⅰ.甲醇燃料电池被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH3OH液体完全燃烧生成CO2和液态水时放出热量726.51 kJ,则表示甲醇燃烧的热化学方程式为_______________________________ 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+49.0 kJ·mol-1 ②CH3OH(g)+ O2(g)= CO2(g)+2H2(g) △H2
O2(g)= CO2(g)+2H2(g) △H2
已知H2(g)+ O2(g)===H2O(g) △H = —241.8kJ·mol-1,则反应②的△H2=
O2(g)===H2O(g) △H = —241.8kJ·mol-1,则反应②的△H2=_____________ 。
(3)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)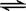 CH3OH(g),现在实验室模拟该反应并进行分析。下图是该反应在不同温度下CO的转化率随时间变化的曲线如右图。
CH3OH(g),现在实验室模拟该反应并进行分析。下图是该反应在不同温度下CO的转化率随时间变化的曲线如右图。
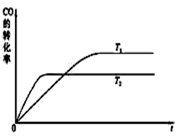
①该反应的焓变ΔH______ 0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1_______ K2(填“>”、“<”或“=”)。
(4)H2 和CO合成甲醇反应为:CO(g)+2H2(g) CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为
CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为_______ ;10min内用H2表示的化学反应速率为_______ ;若要加快CH3OH的生成速率并提高CO的转化率,可采取的措施有________________ (填一种合理的措施)。
(5) 二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为: CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H 。
CH3OH(g) +H2O(g) △H 。
①该反应的平衡常数表达式为K=___________ 。
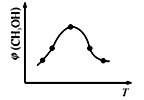
②在恒容密闭容器中使CO2和H2(物质的量之比为1∶3)发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如下图所示,则△H_________ 0(填“大于”或“小于”)
(1)101 kPa时,1 mol CH3OH液体完全燃烧生成CO2和液态水时放出热量726.51 kJ,则表示甲醇燃烧的热化学方程式为
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=+49.0 kJ·mol-1 ②CH3OH(g)+
 O2(g)= CO2(g)+2H2(g) △H2
O2(g)= CO2(g)+2H2(g) △H2已知H2(g)+
 O2(g)===H2O(g) △H = —241.8kJ·mol-1,则反应②的△H2=
O2(g)===H2O(g) △H = —241.8kJ·mol-1,则反应②的△H2=(3)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)
 CH3OH(g),现在实验室模拟该反应并进行分析。下图是该反应在不同温度下CO的转化率随时间变化的曲线如右图。
CH3OH(g),现在实验室模拟该反应并进行分析。下图是该反应在不同温度下CO的转化率随时间变化的曲线如右图。
①该反应的焓变ΔH
②T1和T2温度下的平衡常数大小关系是K1
(4)H2 和CO合成甲醇反应为:CO(g)+2H2(g)
 CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为
CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为(5) 二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为: CO2(g) +3H2(g)
 CH3OH(g) +H2O(g) △H 。
CH3OH(g) +H2O(g) △H 。①该反应的平衡常数表达式为K=
②在恒容密闭容器中使CO2和H2(物质的量之比为1∶3)发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如下图所示,则△H

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】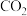 和
和 是两种重要的温室气体,通过
是两种重要的温室气体,通过 和
和 反应制造更高价值化学品是目前的研究目标。
反应制造更高价值化学品是目前的研究目标。
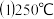 时,以镍合金为催化剂,向
时,以镍合金为催化剂,向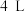 容器中通入
容器中通入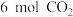 、
、 ,发生如下反应:
,发生如下反应: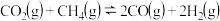 。平衡体系中各组分体积分数如下表:
。平衡体系中各组分体积分数如下表:
 此温度下该反应的平衡常数
此温度下该反应的平衡常数
__________
 已知:
已知: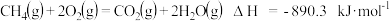
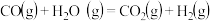
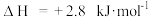
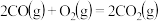
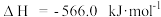
反应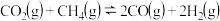 的
的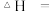
_____________ 
 以二氧化钛表面覆盖
以二氧化钛表面覆盖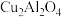 为催化剂,可以将
为催化剂,可以将 和
和 直接转化成乙酸。
直接转化成乙酸。
 在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。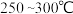 时,温度升高而乙酸的生成速率降低的原因是
时,温度升高而乙酸的生成速率降低的原因是___________ 。

 为了提高该反应中
为了提高该反应中 的转化率,可以采取的措施是
的转化率,可以采取的措施是_________ 。
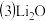 、
、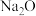 、MgO均能吸收
、MgO均能吸收 ;
;
 如果寻找吸收
如果寻找吸收 的其他物质,下列建议不合理的是
的其他物质,下列建议不合理的是______
 可在具有强氧化性的物质中寻找
可在具有强氧化性的物质中寻找
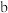 可在碱性氧化物中寻找
可在碱性氧化物中寻找
 可在ⅠA、ⅡA族元素形成的氧化物中寻找
可在ⅠA、ⅡA族元素形成的氧化物中寻找
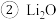 吸收
吸收 后,产物用于合成
后,产物用于合成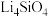 ,
,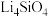 用于吸收、释放
用于吸收、释放 ,原理是:在
,原理是:在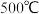 ,
, 与
与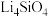 接触后生成
接触后生成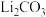 ;平衡后加热至
;平衡后加热至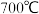 ,反应逆向进行,放出
,反应逆向进行,放出 ,
,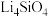 再生,说明该原理的化学方程式是
再生,说明该原理的化学方程式是_____________ 。
 高温电解技术能高效实现下列反应:
高温电解技术能高效实现下列反应: ,其可将释放的
,其可将释放的 转化为具有工业利用价值的产品。工作原理示意图如下:
转化为具有工业利用价值的产品。工作原理示意图如下:
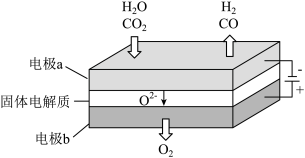
 在电极a放电的电极反应式是
在电极a放电的电极反应式是____________ 。
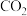 和
和 是两种重要的温室气体,通过
是两种重要的温室气体,通过 和
和 反应制造更高价值化学品是目前的研究目标。
反应制造更高价值化学品是目前的研究目标。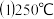 时,以镍合金为催化剂,向
时,以镍合金为催化剂,向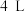 容器中通入
容器中通入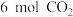 、
、 ,发生如下反应:
,发生如下反应: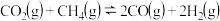 。平衡体系中各组分体积分数如下表:
。平衡体系中各组分体积分数如下表:| 物质 |  |  | CO |  |
| 体积分数 | 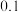 | 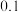 | 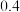 |  |
 此温度下该反应的平衡常数
此温度下该反应的平衡常数
 已知:
已知: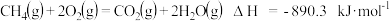
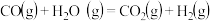
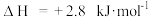
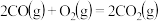
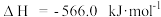
反应
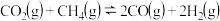 的
的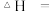

 以二氧化钛表面覆盖
以二氧化钛表面覆盖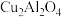 为催化剂,可以将
为催化剂,可以将 和
和 直接转化成乙酸。
直接转化成乙酸。 在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。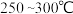 时,温度升高而乙酸的生成速率降低的原因是
时,温度升高而乙酸的生成速率降低的原因是
 为了提高该反应中
为了提高该反应中 的转化率,可以采取的措施是
的转化率,可以采取的措施是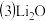 、
、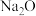 、MgO均能吸收
、MgO均能吸收 ;
; 如果寻找吸收
如果寻找吸收 的其他物质,下列建议不合理的是
的其他物质,下列建议不合理的是 可在具有强氧化性的物质中寻找
可在具有强氧化性的物质中寻找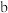 可在碱性氧化物中寻找
可在碱性氧化物中寻找 可在ⅠA、ⅡA族元素形成的氧化物中寻找
可在ⅠA、ⅡA族元素形成的氧化物中寻找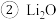 吸收
吸收 后,产物用于合成
后,产物用于合成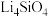 ,
,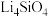 用于吸收、释放
用于吸收、释放 ,原理是:在
,原理是:在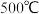 ,
, 与
与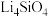 接触后生成
接触后生成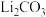 ;平衡后加热至
;平衡后加热至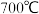 ,反应逆向进行,放出
,反应逆向进行,放出 ,
,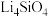 再生,说明该原理的化学方程式是
再生,说明该原理的化学方程式是 高温电解技术能高效实现下列反应:
高温电解技术能高效实现下列反应: ,其可将释放的
,其可将释放的 转化为具有工业利用价值的产品。工作原理示意图如下:
转化为具有工业利用价值的产品。工作原理示意图如下:
 在电极a放电的电极反应式是
在电极a放电的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】工业合成尿素 以
以 和
和 为原料,在合成塔中存在如图转化:
为原料,在合成塔中存在如图转化:

(1)液相中,合成尿素总反应的热化学反应方程式为_______ 。
(2)一定条件下, 的平衡转化率与温度、初始氨碳比
的平衡转化率与温度、初始氨碳比 、水碳比
、水碳比 的关系如图2和图3所示,回答下列问题:
的关系如图2和图3所示,回答下列问题:

下列说法不正确的是_______(填标号)。
(3)氮及其化合物在工农业生产、生活中有着重要作用。合成氨工业中:
 ,其化学平衡常数K与温度t的关系如表:
,其化学平衡常数K与温度t的关系如表:
完成下列填空:
①试比较 、
、 的大小,
的大小,
_______  (填写“>”“=”或“<”)。
(填写“>”“=”或“<”)。
②将 和
和 投到一个温度恒定、体积恒定的容器中进行上述反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是
投到一个温度恒定、体积恒定的容器中进行上述反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是_______ (填标号)。
A.
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
③某合成氨速率方程为 ,其中k为速率常数,根据表中数据,
,其中k为速率常数,根据表中数据,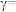
_______ 。
在合成氨过程中,需要不断分离出氨的原因为_______ (填标号)。
A.有利于平衡正向移动 B.提高正反应速率 C.防止催化剂中毒
 以
以 和
和 为原料,在合成塔中存在如图转化:
为原料,在合成塔中存在如图转化:
(1)液相中,合成尿素总反应的热化学反应方程式为
(2)一定条件下,
 的平衡转化率与温度、初始氨碳比
的平衡转化率与温度、初始氨碳比 、水碳比
、水碳比 的关系如图2和图3所示,回答下列问题:
的关系如图2和图3所示,回答下列问题:
下列说法不正确的是_______(填标号)。
A.图2两曲线中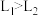 |
| B.增大氨碳比有利于提高尿素产率,过量氨气能与水蒸气作用促进第二步反应正移 |
C.图3曲线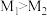 ,增大水碳比有利于尿素生成 ,增大水碳比有利于尿素生成 |
D.实际工业生产时,可选用初始条件为氨碳比 和水碳比 和水碳比 |

 ,其化学平衡常数K与温度t的关系如表:
,其化学平衡常数K与温度t的关系如表:| t/℃ | 200 | 300 | 400 |
| K |  |  | 0.5 |
①试比较
 、
、 的大小,
的大小,
 (填写“>”“=”或“<”)。
(填写“>”“=”或“<”)。②将
 和
和 投到一个温度恒定、体积恒定的容器中进行上述反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是
投到一个温度恒定、体积恒定的容器中进行上述反应,一段时间后可判断该可逆反应达到化学平衡状态的标志是A.

B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
③某合成氨速率方程为
 ,其中k为速率常数,根据表中数据,
,其中k为速率常数,根据表中数据,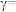
| 实验 |  |  |  |  |
| 1 | m | n | p | q |
| 2 | 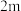 | n | p |  |
| 3 | m | n |  | 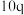 |
| 4 | m |  | P | 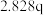 |
A.有利于平衡正向移动 B.提高正反应速率 C.防止催化剂中毒
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】草酸晶体的组成可用H2C2O4·xH2O表示,为了测定x值,进行如下实验:称取Wg草酸晶体,配成100.00mL无色水溶液。量取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为amol·L-1的KMnO4溶液滴定。试回答:
(1)滴定时所发生反应的化学方程式为___________ 。
(2)草酸是二元弱酸,则草酸的电离方程式为___________ ,请从“电离平衡”的角度解释:为什么草酸的第二步电离比第一步难___________ 。
(3)实验中不需要的仪器有(填序号)___________ ,还缺少的仪器有(填名称)___________ 。
a.托盘天平(带砝码,镊子)b.酸式滴定管c.碱式滴定管d.100mL容量瓶e.烧杯f.漏斗g.锥形瓶h.玻璃棒i.药匙j.烧瓶
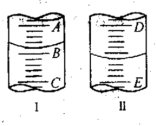
图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是___________ mL。图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)___________ 。
A.是amL B.是(25-a)mL C.一定大于amL D.一定大于(25-a)mL
(4)实验中,标准液KMnO4溶液应装在___________ 式滴定管中。若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴定至终点,则所测得的x值会___________ (偏大、偏小、无影响),达到滴定终点,溶液由___________ 色变为___________ 色。
(5)在滴定过程中若用amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为___________ mol·L-1。
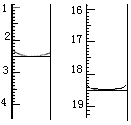
(6)若测得x=2,称取某二水合草酸晶体0.1200g,加适量水完全溶解,然后用0.02000mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为___________ 。(保留两位有效数字)
(1)滴定时所发生反应的化学方程式为
(2)草酸是二元弱酸,则草酸的电离方程式为
(3)实验中不需要的仪器有(填序号)
a.托盘天平(带砝码,镊子)b.酸式滴定管c.碱式滴定管d.100mL容量瓶e.烧杯f.漏斗g.锥形瓶h.玻璃棒i.药匙j.烧瓶

图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是
A.是amL B.是(25-a)mL C.一定大于amL D.一定大于(25-a)mL
(4)实验中,标准液KMnO4溶液应装在
(5)在滴定过程中若用amol·L-1的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为
(6)若测得x=2,称取某二水合草酸晶体0.1200g,加适量水完全溶解,然后用0.02000mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图。
的工艺流程如图。

资料:金属离子沉淀的pH
(1)酸浸前将菱锰矿石粉碎的目的是_______ 。
(2)沉淀池1中,先加 充分反应后再加氨水,写出加
充分反应后再加氨水,写出加 时发生反应的离子方程式:
时发生反应的离子方程式:_______ 。
(3)沉淀池2中,不能用 代替含硫沉淀剂,原因是
代替含硫沉淀剂,原因是_______ 。
(4)如图为 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为:在约100℃蒸发浓缩,
晶体”的操作为:在约100℃蒸发浓缩,_______ ,洗涤、干燥。

(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取 废渣,加酸将锰元素全部溶出成
废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于
,过滤,将滤液定容于 容量瓶中。
容量瓶中。
ⅱ.取 溶液于锥形瓶中,加入少量催化剂和过量
溶液于锥形瓶中,加入少量催化剂和过量 (过硫酸铵)溶液,加热、充分反应后,煮沸溶液使过量的
(过硫酸铵)溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。
ⅲ.用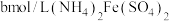 溶液滴定。
溶液滴定。
①补全步骤ⅱ中反应的离子方程式_______ 。
_______ _______
_______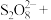 _______=_______
_______=_______ _______+_______
_______+_______
②步骤ⅱ中若未煮沸溶液,测定结果会:_______ (填“偏大”、“偏小”或“无影响”)。
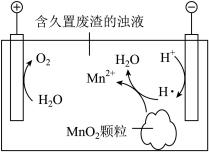
(6)废渣长期露置于空气,其中的锰元素逐渐转化为 。研究者用如图装置提取
。研究者用如图装置提取 中的锰元素。阴极的电极反应式为
中的锰元素。阴极的电极反应式为_______ 。
 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、
、 、
、 等)为原料制备
等)为原料制备 的工艺流程如图。
的工艺流程如图。
资料:金属离子沉淀的pH
| 金属离子 |  |  |  |  |
| 开始沉淀 | 1.5 | 6.3 | 7.4 | 7.6 |
| 完全沉淀 | 2.8 | 8.3 | 9.4 | 10.2 |
(2)沉淀池1中,先加
 充分反应后再加氨水,写出加
充分反应后再加氨水,写出加 时发生反应的离子方程式:
时发生反应的离子方程式:(3)沉淀池2中,不能用
 代替含硫沉淀剂,原因是
代替含硫沉淀剂,原因是(4)如图为
 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取“
的溶液”中提取“ 晶体”的操作为:在约100℃蒸发浓缩,
晶体”的操作为:在约100℃蒸发浓缩,
(5)受实际条件限制,“酸浸池”所得的废渣中还含有锰元素,其含量测定方法如下。
ⅰ.称取
 废渣,加酸将锰元素全部溶出成
废渣,加酸将锰元素全部溶出成 ,过滤,将滤液定容于
,过滤,将滤液定容于 容量瓶中。
容量瓶中。ⅱ.取
 溶液于锥形瓶中,加入少量催化剂和过量
溶液于锥形瓶中,加入少量催化剂和过量 (过硫酸铵)溶液,加热、充分反应后,煮沸溶液使过量的
(过硫酸铵)溶液,加热、充分反应后,煮沸溶液使过量的 分解。
分解。ⅲ.用
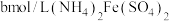 溶液滴定。
溶液滴定。①补全步骤ⅱ中反应的离子方程式
_______
 _______
_______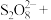 _______=_______
_______=_______ _______+_______
_______+_______②步骤ⅱ中若未煮沸溶液,测定结果会:
(6)废渣长期露置于空气,其中的锰元素逐渐转化为
 。研究者用如图装置提取
。研究者用如图装置提取 中的锰元素。阴极的电极反应式为
中的锰元素。阴极的电极反应式为
您最近一年使用:0次
【推荐3】海水中有非常丰富的化学资源。
(一)从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物:③将沉淀物与盐酸反应,结晶、过滤、干燥;④加热,将MgCl2·6H2O晶体转化为无水MgCl2⑤电解得到产物。
(1)以上提取镁的全过程中,没有涉及的化学反应类型是___________ (填字母)
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)步骤中多次进行过滤,实验室进行过滤时用到的玻璃仪器主要有___________ 。
(3)某兴趣小组模拟步骤④设计下图装置进行实验,
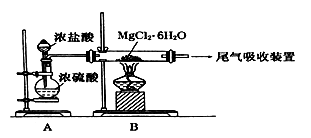
该装置中A的作用是___________ 。
(4)下列关于提取镁的说法中,正确的是___________ (填字母)
A.此法的优点之一是原料取自大海 B.进行①②③步骤的目的是富集MgCl2
C.可用电解熔融氧化镁的方法制取镁 D.将氯气循环利用,可提高经济效益
(二)从海水中得到的某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。
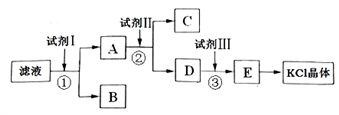
(1)起始滤液的pH___________ 7 (填“大于”、“小于”或“等于”),其原因是(用离子方程式表示)___________ 。
(2)试剂Ⅱ的化学式为___________ ,②中加入试剂Ⅱ的目的是___________ ;③中发生反应的离子方程式为___________ ;
(3)某同学称取提纯的产品0.6984g,溶解后定容在100mL容量瓶中,每次取25,00mL溶液,用0.1000mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为22.50mL,该产品的纯度为___________ 。
(一)从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物:③将沉淀物与盐酸反应,结晶、过滤、干燥;④加热,将MgCl2·6H2O晶体转化为无水MgCl2⑤电解得到产物。
(1)以上提取镁的全过程中,没有涉及的化学反应类型是
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
(2)步骤中多次进行过滤,实验室进行过滤时用到的玻璃仪器主要有
(3)某兴趣小组模拟步骤④设计下图装置进行实验,

该装置中A的作用是
(4)下列关于提取镁的说法中,正确的是
A.此法的优点之一是原料取自大海 B.进行①②③步骤的目的是富集MgCl2
C.可用电解熔融氧化镁的方法制取镁 D.将氯气循环利用,可提高经济效益
(二)从海水中得到的某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作。

(1)起始滤液的pH
(2)试剂Ⅱ的化学式为
(3)某同学称取提纯的产品0.6984g,溶解后定容在100mL容量瓶中,每次取25,00mL溶液,用0.1000mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为22.50mL,该产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】碳酸镧 为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧
为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧 ,如果溶液碱性太强,易生成受热分解的碱式碳酸镧
,如果溶液碱性太强,易生成受热分解的碱式碳酸镧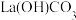 。回答下列问题:
。回答下列问题:
(一)利用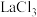 溶液制备水合碳酸澜
溶液制备水合碳酸澜

(1)仪器B的名称为_______ 。
(2)装置接口的连接顺序为f→_______ 。
(3)Z中应先通入_______ (填化学式),后通入过量的另一种气体,该气体需要过量的原因是_______ 。
(4)该反应中生成副产物氯化铵,请写出Z中生成水合碳酸镧的化学方程式:_______ 。
(二) 中x值的测定
中x值的测定
将石英玻璃A管称重,记为 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为 ,将装有试剂的装置C称重,记为
,将装有试剂的装置C称重,记为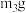 。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
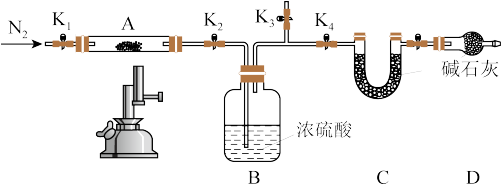
实验步骤如下:
①打开 和
和 ,缓缓通入;
,缓缓通入;
②数分钟后关闭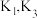 ,打开
,打开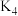 ,点燃酒精喷灯,加热A中样品;
,点燃酒精喷灯,加热A中样品;
③一段时间后,熄灭酒精喷灯,打开 ,通入数分钟后关闭
,通入数分钟后关闭 和
和 ,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为
,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为 (此时装置A中固体为
(此时装置A中固体为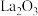 )。称重装置C,记为
)。称重装置C,记为 。
。
(5)实验中第二次通入 的目的为
的目的为_______ 。
(6)根据实验记录,当
_______ ,说明制得的样品中不含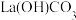 。
。
(7)水合碳酸镧的化学式中x=_________ (用含 的代数式表示,可不化简)。
的代数式表示,可不化简)。
 为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧
为白色粉末,难溶于水,分解温度900℃,可用于治疗高磷酸盐血症。在溶液中制备时,生成不溶于水的水合碳酸镧 ,如果溶液碱性太强,易生成受热分解的碱式碳酸镧
,如果溶液碱性太强,易生成受热分解的碱式碳酸镧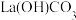 。回答下列问题:
。回答下列问题:(一)利用
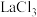 溶液制备水合碳酸澜
溶液制备水合碳酸澜
(1)仪器B的名称为
(2)装置接口的连接顺序为f→
(3)Z中应先通入
(4)该反应中生成副产物氯化铵,请写出Z中生成水合碳酸镧的化学方程式:
(二)
 中x值的测定
中x值的测定将石英玻璃A管称重,记为
 ,将样品装入石英玻璃管中,再次将装置A称重,记为
,将样品装入石英玻璃管中,再次将装置A称重,记为 ,将装有试剂的装置C称重,记为
,将装有试剂的装置C称重,记为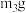 。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
。按图示连接好装置进行实验。(已知酒精喷灯温度可达1000℃)
实验步骤如下:
①打开
 和
和 ,缓缓通入;
,缓缓通入;②数分钟后关闭
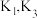 ,打开
,打开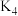 ,点燃酒精喷灯,加热A中样品;
,点燃酒精喷灯,加热A中样品;③一段时间后,熄灭酒精喷灯,打开
 ,通入数分钟后关闭
,通入数分钟后关闭 和
和 ,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为
,冷却到室温,称量A。重复上述操作步骤,直至A恒重,记为 (此时装置A中固体为
(此时装置A中固体为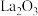 )。称重装置C,记为
)。称重装置C,记为 。
。(5)实验中第二次通入
 的目的为
的目的为(6)根据实验记录,当

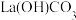 。
。(7)水合碳酸镧的化学式中x=
 的代数式表示,可不化简)。
的代数式表示,可不化简)。
您最近一年使用:0次
【推荐2】镁菱锌矿(主要成分为 等,含有少量
等,含有少量 等杂质)可用于生产媒染剂、防腐剂
等杂质)可用于生产媒染剂、防腐剂 以及耐火材料
以及耐火材料 。制备工艺流程如图:
。制备工艺流程如图:

已知: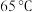 时
时 。
。
回答下列有关问题:
(1)浓盐酸浸取矿石时,保持较大液固体积比(如 ),目的是
),目的是___________ 。
(2)“氧化除铁”在 ,控制溶液
,控制溶液 在4.0~5.0,得到针铁矿渣的离子方程式为
在4.0~5.0,得到针铁矿渣的离子方程式为___________ 。
(3)“沉锌”前,滤液 中含有
中含有 和
和 ,保持该温度,则应加入氨水调节
,保持该温度,则应加入氨水调节 值在
值在___________ 
___________ 范围(离子浓度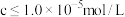 ,该离子沉淀完全)。
,该离子沉淀完全)。
(4)“酸解”后获得 的操作依次经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥。制得的
的操作依次经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥。制得的 在烘干时需减压烘干的原因是
在烘干时需减压烘干的原因是___________ 。
(5)“滤液”中加入 饱和溶液产生
饱和溶液产生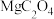 沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:
沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:___________ 。
 等,含有少量
等,含有少量 等杂质)可用于生产媒染剂、防腐剂
等杂质)可用于生产媒染剂、防腐剂 以及耐火材料
以及耐火材料 。制备工艺流程如图:
。制备工艺流程如图:
已知:
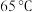 时
时 。
。回答下列有关问题:
(1)浓盐酸浸取矿石时,保持较大液固体积比(如
 ),目的是
),目的是(2)“氧化除铁”在
 ,控制溶液
,控制溶液 在4.0~5.0,得到针铁矿渣的离子方程式为
在4.0~5.0,得到针铁矿渣的离子方程式为(3)“沉锌”前,滤液
 中含有
中含有 和
和 ,保持该温度,则应加入氨水调节
,保持该温度,则应加入氨水调节 值在
值在
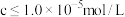 ,该离子沉淀完全)。
,该离子沉淀完全)。(4)“酸解”后获得
 的操作依次经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥。制得的
的操作依次经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥。制得的 在烘干时需减压烘干的原因是
在烘干时需减压烘干的原因是(5)“滤液”中加入
 饱和溶液产生
饱和溶液产生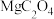 沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:
沉淀,若“灼烧”时产生两种气体,则该反应的化学方程式为:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】某工厂利用褐煤烟灰(主要成分为碳、二氧化锗,还有少量氧化铝和二氧化硅)制取纯GeO2的主要流程如下:

已知:GeO2是一种难溶于水的偏弱酸性的两性氧化物,GeCl4的沸点是83.1℃。
(1)写出二氧化锗与碳酸钠焙烧时发生反应的化学方程式:_______________ 。
(2)用水浸取焙烧物长达2小时的目的是_______________________ 。
(3)“酸化”至溶液中盐酸浓度为5.3 mol·L-1时有利于生成四氯化锗,写出该反应的化学方程式:_____________ 。
(4)若滤液“酸化”时酸度不够,溶液会出现明显的浑浊,原因是_____________________ 。
(5)操作“X”的名称为________________ 。
(6)四氯化锗与高纯水反应的化学方程式为__________________ 。

已知:GeO2是一种难溶于水的偏弱酸性的两性氧化物,GeCl4的沸点是83.1℃。
(1)写出二氧化锗与碳酸钠焙烧时发生反应的化学方程式:
(2)用水浸取焙烧物长达2小时的目的是
(3)“酸化”至溶液中盐酸浓度为5.3 mol·L-1时有利于生成四氯化锗,写出该反应的化学方程式:
(4)若滤液“酸化”时酸度不够,溶液会出现明显的浑浊,原因是
(5)操作“X”的名称为
(6)四氯化锗与高纯水反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】某油脂厂废弃的油脂氢化镍催化剂主要成分为金属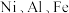 及其氧化物,还有少量其他不溶性物质。回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。回收其中的镍制备硫酸镍晶体 的工艺流程如下。
的工艺流程如下。
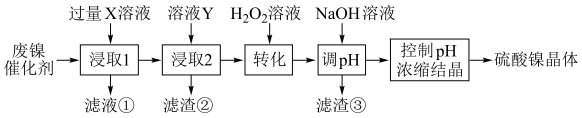
已知: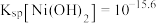 ;
;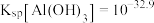 ;
;
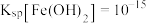 ;
;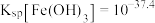 ;
;
(1)在镍催化下油脂氢化过程中发生的反应类型为_______ ;油脂氢化的优点是_________ 。
(2)“滤液①”中主要溶质的化学式为___________ 。
(3)加入 溶液“转化”后,溶液中大量减少的阳离子是
溶液“转化”后,溶液中大量减少的阳离子是___________ 。
(4)若“转化”后溶液中 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是___________ 。
(5)TG-DTA是指对同一个焙烧试样同时进行热重(TG)和差热(DTA)分析的同步热分析技术。由TG-DTA曲线可以同时得到焙烧试样的质量及焙烧过程热效应随温度的变化关系如图所示。当DTA曲线中出现明显的吸收峰时,说明该温度区间发生吸热反应。
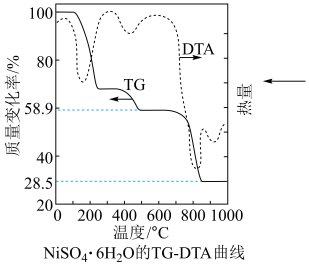
①通过计算确定500℃下焙烧产物的成分为___________ 。(写出计算过程)
②900℃下,DTA曲线出现一个吸收峰的可能原因是___________ 。
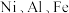 及其氧化物,还有少量其他不溶性物质。回收其中的镍制备硫酸镍晶体
及其氧化物,还有少量其他不溶性物质。回收其中的镍制备硫酸镍晶体 的工艺流程如下。
的工艺流程如下。
已知:
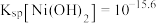 ;
;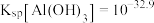 ;
;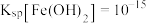 ;
;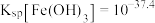 ;
;(1)在镍催化下油脂氢化过程中发生的反应类型为
(2)“滤液①”中主要溶质的化学式为
(3)加入
 溶液“转化”后,溶液中大量减少的阳离子是
溶液“转化”后,溶液中大量减少的阳离子是(4)若“转化”后溶液中
 ,则“调
,则“调 ”应控制的
”应控制的 范围是
范围是(5)TG-DTA是指对同一个焙烧试样同时进行热重(TG)和差热(DTA)分析的同步热分析技术。由TG-DTA曲线可以同时得到焙烧试样的质量及焙烧过程热效应随温度的变化关系如图所示。当DTA曲线中出现明显的吸收峰时,说明该温度区间发生吸热反应。

①通过计算确定500℃下焙烧产物的成分为
②900℃下,DTA曲线出现一个吸收峰的可能原因是
您最近一年使用:0次
【推荐2】砷 是生命的第七元素,可形成多种重要的化合物。
是生命的第七元素,可形成多种重要的化合物。
I.三氧化二砷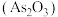 是重要的化工原料,也可以用于治疗某些疾病。一种以含砷废水制备三氧化二砷的流程如图:
是重要的化工原料,也可以用于治疗某些疾病。一种以含砷废水制备三氧化二砷的流程如图:

资料:
i.含砷废水的主要成分: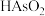 (亚砷酸)、
(亚砷酸)、 、
、 、
、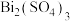 (硫酸铋)。
(硫酸铋)。
ii.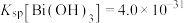 。
。
(1)纯化
纯化过程中加NaOH调节 ,主要目的是
,主要目的是___________ 。充分反应后,过滤分离出精制含砷废水。
(2)还原浸出
①补全还原浸出过程发生主要反应的化学方程式:___________ 。
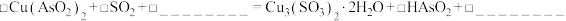 。
。
②其他条件相同时,还原浸出1h,不同温度下砷的浸出率如图。随着温度升高,砷的浸出率先增大后减小的原因是___________ 。

(3)测定产品纯度
取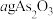 产品,加适量硫酸溶解,加入指示剂,用
产品,加适量硫酸溶解,加入指示剂,用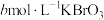 溶液滴定,终点时生成
溶液滴定,终点时生成 和
和 ,消耗
,消耗 溶液。
溶液。 产品中
产品中 的质量分数是
的质量分数是___________ %( 的摩尔质量为
的摩尔质量为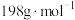 )。
)。
II.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。
(4)基态砷原子的价电子轨道排布图为___________ 。
(5)砷化镓晶胞结构如图所示,若沿体对角线方向进行投影则得到如图,请在图中将As原子的位置涂黑。晶体中As原子周围与其距离最近的As原子的个数为___________ ,若As原子的半径为xpm,Ga原子的半径为ypm,则最近的两个As原子的距离为___________ pm。

 是生命的第七元素,可形成多种重要的化合物。
是生命的第七元素,可形成多种重要的化合物。I.三氧化二砷
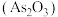 是重要的化工原料,也可以用于治疗某些疾病。一种以含砷废水制备三氧化二砷的流程如图:
是重要的化工原料,也可以用于治疗某些疾病。一种以含砷废水制备三氧化二砷的流程如图:
资料:
i.含砷废水的主要成分:
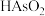 (亚砷酸)、
(亚砷酸)、 、
、 、
、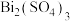 (硫酸铋)。
(硫酸铋)。ii.
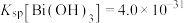 。
。(1)纯化
纯化过程中加NaOH调节
 ,主要目的是
,主要目的是(2)还原浸出
①补全还原浸出过程发生主要反应的化学方程式:
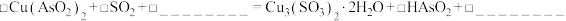 。
。②其他条件相同时,还原浸出1h,不同温度下砷的浸出率如图。随着温度升高,砷的浸出率先增大后减小的原因是

(3)测定产品纯度
取
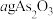 产品,加适量硫酸溶解,加入指示剂,用
产品,加适量硫酸溶解,加入指示剂,用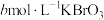 溶液滴定,终点时生成
溶液滴定,终点时生成 和
和 ,消耗
,消耗 溶液。
溶液。 产品中
产品中 的质量分数是
的质量分数是 的摩尔质量为
的摩尔质量为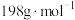 )。
)。II.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。
(4)基态砷原子的价电子轨道排布图为
(5)砷化镓晶胞结构如图所示,若沿体对角线方向进行投影则得到如图,请在图中将As原子的位置涂黑。晶体中As原子周围与其距离最近的As原子的个数为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】硫脲[CS(NH2)2](M=76)在药物制备、金属矿物浮选等方面有广泛应用。实验室中先制备Ca(HS)2,再与CaCN2溶液反应合成CS(NH2)2,实验装置如图所示(夹持及加热装置略)。

已知:CS(NH2)2易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)盛装盐酸的仪器名称是___________ 。
(2)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整___________ 。
(3)检查装置气密性后加入药品,打开K2.装置B中盛装的试剂为___________ 。
(4)关闭K2,撤走搅拌器,打开K3,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度不高于80℃的原因是_________ ,D处合成硫脲的化学方程式为________ 。
(5)将装置D中液体过滤后,结晶得到粗产品。
①称取mg产品,加水溶解配成500mL溶液。在锥形瓶中加入足量氢氧化钠溶液和n×10-3mol单质碘,
发生反应:6NaOH+3I2=NaIO3+5NaI+3H2O,量取25.00mL硫脲溶液加入锥形瓶,发生反应:NaIO3+3CS(NH2)2=3HOSC(NH)NH2+NaI。
②充分反应后加稀硫酸至酸性,发生反应:NaIO3+5NaI+3H2SO4=3I2+3Na2SO4+3H2O,滴加两滴淀粉溶液,用cmol/LNa2S2O3标准溶液滴定,发生反应:I2+2Na2S2O3=2NaI+Na2S4O6.至终点时消耗标准溶液VmL。
粗产品中硫脲的质量分数为___________ (用含“m、n、C、V的式子表示);若滴定时加入的稀硫酸量不足,会导致所测硫脲的质量分数___________ (填“偏高”、“偏低”或“不变”)。(已知:4NaIO3+3Na2S2O3+6NaOH=4NaI+6Na2SO4+3H2O。)

已知:CS(NH2)2易溶于水,易被氧化,受热时部分发生异构化生成NH4SCN。
回答下列问题:
(1)盛装盐酸的仪器名称是
(2)实验前先检查装置气密性,操作:
①在E中加水至浸没导管末端,……;
②微热A处三颈烧瓶,观察到E处导管末端有气泡冒出,移走酒精灯;
③一段时间后,E处导管末端形成一段水柱,且高度不变。
将操作①补充完整
(3)检查装置气密性后加入药品,打开K2.装置B中盛装的试剂为
(4)关闭K2,撤走搅拌器,打开K3,水浴加热D中三颈烧瓶,在80℃时合成硫脲,同时生成一种常见的碱。控制温度不高于80℃的原因是
(5)将装置D中液体过滤后,结晶得到粗产品。
①称取mg产品,加水溶解配成500mL溶液。在锥形瓶中加入足量氢氧化钠溶液和n×10-3mol单质碘,
发生反应:6NaOH+3I2=NaIO3+5NaI+3H2O,量取25.00mL硫脲溶液加入锥形瓶,发生反应:NaIO3+3CS(NH2)2=3HOSC(NH)NH2+NaI。
②充分反应后加稀硫酸至酸性,发生反应:NaIO3+5NaI+3H2SO4=3I2+3Na2SO4+3H2O,滴加两滴淀粉溶液,用cmol/LNa2S2O3标准溶液滴定,发生反应:I2+2Na2S2O3=2NaI+Na2S4O6.至终点时消耗标准溶液VmL。
粗产品中硫脲的质量分数为
您最近一年使用:0次



