2024高三下·全国·专题练习
1 . 研究CO2 加氢制CH4 对资源综合利用有重要意义。相关的主要化学反应如下:
Ⅰ.CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1<0
CH4(g)+2H2O(g) ΔH1<0
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
Ⅲ.2CO(g)+2H2(g) CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
在一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和4 mol H2发生上述反应,20 min时,容器内反应达到平衡,容器中CH4(g)为a mol,CO为b mol,以H2表示的0~20 min内平均反应速率v(H2)=________ mol·L-1·min-1(用含a、b、V的代数式表示,下同),此时H2O(g) 的浓度为________ mol·L-1,反应Ⅱ的平衡常数为________ (列出计算式)。
Ⅰ.CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH1<0
CH4(g)+2H2O(g) ΔH1<0Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2Ⅲ.2CO(g)+2H2(g)
 CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1在一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和4 mol H2发生上述反应,20 min时,容器内反应达到平衡,容器中CH4(g)为a mol,CO为b mol,以H2表示的0~20 min内平均反应速率v(H2)=
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
2 . 对于基元反应,如aA+bB cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
反应Ⅰ:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
反应Ⅱ:8NH3(g)+6NO2(g) 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g) 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
(1)ΔH4=______ kJ·mol-1
(2)计算653K时的平衡常数K=______ 。
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为______ mol·L-1·s-1
 cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:反应Ⅰ:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1反应Ⅱ:8NH3(g)+6NO2(g)
 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g)
 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1(1)ΔH4=
(2)计算653K时的平衡常数K=
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
3 . 空气中CO2含量的控制和CO2资源利用具有重要意义。
(1)已知25℃、101 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
Ⅰ:CO2(g)+H2(g) CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1
CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1
该反应的速率方程为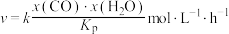 ,其中x表示相应气体的物质的量分数,
,其中x表示相应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后
为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后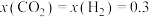 ,此时反应Ⅰ的速率
,此时反应Ⅰ的速率
______  (用含k的代数式表示)。
(用含k的代数式表示)。
(1)已知25℃、101
 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:Ⅰ:CO2(g)+H2(g)
 CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1
CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1该反应的速率方程为
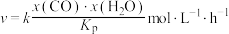 ,其中x表示相应气体的物质的量分数,
,其中x表示相应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后
为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后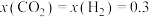 ,此时反应Ⅰ的速率
,此时反应Ⅰ的速率
 (用含k的代数式表示)。
(用含k的代数式表示)。
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
4 . H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=
COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=______ 。H2S的平衡转化率
______ %。
 COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=
COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
5 . Bodensteins研究了下列反应:2HI(g)  H2(g)+I2(g),在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g),在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为___________ (以K和k正表示)。若k正=0.0027 min-1,在t=40 min时,v正=___________ min-1。
 H2(g)+I2(g),在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g),在716 K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
您最近一年使用:0次
2023高三·全国·专题练习
6 . 某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1 mol NH3通入3 L的密闭容器中进行反应(此时容器内总压为200 kPa),各物质的分压随时间的变化曲线如图所示。

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=___________ mol·L-1·min-1(用含t1的代数式表示)
(2)在该温度下,反应的标准平衡常数K⊖=___________ [已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g)  gG(g)+hH(g) K⊖=
gG(g)+hH(g) K⊖= ,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]
,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]

(1)若保持容器容积不变,t1时反应达到平衡,用H2的浓度变化表示0~t1时间内的反应速率v(H2)=
(2)在该温度下,反应的标准平衡常数K⊖=
 gG(g)+hH(g) K⊖=
gG(g)+hH(g) K⊖= ,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]
,其中p⊖=100 kPa,pG、pH、pD、pE为各组分的平衡分压]
您最近一年使用:0次
7 . 一定条件下,将
 和
和
 充入固定容积为2 L的密闭容器中,发生反应
充入固定容积为2 L的密闭容器中,发生反应 ,反应体系中某组分浓度随时间的变化关系如图所示。
,反应体系中某组分浓度随时间的变化关系如图所示。
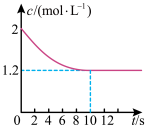
(1)从反应开始到平衡状态,以 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为________  。
。
(2)此条件下,该反应的化学平衡常数
________ (列出计算式即可), 的平衡转化率为
的平衡转化率为________ 。

 和
和
 充入固定容积为2 L的密闭容器中,发生反应
充入固定容积为2 L的密闭容器中,发生反应 ,反应体系中某组分浓度随时间的变化关系如图所示。
,反应体系中某组分浓度随时间的变化关系如图所示。
(1)从反应开始到平衡状态,以
 的浓度变化表示的平均反应速率为
的浓度变化表示的平均反应速率为 。
。(2)此条件下,该反应的化学平衡常数

 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
2023高三·全国·专题练习
8 .  时,
时, 的正反应速率表达式为
的正反应速率表达式为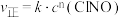 ,测得速率和浓度的关系如下表:
,测得速率和浓度的关系如下表:

_______ ;
_______ 。
 时,
时, 的正反应速率表达式为
的正反应速率表达式为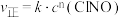 ,测得速率和浓度的关系如下表:
,测得速率和浓度的关系如下表:| 序号 | 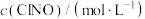 | 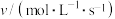 |
| ① | 0.30 | 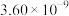 |
| ② | 0.60 | 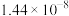 |
| ③ | 0.90 | 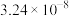 |


您最近一年使用:0次
2023高三·全国·专题练习
9 . 一定温度下,在 的四氯化碳溶液
的四氯化碳溶液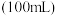 中发生分解反应:
中发生分解反应: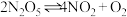 。在不同时刻测量放出的
。在不同时刻测量放出的 体积,换算成
体积,换算成 浓度如下表:
浓度如下表:
(1)计算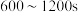 ,生成
,生成 的平均速率
的平均速率_______
(2)计算反应 时,放出标准状况下的
时,放出标准状况下的 体积
体积_______
(3)分析上表的变化规律,推测表中x值_______
 的四氯化碳溶液
的四氯化碳溶液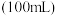 中发生分解反应:
中发生分解反应: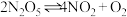 。在不同时刻测量放出的
。在不同时刻测量放出的 体积,换算成
体积,换算成 浓度如下表:
浓度如下表: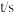 | 0 | 600 | 1200 | 1710 | 2220 | 2820 | x |
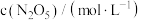 | 1.40 | 0.96 | 0.66 | 0.48 | 0.35 | 0.24 | 0.12 |
(1)计算
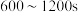 ,生成
,生成 的平均速率
的平均速率(2)计算反应
 时,放出标准状况下的
时,放出标准状况下的 体积
体积(3)分析上表的变化规律,推测表中x值
您最近一年使用:0次

 催化剂作用下,使
催化剂作用下,使 转化为
转化为 的反应
的反应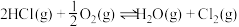 具有更好的催化活性。一定条件下测得反应过程中
具有更好的催化活性。一定条件下测得反应过程中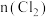 的数据如下:
的数据如下: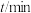

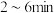 内以
内以 为单位,写出计算过程)。
为单位,写出计算过程)。


