1 . 研究CO、CO2的转化既可减少碳排放,又可获得许多实用的含碳物质。回答下列问题:
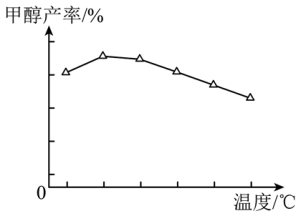
(1)以CO2、H2为原料,在铜基催化剂作用下可合成甲醇,反应如下(不考虑副反应):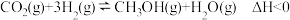 ,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
①该反应自发进行的条件是___________ (填“高温”“低温”或“任意温度”)。
②甲醇产率随温度升高先增大后减小的原因是___________ 。
(2)以CO、H2为原料在一定条件下也可合成甲醇,发生的反应如下:
主反应:
副反应:
一定条件下,向体积为V L的恒容密闭容器中投入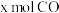 和
和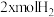 ,发生上述反应,平衡时容器内CH3OH的物质的量为
,发生上述反应,平衡时容器内CH3OH的物质的量为 ,C的物质的量为
,C的物质的量为 。则主反应的平衡常数K=
。则主反应的平衡常数K=___________ 。
(3)我国科学家设计 熔盐捕获与转化装置如图所示:
熔盐捕获与转化装置如图所示:
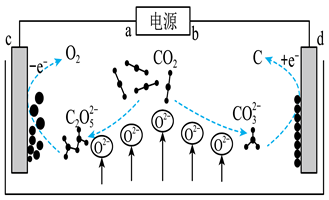
①d极的电极反应式为___________ 。
②若电源使用铅蓄电池,当电路中转移2 mol电子时,Pb电极的质量理论上___________ (填“增加”或“减少”)了____ g。
(4)水煤气变换是重要的化工过程,反应为: 。已知该反应的平衡常数K与热力学温度T的关系为
。已知该反应的平衡常数K与热力学温度T的关系为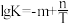 (m、n均为正数)。
(m、n均为正数)。
①水煤气变换是____ (填“吸热”或“放热”)反应。
②热力学温度为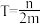 时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为
时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为 ,则
,则____ (填标号)。
A.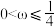 B.
B.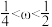 C.
C.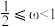
(1)以CO2、H2为原料,在铜基催化剂作用下可合成甲醇,反应如下(不考虑副反应):
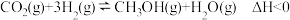 ,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
,反应在恒容密闭容器中进行。反应时间一定,甲醇的产率随温度的变化如图所示(不考虑此过程中催化剂活性的变化)。
①该反应自发进行的条件是
②甲醇产率随温度升高先增大后减小的原因是
(2)以CO、H2为原料在一定条件下也可合成甲醇,发生的反应如下:
主反应:

副反应:

一定条件下,向体积为V L的恒容密闭容器中投入
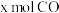 和
和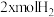 ,发生上述反应,平衡时容器内CH3OH的物质的量为
,发生上述反应,平衡时容器内CH3OH的物质的量为 ,C的物质的量为
,C的物质的量为 。则主反应的平衡常数K=
。则主反应的平衡常数K=(3)我国科学家设计
 熔盐捕获与转化装置如图所示:
熔盐捕获与转化装置如图所示:
①d极的电极反应式为
②若电源使用铅蓄电池,当电路中转移2 mol电子时,Pb电极的质量理论上
(4)水煤气变换是重要的化工过程,反应为:
 。已知该反应的平衡常数K与热力学温度T的关系为
。已知该反应的平衡常数K与热力学温度T的关系为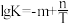 (m、n均为正数)。
(m、n均为正数)。①水煤气变换是
②热力学温度为
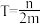 时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为
时,在恒温密闭容器中将等物质的量的CO和H2O(g)混合,选择适当的催化剂进行反应。平衡时体系中H2的物质的量分数为 ,则
,则A.
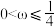 B.
B.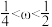 C.
C.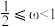
您最近一年使用:0次
2 .  肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:___________ .
(2)实验室用两种固体制取NH3的反应化学方程式为_____________ .
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为_____________ .
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为_____________ .
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
①焓变△H_________ 0(填“>”、“<”或“=”).
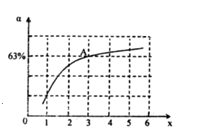
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)\frac{n(NH_{3})}{n(CO_{2})}=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是_____________ .图中A点处,NH3的平衡转化率为___________ .
(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)⇌2NH3(g),测得甲容器中H2的平衡转化率为40%.
①判断乙容器中反应进行的方向是_____________ (填“正向或“逆向”)移动.
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为_____________ 。
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:___________________ ,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是____________ (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为_____________________ 。
(7)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是___________ (填字母代号)。
a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(8)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为__________ {已知Ksp[Mg(OH)2]=4.0×10-12]}
 肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:
肼(N2H4)和氨是氮的两种常见化合物,在科学技术和生产中有广泛应用.回答下列问题:(1)N2H4中N原子核外最外层达到8电子稳定结构.写出N2H4的结构式:
(2)实验室用两种固体制取NH3的反应化学方程式为
(3)NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为
(4)肼一空气燃料电池是一种碱性环保电池,该电池放电时,负极的反应式为
(5)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2]反应的化学方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)\frac{n(NH_{3})}{n(CO_{2})}=x,如图是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是

(6)在恒温恒容密闭容器中按照甲、乙、丙三种方式分别投料,发生反应:N2(g)+3H2(g)⇌2NH3(g),测得甲容器中H2的平衡转化率为40%.
| n(N2) | n(H2) | n(NH3) | |
| 甲 | 1mol | 3mol | 0mol |
| 乙 | 0.5mol | 1.5mol | 1mol |
| 丙 | 0mol | 0mol | 4mol |
①判断乙容器中反应进行的方向是
②达平衡时,甲、乙、丙三容器中NH3的体积分数大小顺序为
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式:
(7)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是
4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是a.增大压强 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
(8)如果某氨水的电离程度为1%,浓度为0.01 mol/LMgCl2溶液滴加氨水至开始产生沉淀时(不考虑溶液体积变化),溶液中的NH3·H2O的浓度为
您最近一年使用:0次
3 . Ⅰ.中国科学家首次实现了二氧化碳到淀粉的全合成,相关成果由国际知名学术期刊《科学》在线发表。 的捕集、利用与封存是科学家研究的重要课题,利用
的捕集、利用与封存是科学家研究的重要课题,利用 与
与 制备“合成气”
制备“合成气” 、
、 ,合成气可直接制备甲醇,反应原理为:
,合成气可直接制备甲醇,反应原理为: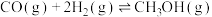
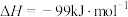
(1)若要该反应自发进行,_____ (填“高温”或“低温”)更有利。
(2)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是_____ (填字母序号)。
A.反应物的物质的量的比值不变
B.混合气体的密度不再变化
C. 的百分含量不再变化
的百分含量不再变化
D.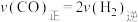
E.混合气体的平均相对分子质量不再变化
(3)把 转化为
转化为 是降碳并生产化工原料的常用方法,有关反应如下:
是降碳并生产化工原料的常用方法,有关反应如下:
①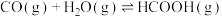
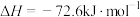
②

③
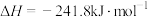
则 与
与 合成
合成 反应的热化学方程式:
反应的热化学方程式:_____
(4)受绿色植物光合作用的启示,太阳能固碳装置被设计出来,则固碳电极反应为_____ 。
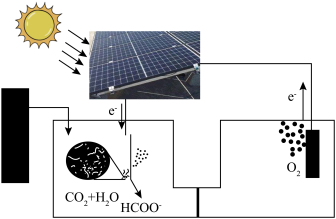
Ⅱ.我国学者结合实验与计算机模拟结果,研究了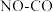 的反应历程。在催化剂作用下,此反应为
的反应历程。在催化剂作用下,此反应为  l可有效降低汽车尾气污染物排放。
l可有效降低汽车尾气污染物排放。
(5)探究温度、压强(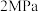 ,
,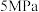 )对反应
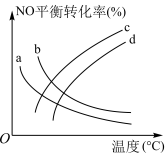
)对反应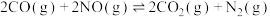 的影响,如图所示,表示
的影响,如图所示,表示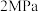 的是
的是_____ (填标号)。
(6)一定温度下,向一容积为1L的恒容密闭容器按体积3∶2比例充入CO和NO,压强为5MPa发生上述反应,当反应达到平衡时容器内压强变为起始时的 ,此温度下该反应的平衡常数
,此温度下该反应的平衡常数 =
=_____ ( 为压强平衡常数)。
为压强平衡常数)。
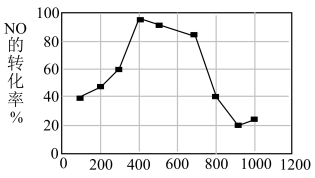
(7)若在相同时间内测得NO的转化率随温度的变化曲线如图,解释NO的转化率随温度的升高由上升到下降、下降由缓到急的主要原因是_____ 。
 的捕集、利用与封存是科学家研究的重要课题,利用
的捕集、利用与封存是科学家研究的重要课题,利用 与
与 制备“合成气”
制备“合成气” 、
、 ,合成气可直接制备甲醇,反应原理为:
,合成气可直接制备甲醇,反应原理为: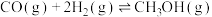
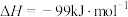
(1)若要该反应自发进行,
(2)在恒温,恒容密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是
A.反应物的物质的量的比值不变
B.混合气体的密度不再变化
C.
 的百分含量不再变化
的百分含量不再变化D.
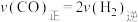
E.混合气体的平均相对分子质量不再变化
(3)把
 转化为
转化为 是降碳并生产化工原料的常用方法,有关反应如下:
是降碳并生产化工原料的常用方法,有关反应如下:①
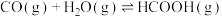
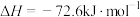
②


③

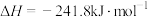
则
 与
与 合成
合成 反应的热化学方程式:
反应的热化学方程式:(4)受绿色植物光合作用的启示,太阳能固碳装置被设计出来,则固碳电极反应为

Ⅱ.我国学者结合实验与计算机模拟结果,研究了
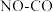 的反应历程。在催化剂作用下,此反应为
的反应历程。在催化剂作用下,此反应为  l可有效降低汽车尾气污染物排放。
l可有效降低汽车尾气污染物排放。(5)探究温度、压强(
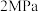 ,
,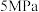 )对反应
)对反应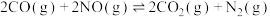 的影响,如图所示,表示
的影响,如图所示,表示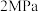 的是
的是
(6)一定温度下,向一容积为1L的恒容密闭容器按体积3∶2比例充入CO和NO,压强为5MPa发生上述反应,当反应达到平衡时容器内压强变为起始时的
 ,此温度下该反应的平衡常数
,此温度下该反应的平衡常数 =
= 为压强平衡常数)。
为压强平衡常数)。
(7)若在相同时间内测得NO的转化率随温度的变化曲线如图,解释NO的转化率随温度的升高由上升到下降、下降由缓到急的主要原因是
您最近一年使用:0次
解题方法
4 . 氨气是现代工业、农业生产最基础的化工原料之一、
Ⅰ.传统的“哈伯法”反应原理为:
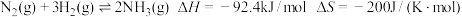
(1)上述反应在常温下___________ (填“能”或“不能”)自发进行。
(2)“哈伯法”合成氨的工业条件为400~500℃、10~30MPa,是综合考虑了___________ 因素(至少写两点)。
(3)t℃时向2L的某刚性容器中充入 和
和 。已知平衡时体系中
。已知平衡时体系中 的体积占比为
的体积占比为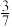 ,则该反应的平衡常数
,则该反应的平衡常数
___________ 。
Ⅱ.“哈伯法”的原料 来自于化石燃料,该过程会产生大量温室气体
来自于化石燃料,该过程会产生大量温室气体 。近年来有科学家提出通过电解氮气和水来合成氨气(NRR反应)。
。近年来有科学家提出通过电解氮气和水来合成氨气(NRR反应)。
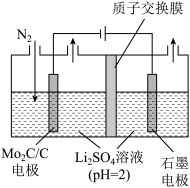
(4)一种常温常压下NRR反应的装置如图所示,请写出阴极的电极反应方程式:___________ 。
(5)下表为不同电压下进行电解时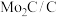 电极表面的气体产生情况(以
电极表面的气体产生情况(以 为计算值)
为计算值)
①表中 的最大产率=
的最大产率=___________ (产率=实际产量/理论产量×100%,常温常压下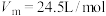 ,结果保留3位有效数值)
,结果保留3位有效数值)
②较高电压下 的生成速率下降的原因是:
的生成速率下降的原因是:___________ 。
(6)如图为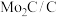 电极表面“
电极表面“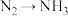 ”的可能路径(
”的可能路径( 表示电极表面)。该过程中会产生两种具有对称结构的副产物,分别为:
表示电极表面)。该过程中会产生两种具有对称结构的副产物,分别为:___________ (填化学式)。
Ⅰ.传统的“哈伯法”反应原理为:
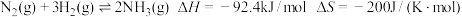
(1)上述反应在常温下
(2)“哈伯法”合成氨的工业条件为400~500℃、10~30MPa,是综合考虑了
(3)t℃时向2L的某刚性容器中充入
 和
和 。已知平衡时体系中
。已知平衡时体系中 的体积占比为
的体积占比为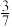 ,则该反应的平衡常数
,则该反应的平衡常数
Ⅱ.“哈伯法”的原料
 来自于化石燃料,该过程会产生大量温室气体
来自于化石燃料,该过程会产生大量温室气体 。近年来有科学家提出通过电解氮气和水来合成氨气(NRR反应)。
。近年来有科学家提出通过电解氮气和水来合成氨气(NRR反应)。(4)一种常温常压下NRR反应的装置如图所示,请写出阴极的电极反应方程式:
(5)下表为不同电压下进行电解时
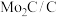 电极表面的气体产生情况(以
电极表面的气体产生情况(以 为计算值)
为计算值)①表中
 的最大产率=
的最大产率=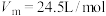 ,结果保留3位有效数值)
,结果保留3位有效数值) ②较高电压下
 的生成速率下降的原因是:
的生成速率下降的原因是:| 电压V |  通入速率mL/min 通入速率mL/min |  生成速率mL/min 生成速率mL/min |  生成速率mg/min 生成速率mg/min |
| 0.2 | 25 | 0.015 | 0.51 |
| 0.3 | 25 | 0.038 | 0.68 |
| 0.4 | 25 | 0.095 | 0.65 |
| 0.5 | 25 | 0.11 | 0.52 |
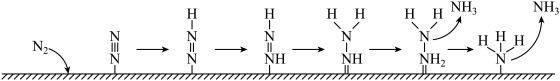
(6)如图为
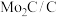 电极表面“
电极表面“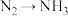 ”的可能路径(
”的可能路径( 表示电极表面)。该过程中会产生两种具有对称结构的副产物,分别为:
表示电极表面)。该过程中会产生两种具有对称结构的副产物,分别为:
您最近一年使用:0次



