名校
1 . 下列实验不能达到目的的是

| A.图①:验证勒夏特列原理 |
| B.图②:探究温度对化学平衡的影响 |
| C.图③:测定锌与稀硫酸反应的反应速率 |
| D.图④:探究反应物的接触面积对反应速率的影响 |
您最近一年使用:0次
2023-10-16更新
|
433次组卷
|
5卷引用:贵州省普通高中部分学校2023-2024学年高二上学期第一次联考化学试题
名校
2 . Ⅰ.为比较 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
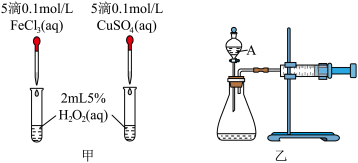
(1)定性分析:如图甲有同学提出将 改为
改为
 更为合理,其理由是
更为合理,其理由是___________ 。
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中需要测量的数据是___________ 。
Ⅱ.某实验小组通过锌粒与稀硫酸反应的实验,研究影响反应速率的因素,并绘制出甲、乙两种图象。

(3)甲图中, 到
到 速率明显加快的主要原因是
速率明显加快的主要原因是___________ 。
(4)乙图中,a为锌粒与足量稀硫酸反应产生氢气的体积随时间变化情况,其它条件不变,添加适量的下列试剂___________,能使a变为b。
Ⅲ.已知恒容密闭容器中发生二氧化碳和氢气合成甲醇的反应 。
。
(5)有利于提高平衡时 转化率的措施有
转化率的措施有___________ (填标号)。
A.使用催化剂 B.加压 C.增大 和
和 的初始投料比
的初始投料比
(6)下列能说明反应达到平衡的是___________(填标号)。
 和
和 对
对 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
(1)定性分析:如图甲有同学提出将
 改为
改为
 更为合理,其理由是
更为合理,其理由是(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中需要测量的数据是
Ⅱ.某实验小组通过锌粒与稀硫酸反应的实验,研究影响反应速率的因素,并绘制出甲、乙两种图象。

(3)甲图中,
 到
到 速率明显加快的主要原因是
速率明显加快的主要原因是(4)乙图中,a为锌粒与足量稀硫酸反应产生氢气的体积随时间变化情况,其它条件不变,添加适量的下列试剂___________,能使a变为b。
A. | B. | C. 溶液 溶液 | D.浓 |
Ⅲ.已知恒容密闭容器中发生二氧化碳和氢气合成甲醇的反应
 。
。(5)有利于提高平衡时
 转化率的措施有
转化率的措施有A.使用催化剂 B.加压 C.增大
 和
和 的初始投料比
的初始投料比(6)下列能说明反应达到平衡的是___________(填标号)。
| A.反应体系内气体的压强不再发生变化 |
| B.反应体系内气体的密度不再发生变化 |
C. 与 与 的浓度之比为1∶1 的浓度之比为1∶1 |
D.当有1mol 被消耗的同时有1mol 被消耗的同时有1mol 被消耗 被消耗 |
您最近一年使用:0次
解题方法
3 . 下列实验装置(部分夹持装置已略去)不能达到对应实验目的的是


| A.测定锌与稀硫酸反应速率 | B.测定中和反应的反应热 |
C.比较 和 和 溶解度大小 溶解度大小 | D.探究铁的吸氧腐蚀 |
您最近一年使用:0次
解题方法
4 . 影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。实验药品:铜、铁、镁、0.5mol·L-1H2SO4溶液、2mol·L-1H2SO4溶液。甲同学研究的实验报告如表:
(1)甲同学表中实验步骤②为___ 。
(2)甲同学的实验目的是___ 。要得出正确的实验结论,还需要控制的实验条件是__ 。
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验。
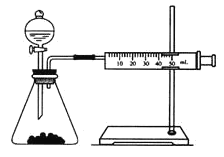
(3)乙同学完成该实验应选用的实验药品是___ 。
(4)乙同学在实验中应该测定的数据是____ 。
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol·L-1的硫酸溶液于三支试管中支试管中 ②______ | 反应速率:镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
(2)甲同学的实验目的是
乙同学为了更精确地研究浓度对反应速率的影响,利用如图所示装置进行实验。

(3)乙同学完成该实验应选用的实验药品是
(4)乙同学在实验中应该测定的数据是
您最近一年使用:0次
名校
5 . KI溶液在酸性条件下能与氧气反应。
现有以下实验记录:
回答下列问题:
(1)该反应的离子方程式为___ 。
(2)该实验的目的是__ 。
(3)实验试剂除了1mol/LKI溶液、0.1mol/LH2SO4溶液外,还需要的试剂是___ ,实验现象为___ 。
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是__ (填字母)。
A.温度
B.试剂的浓度
C.试剂的用量(体积)
D.试剂添加的顺序
(5)由上述实验记录可得出的结论是__ 。
现有以下实验记录:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| 显色时间/s | 160 | 80 | 40 | 20 | 10 |
回答下列问题:
(1)该反应的离子方程式为
(2)该实验的目的是
(3)实验试剂除了1mol/LKI溶液、0.1mol/LH2SO4溶液外,还需要的试剂是
(4)上述实验操作中除了需要(3)的条件外,还必须控制不变的是
A.温度
B.试剂的浓度
C.试剂的用量(体积)
D.试剂添加的顺序
(5)由上述实验记录可得出的结论是
您最近一年使用:0次
2020-10-01更新
|
190次组卷
|
2卷引用:贵州省思南中学2020-2021学年高二上学期第一次月考化学试题
解题方法
6 . I.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案。
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4溶液转化为MnSO4,每消耗1molH2C2O4转移___ mol电子。为了观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4)∶n(KMnO4)≥___ 。
(2)探究温度对化学反应速率影响的实验编号是___ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是____ 。
II.水煤气变换CO(g) + H2O(g)⇌CO2(g) + H2(g)是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。已知T(大于100)℃时,将2molCO(g)和3molH2O(g)通入一容积固定为2L的密闭容器中,回答下列问题:
(1)反应进行到1min时测得CO的物质的量为1.8mol,则H2的平均反应速率为___ ,此时改变某一条件,能使H2的平均反应速率加快的是___ 。
A.恒容时充入氖气 B.升高温度 C.将体积缩小一半 D.恒温恒容,移走CO2
(2)已知在T℃时H2(g)+CoO(s) ⇌Co(s)+H2O(g) K1=1,CO(g)+CoO(s) ⇌Co(s)+CO2(g) K2=4,求T℃时,CO(g)+H2O(g) ⇌ CO2(g)+H2(g)的平衡常数为___ 。
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(2)探究温度对化学反应速率影响的实验编号是
II.水煤气变换CO(g) + H2O(g)⇌CO2(g) + H2(g)是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。已知T(大于100)℃时,将2molCO(g)和3molH2O(g)通入一容积固定为2L的密闭容器中,回答下列问题:
(1)反应进行到1min时测得CO的物质的量为1.8mol,则H2的平均反应速率为
A.恒容时充入氖气 B.升高温度 C.将体积缩小一半 D.恒温恒容,移走CO2
(2)已知在T℃时H2(g)+CoO(s) ⇌Co(s)+H2O(g) K1=1,CO(g)+CoO(s) ⇌Co(s)+CO2(g) K2=4,求T℃时,CO(g)+H2O(g) ⇌ CO2(g)+H2(g)的平衡常数为
您最近一年使用:0次
名校
7 . (1)某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
①本实验待测数据可以是_________________________ ,实验Ⅰ和实验Ⅱ可以探究__________ 对锌与稀硫酸反应速率的影响。
②实验Ⅲ和实验Ⅳ的目的是__________________________ ,写出有关反应的离子方程式________ 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中Vx=________ mL,理由是_________________ 。
| 序号 | 纯锌粉(g) | 2.0 mol·L-1 硫酸溶液(mL) | 温度(℃) | 硫酸铜固体(g) | 加入蒸馏水(mL) |
| Ⅰ | 2.0 | 50.0 | 25 | 0 | 0 |
| Ⅱ | 2.0 | 40.0 | 25 | 0 | 10.0 |
| Ⅲ | 2.0 | 50.0 | 25 | 0.2 | 0 |
| Ⅳ | 2.0 | 50.0 | 25 | 4.0 | 0 |
②实验Ⅲ和实验Ⅳ的目的是
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验 序号 | 体积V/mL | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
您最近一年使用:0次
2019-10-13更新
|
505次组卷
|
10卷引用:贵州省铜仁市贵州铜仁伟才学校2021-2022学年高二上学期期中考试化学试题
贵州省铜仁市贵州铜仁伟才学校2021-2022学年高二上学期期中考试化学试题广西宾阳县宾阳中学2019-2020学年高二9月月考化学试题广东省深圳市第二实验学校2020-2021学年高二上学期期中考试化学试题安徽省六安市城南中学2020-2021学年高二上学期期中考试化学试题第二章 第一节 化学反应速率 第2课时 影响化学反应速率的因素 活化能四川省广安市邻水县邻水实验学校2019-2020学年高一下学期第三次月考化学试题山东师范大学附属中学2020-2021学年高一下学期期中学分认定考试化学(等级考)试题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题(已下线)第七章 化学反应速率与化学平衡 热点强化13 控制变量探究影响化学反应速率的因素甘肃省张掖市某校2023-2024学年高三下学期模拟考试化学试题
名校
解题方法
8 . 在一定温度下,10mL 1.0mol/L H2SO4与Zn粒发生反应。不同时刻测定生成H2的体积(已折算为标准状况)如下表。
下列叙述不正确的是(溶液体积变化忽略不计)
| t/min | 0 | 1 | 3 | 5 | 7 | 9 |
| V(H2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)
| A.0~5 min的平均反应速率:v(H2SO4)≈0.02mol/(L•min) |
| B.5~9 min的平均反应速率:v(H2SO4)< 0.02mol/(L•min) |
| C.反应到5 min时,c(H2SO4)=0.010mol/L |
| D.反应到5 min时,Zn溶解了65mg |
您最近一年使用:0次
2019-01-24更新
|
324次组卷
|
2卷引用:【全国百强校】贵州省都匀市都匀第一中学2018-2019学年高二上学期期末考试化学试题
名校
9 . 下列实验装置(夹持装管略去)选择正确且能够达到实验目的的是
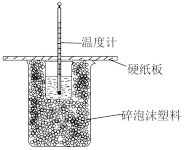 |  |  |  |
| A.测定中和热 | B.测定反应速率 | C.实现化学能转化为电能 | D.测定食醋浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-02-23更新
|
201次组卷
|
7卷引用:贵州省义龙新区2021-2022学年高二上学期期末联考化学试题
10 . 化学实验是进行化学研究的有效方法,请回答下列实验中的有关问题。
I.用如图所示的装置测定中和热。
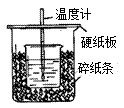
实验药品:100mL 0.50 mol‧L-1盐酸、100mL 0.55 mol‧L-1NaOH溶液。
实验步骤:略。
回答下列问题:
(1)从实验装置上看,还缺少环形玻璃搅拌棒,该装置的作用是____________ ;有同学提议可以用铜质搅拌棒替代,你是否赞同(说明理由)________________ 。
(2)你认为该实验成功的关键是______________________________ 。
II.影响化学反应速率的因素很多,某校课外兴趣小组用实验的方法进行探究。甲、乙两个兴趣小组利用Mg、Fe、Cu和不同浓度的硫酸(0.5 mol‧L-1、2 mol‧L-1、18.4 mol‧L-1),设计实验方案来研究影响反应速率的因素。
(1)请帮助甲小组完成研究的实验报告:
根据控制变量法,要得出正确的实验结论,在实验过程中需要保持温度和压强相同。
(2)乙小组为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。该小组选用的实验药品是:Fe、2mol‧L-1硫酸和______ mol‧L-1硫酸。

I.用如图所示的装置测定中和热。

实验药品:100mL 0.50 mol‧L-1盐酸、100mL 0.55 mol‧L-1NaOH溶液。
实验步骤:略。
回答下列问题:
(1)从实验装置上看,还缺少环形玻璃搅拌棒,该装置的作用是
(2)你认为该实验成功的关键是
II.影响化学反应速率的因素很多,某校课外兴趣小组用实验的方法进行探究。甲、乙两个兴趣小组利用Mg、Fe、Cu和不同浓度的硫酸(0.5 mol‧L-1、2 mol‧L-1、18.4 mol‧L-1),设计实验方案来研究影响反应速率的因素。
(1)请帮助甲小组完成研究的实验报告:
| 实 验 步 骤 | 现 象 | 结 论 |
| ①分别取等体积0.5 mol‧L-1硫酸于试管中 ②分别投入大小、形状相同的Mg、Fe、Cu ③观察金属表面产生气体的快慢 | ①产生气体的速率Mg>Fe ②Cu上无气体产生 |
根据控制变量法,要得出正确的实验结论,在实验过程中需要保持温度和压强相同。
(2)乙小组为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。该小组选用的实验药品是:Fe、2mol‧L-1硫酸和

您最近一年使用:0次



