名校
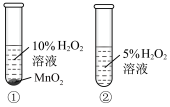
1 . 用下列仪器或装置进行相应实验,可以达到实验目的的是
|
|
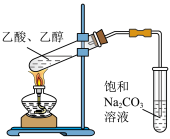
| A.证明MnO2是H2O2分解的催化剂 | B.制备并收集乙酸乙酯 |
|
|
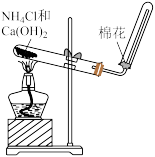
| C.收集NO2气体 | D.实验室制NH3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-12更新
|
370次组卷
|
4卷引用:吉林省“BEST合作体”2022-2023学年高一下学期期末联考化学试题
2 . 用下列仪器或装置(图中夹持略)进行相应实验,能达到实验目的的是
| A | B | C | D |
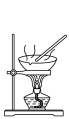 | 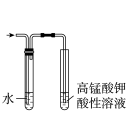 | 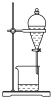 |  |
蒸发结晶制备 晶体 晶体 | 检验溴乙烷消去产物 | 分离苯和溴苯 | 探究不同催化剂 对  分解速率的影响 分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-18更新
|
657次组卷
|
6卷引用:吉林市第一中学2021-2022学年高三下学期4月教学质量检测理科综合化学试题
名校
解题方法
3 . 下列实验操作可以达到实验目的的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将1mL  溶液与1mL 溶液与1mL KI溶液混合,充分反应后分为两份,一份加2滴KSCN,另一份加2滴淀粉试液,观察现象 KI溶液混合,充分反应后分为两份,一份加2滴KSCN,另一份加2滴淀粉试液,观察现象 | 证明KI与 能反应且具有可逆性 能反应且具有可逆性 |
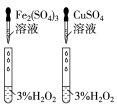
| B | 向两支盛有2mL5% 溶液的试管中分别加入 溶液的试管中分别加入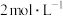 的 的 溶液和 溶液和 的 的 溶液,比较产生气泡速率 溶液,比较产生气泡速率 |  催化 催化 分解效果优于 分解效果优于 |
| C | 向饱和 溶液中通入某无色无味气体X,观察是否有沉淀生成 溶液中通入某无色无味气体X,观察是否有沉淀生成 | 确定X是否为 |
| D | 用pH计分别测定 和 和 的 的 溶液的pH,记录并比较pH变化 溶液的pH,记录并比较pH变化 | 随着溶液中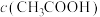 减小, 减小, 的电离程度增大 的电离程度增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列装置及设计不能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 | 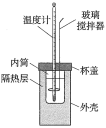 | 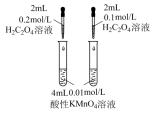 | 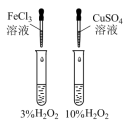 | 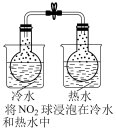 |
| 目的 | 测定中和反应的反应热 | 探究浓度对化学反应速率的影响 | 探究催化剂对 分解速率的影响 分解速率的影响 | 探究温度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-02-18更新
|
387次组卷
|
2卷引用:吉林省抚松县第一中学2021-2022学年高二上学期第三次月考化学试题
名校
5 . H2O2能缓慢分解生成水和氧气,但分解速率较慢,加入催化剂会加快分解速率。某化学兴趣小组为研究不同催化剂对H2O2分解反应的催化效果,设计了如图甲、乙、丙所示的三组实验。

(1)定性分析:可以通过观察甲装置的_____ 现象,而定性得出关于Fe3+和Cu2+催化效果的结论。有同学认为该实验不能比较Fe3+和Cu2+的催化效果,理由是_____ 。
(2)定量测定:用乙装置做对照试验,仪器A的名称是___ 。实验时组装好装置乙,关闭A的旋塞,将注射器活塞向外拉出一段距离后松开,观察活塞是否回到原来的位置。这一操作的实验目的是___ 。实验时以2min时间为准,需要测量的数据是____ 。(其它可能影响实验的因素均已忽略)
(3)定量分析:利用丙装置探究MnO2对H2O2分解的催化效果。将30mL5%H2O2溶液一次性加入盛有0.10molMnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]与时间(t/min)的关系如图所示。图中b点_______ 90mL(填“大于”、“小于”或“等于”)。

(4)补充实验:该小组补充进行了如下对比实验,实验药品及其用量如下表所示。实验设计的目的是为了探究______ 。

(1)定性分析:可以通过观察甲装置的
(2)定量测定:用乙装置做对照试验,仪器A的名称是
(3)定量分析:利用丙装置探究MnO2对H2O2分解的催化效果。将30mL5%H2O2溶液一次性加入盛有0.10molMnO2粉末的烧瓶中,测得标准状况下由量气管读出气体的体积[V(量气管)]与时间(t/min)的关系如图所示。图中b点

(4)补充实验:该小组补充进行了如下对比实验,实验药品及其用量如下表所示。实验设计的目的是为了探究
| 编号 | 反应物 | 催化剂 |
① | 30mL5%H2O2溶液,10滴H2O | 0.10molMnO2 |
② | 30mL5%H2O2溶液,10滴0.1mol/LHCl溶液 | 0.10molMnO2 |
③ | 30mL5%H2O2溶液,10滴0.1mol/LNaOH溶液 | 0.10molMnO2 |
您最近一年使用:0次
2021-01-27更新
|
979次组卷
|
5卷引用:吉林省长春市第五中学2021-2022学年高一下学期期末考试化学试题
吉林省长春市第五中学2021-2022学年高一下学期期末考试化学试题四川省遂宁市2020-2021学年高二上学期期末教学水平监测化学试题(已下线)第20讲 化学反应速率(精练)-2022年高考化学一轮复习讲练测四川省江油中学2020-2021学年高二下学期3月月考化学试题(已下线)第2章 化学反应速率与化学平衡(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)
名校
6 . 氨是最重要的氮肥,也是产量最大的化工产品之一。
Ⅰ.合成氨工艺是人工固氮的重要途径。
(1)可用作合成氨的催化剂有很多,如Os,Fe,Pt,Mn,Co等金属及相应的合金或化合物。该反应在LaCoSi催化作用的化学吸附及初步表面反应历程如图:

注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字单位:eV)其中,TS表示过渡态,*表示吸附态。
①请写出N2参与化学吸附的反应方程式:___ 。
②以上历程须克服的最大势垒为____ eV。
(2)在使用同一催化剂时,将2.0molN2和6.0molH2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2时n(H2)的变化(a点恰好达到平衡),曲线B表示T1时n(NH3)的变化。

①T2温度下反应进行到某时刻,测得容器内气体的压强为起始时的80%,则此时v(正)___ v(逆)(填“>”、“<”或“=”)。
②能否由图中数据得出温度T1>T2,并说明理由___ 。
Ⅱ.液氨是一种应用广泛的非水溶剂,以氨为原料可以合成很多重要化合物。
(3)Arrhenius提出:溶剂在液态下能自发发生电离,产生溶剂阳离子与溶剂阴离子的现象,称为自耦电离,如液态水的自耦电离方程式为:2H2O H3O++OH-。在液氨中也存在类似的自耦电离,试写出液氨中NH4Cl与NaNH2反应的离子方程式:
H3O++OH-。在液氨中也存在类似的自耦电离,试写出液氨中NH4Cl与NaNH2反应的离子方程式:____ 。
(4)如图是20℃时,NH3—CO2—H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。
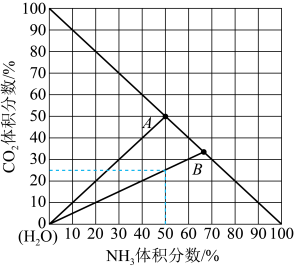
20℃时,可根据需要,选择水溶液体系反应得到(NH4)2CO3(aq)与NH4HCO3(aq),也可选择无水体系反应得到NH4COONH2(s)。
①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是___ (填“A—H2O”或“B—H2O”)。
②B点可得到的产品是____ (填化学式)。
Ⅰ.合成氨工艺是人工固氮的重要途径。
(1)可用作合成氨的催化剂有很多,如Os,Fe,Pt,Mn,Co等金属及相应的合金或化合物。该反应在LaCoSi催化作用的化学吸附及初步表面反应历程如图:

注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字单位:eV)其中,TS表示过渡态,*表示吸附态。
①请写出N2参与化学吸附的反应方程式:
②以上历程须克服的最大势垒为
(2)在使用同一催化剂时,将2.0molN2和6.0molH2通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2时n(H2)的变化(a点恰好达到平衡),曲线B表示T1时n(NH3)的变化。

①T2温度下反应进行到某时刻,测得容器内气体的压强为起始时的80%,则此时v(正)
②能否由图中数据得出温度T1>T2,并说明理由
Ⅱ.液氨是一种应用广泛的非水溶剂,以氨为原料可以合成很多重要化合物。
(3)Arrhenius提出:溶剂在液态下能自发发生电离,产生溶剂阳离子与溶剂阴离子的现象,称为自耦电离,如液态水的自耦电离方程式为:2H2O
 H3O++OH-。在液氨中也存在类似的自耦电离,试写出液氨中NH4Cl与NaNH2反应的离子方程式:
H3O++OH-。在液氨中也存在类似的自耦电离,试写出液氨中NH4Cl与NaNH2反应的离子方程式:(4)如图是20℃时,NH3—CO2—H2O三元体系相图。纵坐标代表CO2的体积分数,横坐标代表NH3的体积分数,坐标原点代表液态纯水。

20℃时,可根据需要,选择水溶液体系反应得到(NH4)2CO3(aq)与NH4HCO3(aq),也可选择无水体系反应得到NH4COONH2(s)。
①20℃时,利用NH3(g)、CO2(g)和H2O(l)制备NH4HCO3(aq)的最佳曲线是
②B点可得到的产品是
您最近一年使用:0次