名校
1 . 利用下列装置进行实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 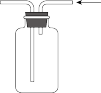 | 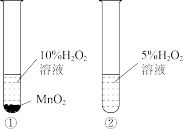 | 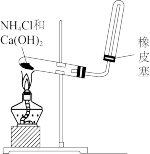 | 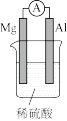 |
| 实验目的 | 收集NO | 探究催化剂对反应速率的影响 | 制备并收集 | 验证Mg比Al活泼 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-08更新
|
135次组卷
|
2卷引用:安徽省池州市2021-2022学年高一下学期期末联考化学试题
2 . 利用下列装置进行实验,能达到实验目的的是
| A | B | C | D |
 | 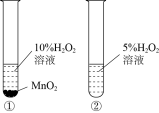 | 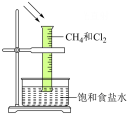 |  |
| 比较Mg、Al的活泼性 | 探究催化剂对反应速率的影响 | 验证甲烷与氯气在光照下发生化学反应 | 制备并收集乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-13更新
|
221次组卷
|
2卷引用:安徽名校2021-2022学年高一下学期阶段性测试(期末)化学试题
名校
3 . 乙醇催化氧化制取乙醛(沸点为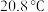 ,能与水互溶)的装置(夹持装置已略)如图所示。下列说法错误的是
,能与水互溶)的装置(夹持装置已略)如图所示。下列说法错误的是
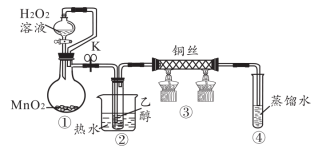
 ,能与水互溶)的装置(夹持装置已略)如图所示。下列说法错误的是
,能与水互溶)的装置(夹持装置已略)如图所示。下列说法错误的是
A.装置①制备 过程 过程 作为氧化剂 作为氧化剂 |
| B.装置②利用了乙醇的挥发性 |
| C.装置③的铜丝出现黑红交替现象 |
| D.装置④可以吸收未反应的乙醇和产物乙醛 |
您最近一年使用:0次
22-23高三上·吉林长春·期末
名校
解题方法
4 . 下列实验操作可以达到实验目的的是
| 选项 | 实验操作 | 实验目的或结论 |
| A | 将1mL  溶液与1mL 溶液与1mL KI溶液混合,充分反应后分为两份,一份加2滴KSCN,另一份加2滴淀粉试液,观察现象 KI溶液混合,充分反应后分为两份,一份加2滴KSCN,另一份加2滴淀粉试液,观察现象 | 证明KI与 能反应且具有可逆性 能反应且具有可逆性 |
| B | 向两支盛有2mL5% 溶液的试管中分别加入 溶液的试管中分别加入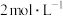 的 的 溶液和 溶液和 的 的 溶液,比较产生气泡速率 溶液,比较产生气泡速率 |  催化 催化 分解效果优于 分解效果优于 |
| C | 向饱和 溶液中通入某无色无味气体X,观察是否有沉淀生成 溶液中通入某无色无味气体X,观察是否有沉淀生成 | 确定X是否为 |
| D | 用pH计分别测定 和 和 的 的 溶液的pH,记录并比较pH变化 溶液的pH,记录并比较pH变化 | 随着溶液中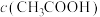 减小, 减小, 的电离程度增大 的电离程度增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列实验装置能达到实验目的的是
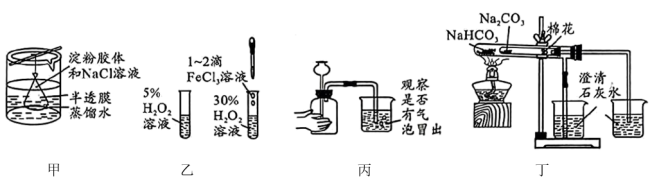
A.图甲装置可除去淀粉胶体中的 |
| B.图乙装置探究催化剂对化学反应速率的影响 |
| C.图丙装置检查装置的气密性 |
D.图丁装置可比较 和 和 的稳定性 的稳定性 |
您最近一年使用:0次
名校
6 . H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。
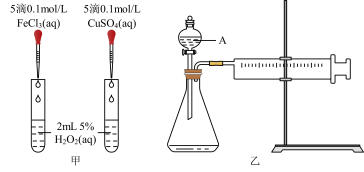
(1)若利用图甲装置,可通过观察__________ 现象,从而定性比较得出结论。
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是________ 。写出H2O2在二氧化锰催化作用下发生反应的化学方程式:___________ 。
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为________ ,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是________ 。
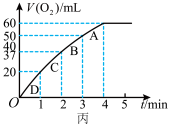
(4)将0.1molMnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释反应速率变化的原因:________ 。H2O2初始物质的量浓度为_______ (保留两位小数)。

(1)若利用图甲装置,可通过观察
(2)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
(3)若利用乙实验可进行定量分析,图乙中仪器A的名称为
(4)将0.1molMnO2粉末加入50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释反应速率变化的原因:

您最近一年使用:0次
2019-09-20更新
|
445次组卷
|
10卷引用:安徽省定远县育才学校2019-2020学年高一下学期期末考试化学试题
安徽省定远县育才学校2019-2020学年高一下学期期末考试化学试题云南省盈江县一中2019-2020学年高二上学期开学考试化学试题人教版高中化学必修二第二单元《化学反应与能量》测试卷2019-2020人教版高中化学必修2第二章《化学反应与能量》测试卷2020年人教版高中化学必修2第二章《化学反应与能量》测试卷12020年春季苏教版高中化学必修2专题二《化学反应与能量转化》测试卷(已下线)2.1.2 影响化学反应速率的因素(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)云南省普洱市第一中学2021-2022学年高一下学期3月份考试化学试题云南省石屏县第一中学2021-2022学年高一下学期3月份考试化学试题云南省广南县第一中学校2021-2022学年高一下学期3月份考试化学试题
名校
7 . 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
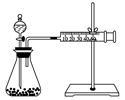
(1)该同学的实验目的是________________________ ;要得出正确的实验结论,还需控制的实验条件是________________________________________ 。
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用上图装置进行定量实验。完成该实验应选用的实验药品是____________________________ ;应该测定的实验数据是________________________________________________________________________ 。
实验二:已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在酸性高锰酸钾溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是________ 的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是________ 。
A.硫酸钾 B.硫酸锰
C.氯化锰 D.水
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol·L-1、2 mol·L-1、18.4 mol·L-1),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2 mol·L-1硫酸于试管中; ②分别投入大小、形状相同的Cu、Fe、Mg。 | 反应快慢:Mg>Fe>Cu | 反应物的性质越活泼,反应速率越快 |

(1)该同学的实验目的是
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用上图装置进行定量实验。完成该实验应选用的实验药品是
实验二:已知2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+8H2O+10CO2↑,在酸性高锰酸钾溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是
A.硫酸钾 B.硫酸锰
C.氯化锰 D.水
您最近一年使用:0次
2016-12-09更新
|
1012次组卷
|
6卷引用:安徽省合肥市第十一中学2020-2021学年高二上学期第一次月考化学试题
安徽省合肥市第十一中学2020-2021学年高二上学期第一次月考化学试题(已下线)2010-2011学年辽宁省师大附中高一下学期期中考试化学试卷(已下线)2011-2012学年湖北省武汉市五校高二上学期期中统考化学试卷(已下线)2012-2013学年新疆乌鲁木齐市一中高一(平行班)下学期期中考试化学试卷(已下线)2012年鲁科版高中化学选修6 2反应条件对化学反应的影响练习卷(已下线)2013届新疆乌鲁木齐市一中高一下学期平行班期中考试化学试卷
名校
8 . 硫酸、硝酸均为重要的化工产品,它们的制备工艺流程示意图如下:

回答下列问题。
(1)若上述过程为工业制硫酸。
①若原料A为黄铁矿(主要成分为FeS2)时,设备I中高温煅烧后会生成固体废渣,该废渣的一种用途是_______ 。
②气体B制备气体C可在V2O5催化下进行,该反应的机理分为两步:
第一步:V2O5+SO2=2VO2+SO3(快)
第二步:_______ (慢)
关于该过程,说法正确的是_______ (填标号)。
A.该过程的反应速率主要取决于第一步
B.VO2是该反应的催化剂
C.增大SO2的浓度可显著提高反应速率
D.增大O2的浓度可显著提高反应速率
(2)若上述过程为工业制硝酸,原料A为氨气。
①气体C在设备III中转化为硝酸时,还需要通入气体E,则气体E的化学式为_______ ,通入气体E的目的是_______ 。
②尾气中的NO2会形成光化学烟雾和酸雨,污染环境,可用碱性溶液吸收。已知NO2用碳酸钠溶液吸收时会生成NaNO2,则吸收NO2的离子方程式为_______ 。
(3)目前,NaClO溶液广泛应用于脱硫脱硝。
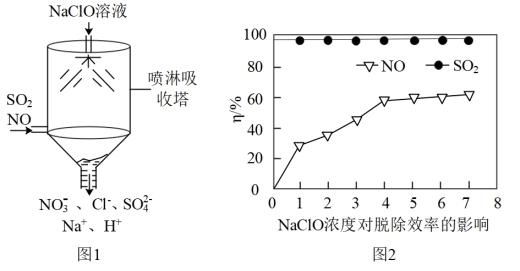
①某课外小组同学设计了如图喷淋吸收塔装置(如图1),设计该装置的优点是_______ 。
②如图2为NaClO浓度对脱硫脱硝效率(η/%)的影响。当温度为50°C,溶液的pH=10(溶液显碱性),c(SO2)=c(NO)=300mg·m-3时,SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因是_______ 。

回答下列问题。
(1)若上述过程为工业制硫酸。
①若原料A为黄铁矿(主要成分为FeS2)时,设备I中高温煅烧后会生成固体废渣,该废渣的一种用途是
②气体B制备气体C可在V2O5催化下进行,该反应的机理分为两步:
第一步:V2O5+SO2=2VO2+SO3(快)
第二步:
关于该过程,说法正确的是
A.该过程的反应速率主要取决于第一步
B.VO2是该反应的催化剂
C.增大SO2的浓度可显著提高反应速率
D.增大O2的浓度可显著提高反应速率
(2)若上述过程为工业制硝酸,原料A为氨气。
①气体C在设备III中转化为硝酸时,还需要通入气体E,则气体E的化学式为
②尾气中的NO2会形成光化学烟雾和酸雨,污染环境,可用碱性溶液吸收。已知NO2用碳酸钠溶液吸收时会生成NaNO2,则吸收NO2的离子方程式为
(3)目前,NaClO溶液广泛应用于脱硫脱硝。

①某课外小组同学设计了如图喷淋吸收塔装置(如图1),设计该装置的优点是
②如图2为NaClO浓度对脱硫脱硝效率(η/%)的影响。当温度为50°C,溶液的pH=10(溶液显碱性),c(SO2)=c(NO)=300mg·m-3时,SO2的脱除效率一直维持在98%以上,而NO脱除效率相对较低,其原因是
您最近一年使用:0次
2022-04-21更新
|
285次组卷
|
2卷引用:安徽省亳州市第二完全中学2022-2023学年高一下学期期末考试化学(A卷)试题



