名校
解题方法
1 . 在容积为2L的恒温密闭容器中,充入一定量的反应物发生化学后应,各物质(B为固体,其余物质均为气体)的含量随时间的变化如图所示,下列有关说法错误的是
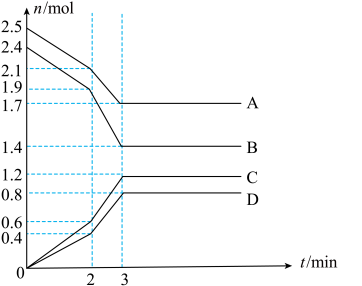

A.该反应的化学方程式为 |
| B.反应达到平衡状态时混合气体的压强与起始时的压强之比为37:25 |
| C.若反应条件不改变,则在2~3min发生该变化的原因可能为生成的产物充当了反应的催化剂 |
D. 时,反应达到平衡状态 时,反应达到平衡状态 |
您最近一年使用:0次
名校
解题方法
2 . 乙苯与 在光照条件下反应生成两种一氯取代物,反应过程中的能量变化如图所示。下列说法错误的是
在光照条件下反应生成两种一氯取代物,反应过程中的能量变化如图所示。下列说法错误的是
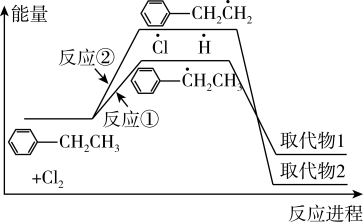
 在光照条件下反应生成两种一氯取代物,反应过程中的能量变化如图所示。下列说法错误的是
在光照条件下反应生成两种一氯取代物,反应过程中的能量变化如图所示。下列说法错误的是
A.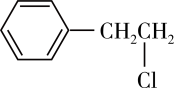 比 比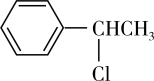 稳定 稳定 |
| B.反应①比反应②的速率快 |
| C.选择合适催化剂可提高单位时间内取代物2的含量 |
| D.若升温时取代物2的含量提高,则原因是反应②平衡正向移动 |
您最近一年使用:0次
2022-01-25更新
|
600次组卷
|
5卷引用:湖南省衡阳市第八中学2022-2023学年高二下学期第二次月考化学试题
湖南省衡阳市第八中学2022-2023学年高二下学期第二次月考化学试题山东省威海市2021-2022学年高三上学期期末考试化学试题河南省豫北名校2021-2022学年高二下学期4月份教学质量检测化学试题(已下线)【直击双一流】03-备战2022年高考化学名校进阶模拟卷(通用版)上海市南洋模范中学2022届高三等级考模拟训练七化学试题
3 . 亚硝酰硫酸(NOSO4H)是一种浅黄色液体,遇水易分解,溶于浓硫酸,主要用于染料、医药领域的重氮化反应。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品中杂质硝酸的含量。
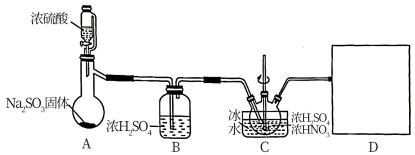
回答下列问题:
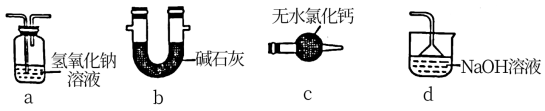
(1)装置A中盛装Na2SO3固体的仪器名称是_______ ,装置D最好选用_______ (填序号)。
(2)装置C中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①装置C中温度过高产率降低的原因是_______ 。
②开始通SO2时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是_______ 。
(3)测定亚硝酰硫酸产品中杂质硝酸的含量。
称取1.400g产品放入250mL锥形瓶中,加80mL浓硫酸,用
 标准溶液滴定,消耗标准溶液20.00mL。
标准溶液滴定,消耗标准溶液20.00mL。
已知: 可与NO生成粉红色的FeSO4·NO。
可与NO生成粉红色的FeSO4·NO。
①锥形瓶中加入浓硫酸的作用是_______ 。
②判断滴定达到终点的现象是_______ 。
③亚硝酰硫酸中硝酸的含量为_______ 。

回答下列问题:
(1)装置A中盛装Na2SO3固体的仪器名称是

(2)装置C中浓HNO3与SO2在浓H2SO4作用下反应制得NOSO4H。
①装置C中温度过高产率降低的原因是
②开始通SO2时,反应缓慢,待生成少量NOSO4H后,温度变化不大,但反应速率明显加快,其原因是
(3)测定亚硝酰硫酸产品中杂质硝酸的含量。
称取1.400g产品放入250mL锥形瓶中,加80mL浓硫酸,用

 标准溶液滴定,消耗标准溶液20.00mL。
标准溶液滴定,消耗标准溶液20.00mL。已知:
 可与NO生成粉红色的FeSO4·NO。
可与NO生成粉红色的FeSO4·NO。①锥形瓶中加入浓硫酸的作用是
②判断滴定达到终点的现象是
③亚硝酰硫酸中硝酸的含量为
您最近一年使用:0次
2021-05-28更新
|
624次组卷
|
3卷引用:湖南省长沙市第一中学2023-2024学年高三上学期月考卷(四)化学试题
4 . 2020年11月7日是“中国稀土之父”徐光宪先生诞辰100周年纪念日。金属铈( )是地壳中含量最高的稀土元素。关于铈的有关化合物及H2O2的转化关系如图所示,下列说法错误的是
)是地壳中含量最高的稀土元素。关于铈的有关化合物及H2O2的转化关系如图所示,下列说法错误的是
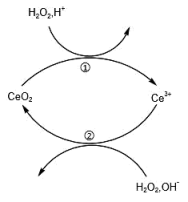
 )是地壳中含量最高的稀土元素。关于铈的有关化合物及H2O2的转化关系如图所示,下列说法错误的是
)是地壳中含量最高的稀土元素。关于铈的有关化合物及H2O2的转化关系如图所示,下列说法错误的是
| A.CeO2是整个转化过程中的催化剂 |
B.过程①的离子方程式: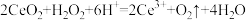 |
| C.该反应历程的总反应为:2H2O2=2H2O+O2↑ |
| D.氧化性:CeO2>H2O2 |
您最近一年使用:0次
2021-11-08更新
|
309次组卷
|
5卷引用:湖南省醴陵市第一中学2023届高三下学期第七次月考化学试题



