解题方法
1 . 研究催化剂对2NH3 N2+3H2反应速率的影响。恒温、恒容时,c(NH3)随时间的变化如表。
N2+3H2反应速率的影响。恒温、恒容时,c(NH3)随时间的变化如表。
下列说法不正确的是
 N2+3H2反应速率的影响。恒温、恒容时,c(NH3)随时间的变化如表。
N2+3H2反应速率的影响。恒温、恒容时,c(NH3)随时间的变化如表。| 时间/min c(NH3)/(×10-3mol•L-1) 催化剂 | 0 | 20 | 40 | 60 | 80 |
| 催化剂I | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| 催化剂II | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
| A.使用催化剂I,0~20min的平均反应速率v(N2)=1.00×10-5mol·L-1·min-1 |
B.使用催化剂Ⅱ,达平衡后容器内的压强是初始时的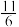 倍 倍 |
| C.相同条件下,使用催化剂Ⅱ可使该反应更快 |
| D.相同条件下,使用催化剂Ⅱ可使该反应的化学平衡常数更大 |
您最近一年使用:0次



