名校
1 . 利用CO2合成二甲醚的原理为2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ∆H,其中投料比
CH3OCH3(g)+3H2O(g) ∆H,其中投料比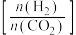 (取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示
(取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示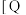 点c(CO2)= 0.2mol·L-1。下列说法正确的是
点c(CO2)= 0.2mol·L-1。下列说法正确的是
 CH3OCH3(g)+3H2O(g) ∆H,其中投料比
CH3OCH3(g)+3H2O(g) ∆H,其中投料比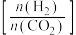 (取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示
(取值为2、3、4)和温度与CO2的平衡转化率的关系如图所示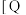 点c(CO2)= 0.2mol·L-1。下列说法正确的是
点c(CO2)= 0.2mol·L-1。下列说法正确的是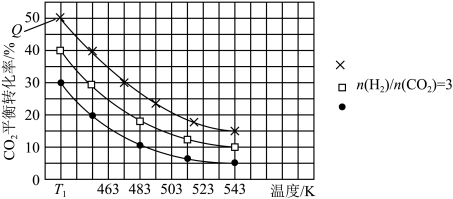
| A.T1K时,Kc=0.0675 | B.△H>0 |
C.X表示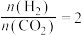 | D.催化剂可以改变CO2的平衡转化率 |
您最近半年使用:0次
名校
2 . 科学家提出在排气管内设置催化剂,使污染气体(CO、NO)转化为大气成分后再排出(反应过程如图)。下列说法错误的是


| A.NO可用排水法收集 |
| B.将燃油净化后使用,可减少NO的排放 |
| C.使用合适的催化剂能加快反应②的速率 |
D.反应②的化学方程式为 |
您最近半年使用:0次
名校
解题方法
3 . 某科研人员提出HCHO与 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
A.HAP降低了该反应的焓变( ) ) |
| B.反应过程中,发生了非极性键的断裂和生成 |
C.HCHO在反应过程中,无 键发生断裂 键发生断裂 |
D. 和 和 的中心原子上所含孤电子对数不同 的中心原子上所含孤电子对数不同 |
您最近半年使用:0次
7日内更新
|
265次组卷
|
4卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
4 . 中国提出二氧化碳排放在2030年前达到峰值,2060年前实现碳中和。这体现了中国作为全球负责任大国的环境承诺和行动决心。二氧化碳选择性加氢制甲醇是解决温室效应、发展绿色能源和实现经济可持续发展的重要途径之一、常温常压下利用铜基催化剂实现二氧化碳选择性加氢制甲醇的反应机理和能量变化图如下(其中吸附在催化剂表面上的粒子用*标注),下列说法错误的是
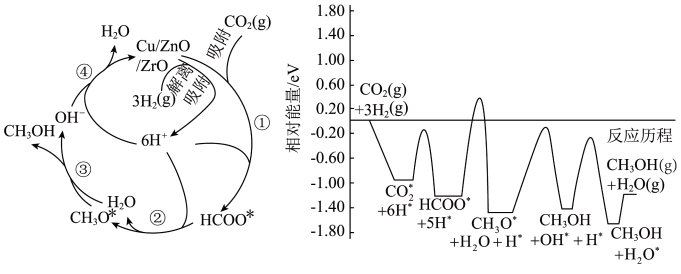
| A.二氧化碳选择性加氢制甲醇是放热反应 |
| B.催化剂能改变反应机理,加快反应速率,降低反应热 |
| C.总反应为CO2(g)+3H2(g)=CH3OH(g)+H2O(g) |
| D.该历程的决速步为HCOO*+4H*=CH3O*+H2O |
您最近半年使用:0次
名校
解题方法
5 . N2H4是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某Ru(Ⅱ)催化剂用[L-Ru-NH3]+表示|能高效电催化氧化NH3合成N2H4,其反应机理如图所示(图中L为原子团)。下列说法错误的是
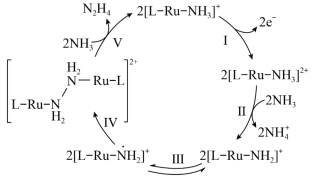
| A.[L-Ru-NH3]2+中Ru的化合价为+3 |
| B.反应Ⅳ中有非极性键的断裂与形成 |
| C.电催化氧化NH3合成N2H4发生在电解池阳极区 |
| D.N2H4与NH3中 N 原子的 VSEPR 模型均为四面体形 |
您最近半年使用:0次
7日内更新
|
337次组卷
|
4卷引用:安徽省示范高中皖北协作区2024届高三联考化学试题
安徽省示范高中皖北协作区2024届高三联考化学试题江西省南昌十九中2023-2024学年高三下学期第一次模拟考试化学试卷 河南省郑州市宇华实验学校2024届高三下学期第三次模拟考试化学试题(已下线)通关练07 原子、分子、晶体结构再归纳-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
解题方法
6 . 甲醇用途广泛,可用作溶剂、防冻剂、燃料,也可用于生产生物柴油,利用合成气(主要成分为CO、CO2和H2)可以合成甲醇,涉及的反应如下,回答下列问题:
反应ⅰ:CO(g)+2H2(g) CH3OH(g) △H1=−91.5kJ∙mol−1
CH3OH(g) △H1=−91.5kJ∙mol−1
反应ii:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2=−49.9kJ∙mol−1
CH3OH(g)+H2O(g) △H2=−49.9kJ∙mol−1
反应iii:CO2(g)+H2(g) CO(g)+H2O(g) △H3=+41.6kJ∙mol−1
CO(g)+H2O(g) △H3=+41.6kJ∙mol−1
(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):___________ 。
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式___________ 。
③m=___________ (计算结果保留两位有效数字,已知1eV=1.6×10−22kJ)。
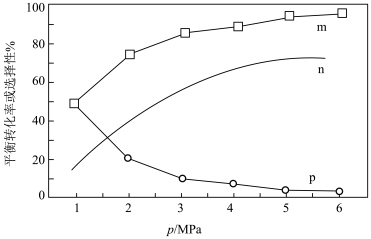
(2)反应ⅰ的Arrhenius经验公式Rlnk=− +C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是
+C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是___________ 。 和CO的选择性
和CO的选择性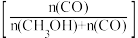 随压强变化曲线如图所示。
随压强变化曲线如图所示。___________ (填“m”“n”或“p”),简述判断方法___________ 。___________ mol·L−1·s−1(保留两位有效数字)。
反应ⅰ:CO(g)+2H2(g)
 CH3OH(g) △H1=−91.5kJ∙mol−1
CH3OH(g) △H1=−91.5kJ∙mol−1反应ii:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H2=−49.9kJ∙mol−1
CH3OH(g)+H2O(g) △H2=−49.9kJ∙mol−1反应iii:CO2(g)+H2(g)
 CO(g)+H2O(g) △H3=+41.6kJ∙mol−1
CO(g)+H2O(g) △H3=+41.6kJ∙mol−1(1)在某催化剂作用下,反应ⅰ的反应历程如图所示(图中数据表示微粒数目以及微粒的相对总能量,*表示吸附在催化剂上):
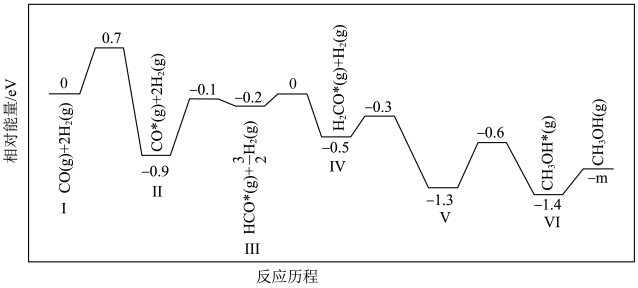
②结合反应历程,写出反应ⅰ中生成甲醇的决速步骤的反应方程式
③m=
(2)反应ⅰ的Arrhenius经验公式Rlnk=−
 +C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是
+C(Ea为活化能,k为速率常数,R和C均为常数,T为温度),实验数据如图中曲线M所示。当改变外界条件时,实验数据如图中曲线N所示,则实验可能改变的外界条件是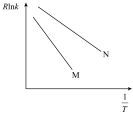
 和CO的选择性
和CO的选择性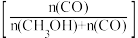 随压强变化曲线如图所示。
随压强变化曲线如图所示。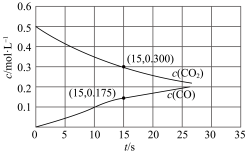
您最近半年使用:0次
名校
解题方法
7 .  (可表示为
(可表示为 )催化剂的催化原理如下图所示(
)催化剂的催化原理如下图所示( 为烃基)。
为烃基)。
 (可表示为
(可表示为 )催化剂的催化原理如下图所示(
)催化剂的催化原理如下图所示( 为烃基)。
为烃基)。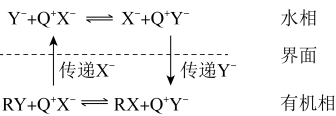
A.总反应为: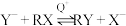 | B.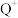 易溶于水相而难溶于有机相 易溶于水相而难溶于有机相 |
C.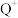 与 与 、 、 之间的离子键强度要适中 之间的离子键强度要适中 | D.PTC催化剂可用作相转移催化剂 |
您最近半年使用:0次
7日内更新
|
267次组卷
|
2卷引用:湖北省圆创联盟2024届高三三月联合测评(一模)化学试卷
名校
解题方法
8 . 碳酸二甲酯(DMC)具有优良的化学反应性能。在众多研究方向中,CO2和甲醇直接合成DMC的方法受到了较多的关注,M2O(OH)催化该反应的一种反应机理如图所示。下列叙述正确的是
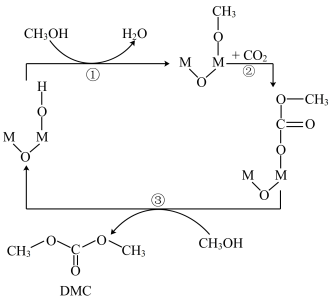
| A.H2O是反应中间体 |
| B.反应①②③均为取代反应 |
| C.DMC中共平面的原子数最多为4个 |
| D.DMC的同分异构体中同时含有酯基和羟基的物质有4种(不考虑立体异构) |
您最近半年使用:0次
名校
解题方法
9 . 过二硫酸钠(Na2S2O8)是白色晶状粉末,易溶于水,不溶于乙醇,加热至65℃就会发生分解,常用作漂白剂,金属表面处理剂等。实验室以过氧化氢、浓硫酸和碳酸钠为原料制备过二硫酸钠。
I.过一硫酸(H2SO5)的合成
原理:H2O2+H2SO4=H2SO5+H2O。________ 。
(2)水槽中盛放的试剂C是________ (填“冰水”或“热水”)。
Ⅱ.过二硫酸钠(Na2S2O8)的合成
取下球形冷凝管A,在适当搅拌的条件下,沿瓶口a向仪器B中加入一定量的无水碳酸钠,控制加入速度,并控制反应温度在60℃左右,待碳酸钠完全溶解后继续恒温搅拌20min使之反应完全,这个过程中瓶口a不能封闭。
(3)合成反应分两步完成:________ ,2Na2SO4+H2SO5=2Na2S2O8+H2O。
(4)反应完毕,将仪器B中的溶液减压浓缩;结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是_________________ 。
(5)1mol Na2S2O8中存在的-O-O-数目为________ 。
(6)Na2S2O8具有强氧化性,可将I-氧化为I2: +2I-=2
+2I-=2 +I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:
+I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:_____________ 、__________ 。
(7)取适量过二硫酸钠,装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D,实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。取硬质玻璃管少量残留固体于试管中,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。写出A装置中发生反应的化学方程式:____________ 。
I.过一硫酸(H2SO5)的合成
原理:H2O2+H2SO4=H2SO5+H2O。
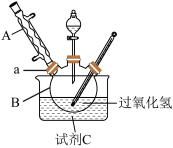
(2)水槽中盛放的试剂C是
Ⅱ.过二硫酸钠(Na2S2O8)的合成
取下球形冷凝管A,在适当搅拌的条件下,沿瓶口a向仪器B中加入一定量的无水碳酸钠,控制加入速度,并控制反应温度在60℃左右,待碳酸钠完全溶解后继续恒温搅拌20min使之反应完全,这个过程中瓶口a不能封闭。
(3)合成反应分两步完成:
(4)反应完毕,将仪器B中的溶液减压浓缩;结晶过滤、洗涤干燥,可得过硫酸钠,减压浓缩的原因是
(5)1mol Na2S2O8中存在的-O-O-数目为
(6)Na2S2O8具有强氧化性,可将I-氧化为I2:
 +2I-=2
+2I-=2 +I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:
+I2↓,可用Fe2+作催化剂改变上述反应途径。试用离子方程式表示Fe2+对上述反应催化的历程:(7)取适量过二硫酸钠,装入硬质玻璃管中,加热,将分解产物依次通过装置B、C、D,实验中发现B中U形管内产生无色液体,接着无色液体慢慢变成固体,C中溶液颜色无明显变化,D中溶液逐渐变蓝色。取硬质玻璃管少量残留固体于试管中,加入蒸馏水,溶解后滴加BaCl2溶液和盐酸,产生白色沉淀。写出A装置中发生反应的化学方程式:

您最近半年使用:0次
名校
10 . 硅铝酸盐沸石离子交换分子筛M-ZSM-5(M为Fe、Co、Ni、Cu)催化N2O氧化CH4制甲醇的反应机理如图所示,下列说法错误的是
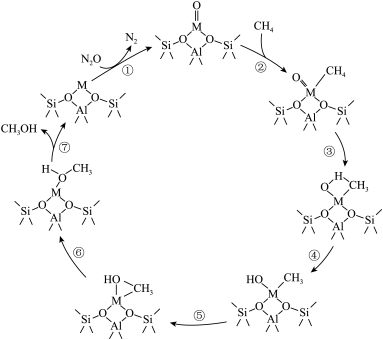
A.反应②的原子利用率为 |
B.反应①、②、③、⑥、⑦中, 的化合价发生了改变 的化合价发生了改变 |
C.M-ZSM-5能降低 氧化 氧化 制甲醇反应的活化能,改变反应的 制甲醇反应的活化能,改变反应的 |
D.总反应为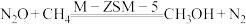 |
您最近半年使用:0次



