解题方法
1 . 采用可再生的生物质原料生产乙醇,再脱水制乙烯的技术是调整能源结构、减少环境污染、促进国民经济的重要途径之一、一定温度下,在某密闭容器中进行乙醇脱水制乙烯的反应: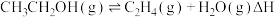 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
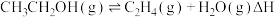 ,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是
,有、无催化剂时,该反应的能量变化与反应进程如图所示,下列说法错误的是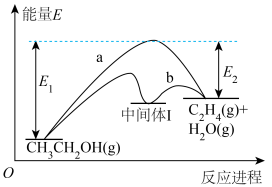
A.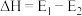 |
B.在 路径中,乙醇 路径中,乙醇 中间体Ⅰ为反应的决速步骤 中间体Ⅰ为反应的决速步骤 |
C.b路径的反应速率大于 路径的 路径的 |
D.反应达到平衡后, 路径中 路径中 的产率比 的产率比 路径的高 路径的高 |
您最近半年使用:0次
名校
2 . 氮及其化合物在生产生活中有广泛的应用,按要求回答下列问题:
I.氨气是重要的化工原料,回答下列问题:
(1)实验室制取 的化学方程式为
的化学方程式为___________ 。
(2)1909年化学家哈伯在实验室首次用单质合成了氨。2007年化学家格哈德埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。用 、
、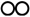 、
、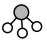 分别表示
分别表示 ,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
II.氮氧化物是造成环境污染的主要原因之一,消除氮氧化物有多种方法。
(3)某学习小组设计如图装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下, 两电极产生气体的体积比为
两电极产生气体的体积比为___________ , 电极的电极反应方程式为
电极的电极反应方程式为___________ 。
I.氨气是重要的化工原料,回答下列问题:
(1)实验室制取
 的化学方程式为
的化学方程式为(2)1909年化学家哈伯在实验室首次用单质合成了氨。2007年化学家格哈德埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。用
 、
、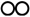 、
、 分别表示
分别表示 ,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。
,观察如图,判断符合在催化剂表面合成氨反应过程的顺序为___________。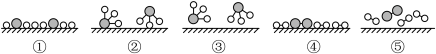
| A.②③④①⑤ | B.③②①④⑤ | C.③②④①⑤ | D.⑤④①②③ |
II.氮氧化物是造成环境污染的主要原因之一,消除氮氧化物有多种方法。
(3)某学习小组设计如图装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下,
 两电极产生气体的体积比为
两电极产生气体的体积比为 电极的电极反应方程式为
电极的电极反应方程式为
您最近半年使用:0次
名校
3 . 图中展示的是乙烯催化氧化的过程(部分相关离子未画出),下列描述正确的是
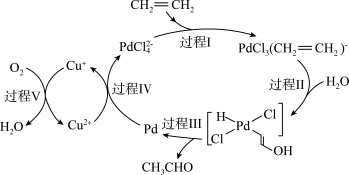
A.乙烯催化氧化反应的化学方程式为 |
B.反应中只有 作催化剂 作催化剂 |
| C.该转化过程中,没有极性键的断裂与形成 |
D.该转化过程中,涉及反应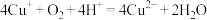 |
您最近半年使用:0次
2024-04-10更新
|
236次组卷
|
2卷引用:广东省深圳市福田区福田中学2023-2024学年高三下学期开学考试化学试题
名校
解题方法
4 . 下列说法正确的是
| A.在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 |
| B.NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57 kJ•mol-1,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
| C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据 |
| D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
您最近半年使用:0次
名校
解题方法
5 . 利用含碳化合物合成燃料是解决能源危机的重要方法,已知CO(g)+2H2(g) CH3OH(g)反应过程中的 能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是
CH3OH(g)反应过程中的 能量变化情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况。下列判断正确的是

| A.该反应的ΔH=+91 kJ·mol-1 |
| B.加入催化剂,该反应的ΔH变小 |
| C.如果该反应生成液态CH3OH,则ΔH增大 |
| D.反应物的总能量大于生成物的总能量 |
您最近半年使用:0次
解题方法
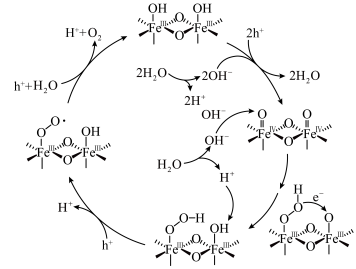
6 . 光阳极表面修饰的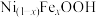 电催化剂可显著降低水氧化半反应的反应能垒,在
电催化剂可显著降低水氧化半反应的反应能垒,在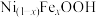 电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去;
电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去; 代表空穴,具有强氧化性)。下列说法错误的是
代表空穴,具有强氧化性)。下列说法错误的是
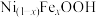 电催化剂可显著降低水氧化半反应的反应能垒,在
电催化剂可显著降低水氧化半反应的反应能垒,在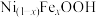 电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去;
电催化剂作用下光电催化水氧化过程中的质子耦合电荷转移路径如图(Ni已略去; 代表空穴,具有强氧化性)。下列说法错误的是
代表空穴,具有强氧化性)。下列说法错误的是
| A.上述路径中涉及极性共价键的断裂和形成 |
B.上述路径中 元素与 元素与 元素均体现出两种化合价 元素均体现出两种化合价 |
C.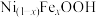 电催化剂中的铁元素位于第Ⅷ族 电催化剂中的铁元素位于第Ⅷ族 |
D.图示光电催化水氧化半反应可表示为 |
您最近半年使用:0次
名校
7 . 可逆反应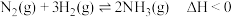 ,对示意图的解释与图像相符的是
,对示意图的解释与图像相符的是
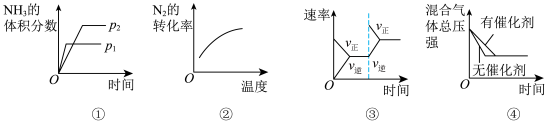
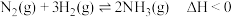 ,对示意图的解释与图像相符的是
,对示意图的解释与图像相符的是
A.①压强对反应的影响 | B.③平衡体系增加 对反应的影响 对反应的影响 |
| C.②温度对反应的影响 | D.④催化剂对反应的影响 |
您最近半年使用:0次
名校
8 . 对于可逆反应
 ,下列研究目的和示意图相符的是
,下列研究目的和示意图相符的是

 ,下列研究目的和示意图相符的是
,下列研究目的和示意图相符的是| A | B | C | D |
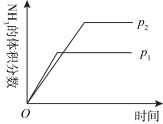 | 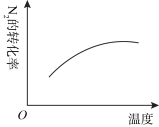 | 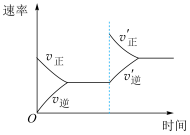 |  |
研究压强对反应的影响( ) ) | 研究温度对反应的影响 | 研究平衡体系增加 对反应的影响 对反应的影响 | 研究催化剂对反应的影响 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
9 . NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现,在催化剂上可能发生的反应过程如图2所示。下列说法正确的是
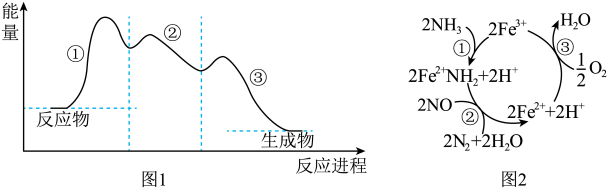

| A.Fe2+为该反应的催化剂 |
| B.过程①中NH3断裂非极性键 |
| C.图2充入过量的O2不利于NO转化为N2 |
D.图2脱硝的总反应为 |
您最近半年使用:0次
名校
10 . 盐酸羟胺 是一种常见的还原剂和显像剂,其结构和性质类似
是一种常见的还原剂和显像剂,其结构和性质类似 。工业上利用电化学方法制备盐酸羟胺时,Fe电极的反应机理如图所示。
。工业上利用电化学方法制备盐酸羟胺时,Fe电极的反应机理如图所示。
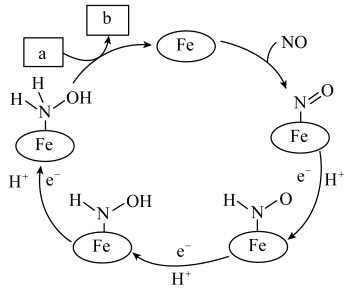
下列说法错误的是
 是一种常见的还原剂和显像剂,其结构和性质类似
是一种常见的还原剂和显像剂,其结构和性质类似 。工业上利用电化学方法制备盐酸羟胺时,Fe电极的反应机理如图所示。
。工业上利用电化学方法制备盐酸羟胺时,Fe电极的反应机理如图所示。
下列说法错误的是
| A.Fe起催化和导电作用 |
B.a为 和 和 ,b为 ,b为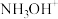 |
| C.反应过程中有极性键的断裂和生成 |
D.该电极反应为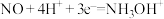 |
您最近半年使用:0次



