1 . 室温下,探究0.1 mol·L-1 FeCl3溶液的性质,下列实验方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向两支试管中分别加入5 mL 5%的H2O2溶液,再向两支试管中滴入3滴浓度均为0.1 mol·L-1 的FeCl3和CuSO4,观察产生气体的速率 | 比较Fe3+和Cu2+的催化效率 |
| B | 向2 mL 0.1 mol·L-1 FeCl3溶液中加入1 mL 0.1 mol·L-1 KI溶液,充分振荡后滴加KSCN溶液,观察颜色变化 | 2Fe3++2I-=2Fe2++I2是否为可逆反应 |
| C | 向苯酚溶液中滴加几滴0.1 mol·L-1 FeCl3溶液,溶液呈紫色 | FeCl3与苯酚发生了氧化还原反应 |
| D | 将5 mL 0.1 mol·L-1 FeCl3溶液和15 mL 0.1 mol·L-1 NaHCO3溶液混合,生成红褐色沉淀和气体 | Fe3+与 发生了双水解反应 发生了双水解反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
2 . 氰化氢(HCN,一元弱酸,易挥发)主要应用于电镀、采矿、药物合成等工业生产。HCN,CN-能抑制人体组织细胞内酶的活性,不能直接排放到环境中。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,___________ 。
(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是___________ 。
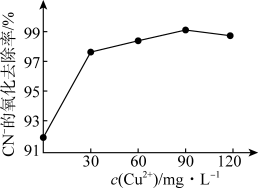
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是___________ 。 ,其反应的离子方程式为
,其反应的离子方程式为___________ 。
(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g) NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0
除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是___________ 。
(1)Na2S2O3在临床上常用于氰化物的解毒剂。解毒的原理是
 将CN-转化为SCN-和
将CN-转化为SCN-和 。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,
。验证该转化过程中生成SCN-的实验方法是:向NaCN溶液中加入过量的Na2S2O3的溶液,充分反应后,取少量反应后的溶液于试管中,加入足量稀盐酸酸化,(2)Cu2+可催化过氧化氢氧化废水中的CN-。
①反应不能在酸性条件下进行,原因是
②在含氰废水总景、过氧化氢用量和溶液pH一定的情况下,反应相同时间,测得CN-的氧化去除率随c(Cu2+)的变化与如图所示。c(Cu2+)超过90mg·L-1时,CN-的氧化去除率有所下降,原因是
 ,其反应的离子方程式为
,其反应的离子方程式为(4)在铜镍为催化剂(Cu、CuO为活性组分,Cu的催化活性效果更好)的条件下,可利用反应:HCN(g)+H2O(g)
 NH3(g)+CO(g) △H>0
NH3(g)+CO(g) △H>0除去废气中的HCN。将含相同比例的HCN(g)、H2O(g)、CO(g)[或N2(g)]混合气体分别通过催化剂,反应相同的时间,测得HCN(g)的去除率随温度变化如图所示。200℃时含CO的混合气体中HCN(g)的去除率较高,而400℃时含CO的混合气体中HCN(g)的去除率较低。其原因是

您最近半年使用:0次
名校
3 . 反应2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
 CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是
CH3OCH3(g)+3H2O(g);△H<0可实现CO2的资源化,下列说法正确的是| A.上述反应在任何温度下均可自发进行 |
| B.上述反应反应物的总能量大于生成物的总能量 |
C.上述反应平衡常数K=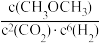 |
| D.上述反应达到平衡后,加入催化剂,平衡正向移动 |
您最近半年使用:0次
名校
解题方法
4 . CI4分)某化学小组欲测定酸性条件下 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为
溶液反应的化学反应速率,所用试剂为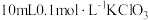 溶液和
溶液和 溶液,所得溶液中
溶液,所得溶液中 的浓度
的浓度 随时间变化的曲线如图1和
随时间变化的曲线如图1和 的速率
的速率 随时间的变化关系如图2:
随时间的变化关系如图2:_____ 。
 (已配平)
(已配平)
(2)根据实验数据可知,该反应在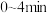 的平均反应速率
的平均反应速率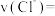
_____ 。
(3)下列说法正确的是_____
A.若纵坐标为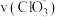 的
的 曲线与图2中的曲线不能重合
曲线与图2中的曲线不能重合
B.图中阴影部分的面积表示 时间内
时间内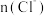 的增大
的增大
C.后期反应速率下降的主要原因是反应物浓度减少
(4)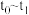 段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
已知: 对该反应无影响;
对该反应无影响;
可供选择的试剂有:A. 固体 B.
固体 B. 固体C.
固体C. D.
D.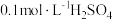 E.
E.
①方案I中所选试剂_____ ,方案Ⅱ中所选试剂_____ 。
②方案Ⅱ烧杯①中加入 水的作用是
水的作用是_____ 。
③除方案I和方案Ⅱ外,请再提出一种可能加快化学反应速率的假设_____ 。
 溶液与
溶液与 溶液反应的化学反应速率,所用试剂为
溶液反应的化学反应速率,所用试剂为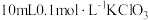 溶液和
溶液和 溶液,所得溶液中
溶液,所得溶液中 的浓度
的浓度 随时间变化的曲线如图1和
随时间变化的曲线如图1和 的速率
的速率 随时间的变化关系如图2:
随时间的变化关系如图2: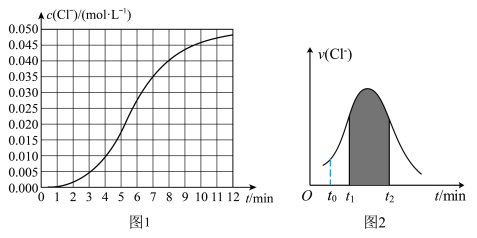
 (已配平)
(已配平)(2)根据实验数据可知,该反应在
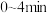 的平均反应速率
的平均反应速率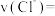
(3)下列说法正确的是
A.若纵坐标为
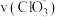 的
的 曲线与图2中的曲线不能重合
曲线与图2中的曲线不能重合B.图中阴影部分的面积表示
 时间内
时间内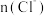 的增大
的增大C.后期反应速率下降的主要原因是反应物浓度减少
(4)
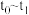 段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:
段该反应速率增大,为探究可能的原因,设计如下方案探究影响化学反应速率的因素:已知:
 对该反应无影响;
对该反应无影响;可供选择的试剂有:A.
 固体 B.
固体 B. 固体C.
固体C. D.
D.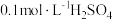 E.
E.
| 方案 | 假设 | 数据处理 | 具体实验操作 |
| I | 反应产物 对反应有催化作用,加快了化学反应速率 对反应有催化作用,加快了化学反应速率 | 取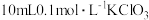 溶液于烧杯中,先加入_____(填字母),再加入 溶液于烧杯中,先加入_____(填字母),再加入 溶液。 溶液。 | 绘制溶液中 浓度 浓度 随时间变化的曲线与图1对比 随时间变化的曲线与图1对比 |
| Ⅱ | 反应中溶液酸性增强,加快了化学反应速率 | 分别向两个烧杯中加入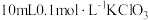 溶液。 溶液。烧杯①:加入  水: 水:烧杯②:加入  _____(填字母)。 _____(填字母)。再分别向两个烧杯中加入  溶液。 溶液。 |
②方案Ⅱ烧杯①中加入
 水的作用是
水的作用是③除方案I和方案Ⅱ外,请再提出一种可能加快化学反应速率的假设
您最近半年使用:0次
名校
5 . CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO−,其离子方程式为_______ ;其他条件不变, 转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,
转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内, 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是_______ 。_______ ;放电过程中需补充的物质A为_______ (填化学式)。
②图中所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为_______ 。
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。_______ (填化学式)。
②研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是提高释放氢气的速率,提高释放出氢气的纯度,请分析原因_______ 。
(1)CO2催化加氢。在密闭容器中,向含有催化剂的KHCO3溶液(CO2与KOH溶液反应制得)中通入H2生成HCOO−,其离子方程式为
 转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内,
转化为HCOO−的转化率随温度的变化如图所示。反应温度在40℃~80℃范围内, 催化加氢的转化率迅速上升,其主要原因是
催化加氢的转化率迅速上升,其主要原因是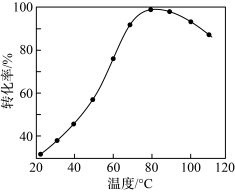
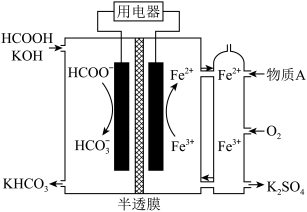
②图中所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为
(3)HCOOH催化释氢。在催化剂作用下,HCOOH分解生成CO2和H2可能的反应机理如图所示。
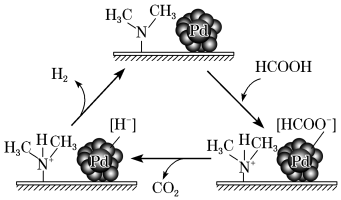
②研究发现:其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳,其具体优点是提高释放氢气的速率,提高释放出氢气的纯度,请分析原因
您最近半年使用:0次
名校
6 .  和
和 在催化剂表面合成氨的微观历程及能量变化的示意图如下,用
在催化剂表面合成氨的微观历程及能量变化的示意图如下,用 、
、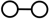 、
、 分别表示
分别表示 、
、 、
、 ,已知:
,已知: ,反应释放热量,下列说法正确的是
,反应释放热量,下列说法正确的是

| A.合成氨反应中,反应物断键吸收能量小于生成物形成新键释放的能量 |
B.②→③过程,是吸热过程且只有 键的断裂 键的断裂 |
C.③→④过程,N原子和H原子形成了含有非极性键的 |
D.使用催化剂,对生成 的速率没有影响 的速率没有影响 |
您最近半年使用:0次
名校
解题方法
7 . 针对反应速率与平衡产率的矛盾,我国科学家提出了采用 复合催化剂解决方案。
复合催化剂解决方案。 合成氨催化反应中活化能最大的
合成氨催化反应中活化能最大的 是
是_______ 。
(2)如图可以得出一个关于复合催化剂的结论是_______ 。
 复合催化剂解决方案。
复合催化剂解决方案。
 合成氨催化反应中活化能最大的
合成氨催化反应中活化能最大的 是
是(2)如图可以得出一个关于复合催化剂的结论是
您最近半年使用:0次
名校
解题方法
8 . 燃油汽车尾气中含有CO和氮氧化物,在 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示:不正确 的是
 的催化作用下,发生反应:
的催化作用下,发生反应: ,可降低污染。其反应历程和相对能量变化如图所示:
,可降低污染。其反应历程和相对能量变化如图所示: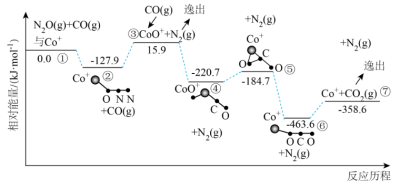
A. 分子的中心原子是N,分子中O—N—N的键角大于 分子的中心原子是N,分子中O—N—N的键角大于 分子中O—N—O的键角 分子中O—N—O的键角 |
| B.历程中决定反应速率的变化过程是②→③ |
C.总反应分两步进行,已知 参与第一步反应,则第二步反应为: 参与第一步反应,则第二步反应为: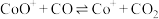 |
D.恒容、绝热下模拟反应: ,体系的温度、 ,体系的温度、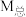 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 (平均相对分子质量)、压强恒定均能说明反应达到平衡状态 |
您最近半年使用:0次
9 . 下列实验装置不能达到实验目的的是

| A.甲:干燥氨气 |
| B.乙:验证溴单质的得电子能力强于碘单质 |
C.丙:用 做喷泉实验 做喷泉实验 |
D.丁:证明 溶液对 溶液对 分解的催化作用 分解的催化作用 |
您最近半年使用:0次
名校
10 . 金表面发生分解反应: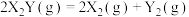 ,其速率方程为
,其速率方程为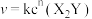 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
下列叙述不正确的是
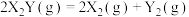 ,其速率方程为
,其速率方程为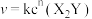 ,已知部分信息如下:
,已知部分信息如下: 为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示:
为速率常数,只与催化剂、温度、固体接触面积有关;在某温度下,实验测得生成物浓度与时间变化的关系如下表所示: | 0 | 20 | 40 | 60 | 80 | 100 |
 | 0.100 | 0.040 | 0.020 | 0 | ||
 | 0 | 0.020 | ||||
 | 0 | 0.020 |
| A.提高反应物浓度,反应速率不变 |
B. |
C.其他条件不变,若 起始浓度为 起始浓度为 ,则反应物浓度减半所需时间为 ,则反应物浓度减半所需时间为 |
D.当升高温度,反应 时 时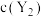 可能小于 可能小于 |
您最近半年使用:0次



