1 . 下列实验事实引出的结论不正确的是
| 选项 | 事实 | 结论 |
| A | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸,比较析出沉淀所需时间 | 当其他条件不变时,反应物浓度增大,化学反应速率加快 |
| B | 向FeCl3溶液中加入几滴KSCN溶液,溶液变红,然后加入少量铁粉,红色变浅 | 铁粉与KSCN溶液反应,减少了FeCl3与KSCN的反应 |
| C | 往浅黄色固体难溶物AgBr中加水,振荡,静置。取上层清液,然后加入NaI固体,产生黄色沉淀 | 难溶物存在沉淀溶解平衡 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . H2是非常重要的化工原料和能源物质。目前在催化剂的作用下,以硼氢化钠(NaBH)和水反应可获取H2,其微观过程如图所示。下列有关说法正确的是
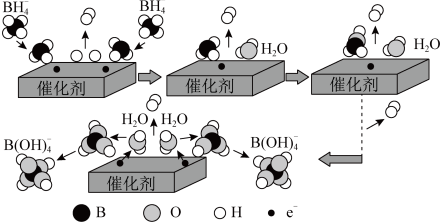
| A.整个过程中H2O多次参与反应历程 |
| B.该催化过程发生的是一个非氧化还原反应 |
| C.反应过程中B原子的成键数目不变 |
| D.催化剂可以加快反应速率,其用量多少不影响反应速率 |
您最近半年使用:0次
解题方法
3 . 甲醇( )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示:
 )作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以
)作为重要的清洁燃料和合成化学的关键前驱体,在化工行业需求旺盛。以 为催化剂在水溶液中电催化二氧化碳还原为
为催化剂在水溶液中电催化二氧化碳还原为 和
和 的能量变化如图所示:
的能量变化如图所示: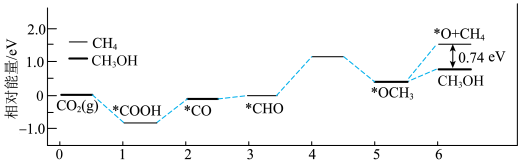
A.生成甲醇反应的决速步为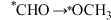 |
| B.两反应只涉及极性键的断裂和生成 |
| C.通过上图分析:甲烷比甲醇稳定 |
D.用 作催化剂可提高甲醇的选择性 作催化剂可提高甲醇的选择性 |
您最近半年使用:0次
4 . 乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为C2H5OH(g)+IB(g) ETBE(g) △H。回答下列问题:
ETBE(g) △H。回答下列问题:
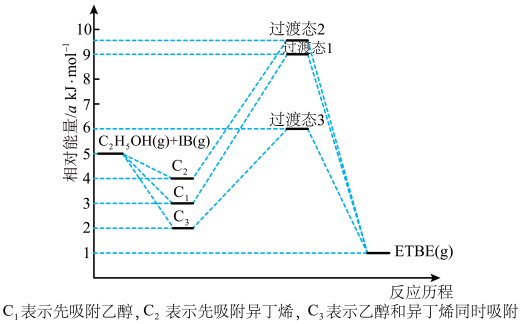
(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=______ kJ•mol-1。反应历程的最优途径是______ (填“C1”、“C2”或“C3”)。 2CO2(g)+S(l) △H=-270kJ•mol-1。
2CO2(g)+S(l) △H=-270kJ•mol-1。
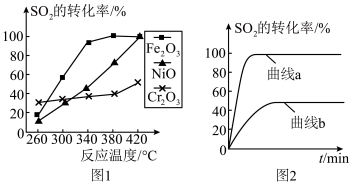
①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是_______ 。
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为______ 。 N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压 物质的量分数)有如下关系:
物质的量分数)有如下关系: (NO2)=k1×p2(NO2),
(NO2)=k1×p2(NO2), (N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
(N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=______ ;在图3标出的点中,能表示反应达到平衡状态的点是______ 。
 ETBE(g) △H。回答下列问题:
ETBE(g) △H。回答下列问题:(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=
 2CO2(g)+S(l) △H=-270kJ•mol-1。
2CO2(g)+S(l) △H=-270kJ•mol-1。①其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了n(CO):n(SO2)为1:1、3:1时SO2转化率的变化情况(图2)。则图2中表示n(CO):n(SO2)=3:1的变化曲线为
 N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压 物质的量分数)有如下关系:
物质的量分数)有如下关系: (NO2)=k1×p2(NO2),
(NO2)=k1×p2(NO2), (N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
(N2O4)=k2×p(N2O4)。相应的消耗速率与其分压的关系如图3所示。一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=
您最近半年使用:0次
解题方法
5 . 向铜屑、稀盐酸和铁盐的混合溶液中持续通入空气可制备氯化铜,其反应过程如图所示。下列说法不正确 的是
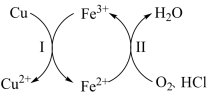

A.制备 的总反应为 的总反应为 |
B.反应Ⅰ中 作氧化剂 作氧化剂 |
C.反应Ⅱ中 作还原剂 作还原剂 |
D.还原性: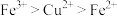 |
您最近半年使用:0次
名校
6 . 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲、乙两位同学分别设计了如图甲、乙所示的实验。下列叙述不正确的是

| A.图甲所示实验可通过观察产生气泡的快慢来比较反应速率的大小 |
| B.若图甲所示实验中反应速率:①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好 |
| C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间 |
| D.为检查图乙所示装置的气密性,可关闭A处旋塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近半年使用:0次
2024-04-05更新
|
892次组卷
|
4卷引用:安徽省蚌埠市怀远禹泽、固镇县汉兴学校2023-2024学年高二上学期12月期末联考化学试题
解题方法
7 . 回收利用 是目前解决空间站供氧问题的有效途径,其物质转化如图:
是目前解决空间站供氧问题的有效途径,其物质转化如图:

反应A为 ,是回收利用
,是回收利用 的关键步骤。
的关键步骤。
发生反应A的过程中,有副反应发生,主要涉及的副反应如下:
Ⅰ.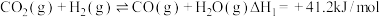
Ⅱ.
(1)反应 的
的
_______  。
。
(2)向某容积为 的恒容密闭容器中充入
的恒容密闭容器中充入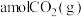 和
和 ,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得
,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得 的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
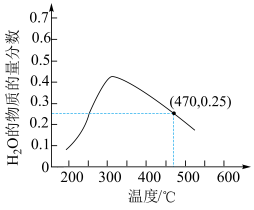
①请用虚线 在上图中画出在250℃-550℃间内,反应 达到平衡时,
达到平衡时, 的物质的量分数随温度变化的曲线
的物质的量分数随温度变化的曲线_______ 。
②在470℃时,反应 的平衡常数
的平衡常数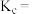
_______  (用含a的最简分数表示)。
(用含a的最简分数表示)。
③实际生产中,温度过高或温度过低均不利于该反应的进行,原因是_______ 。
(3)下列关于空间站内物质转化和能量变化的说法中,不正确 的是_______ (填字母)。
a.反应B的能量变化是电能(或光能) 化学能
化学能
b.目前科学家致力于开发新型催化剂,此催化剂可将 的分解转为放热反应,降低生产
的分解转为放热反应,降低生产 的成本
的成本
c.反应Ⅰ的 ,反应II的
,反应II的
d.镍粒子催化剂的颗粒大小不影响反应速率
(4)用 代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是_______ 。
 是目前解决空间站供氧问题的有效途径,其物质转化如图:
是目前解决空间站供氧问题的有效途径,其物质转化如图:
反应A为
 ,是回收利用
,是回收利用 的关键步骤。
的关键步骤。发生反应A的过程中,有副反应发生,主要涉及的副反应如下:
Ⅰ.
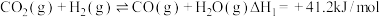
Ⅱ.

(1)反应
 的
的
 。
。(2)向某容积为
 的恒容密闭容器中充入
的恒容密闭容器中充入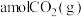 和
和 ,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得
,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得 的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
①请用
 达到平衡时,
达到平衡时, 的物质的量分数随温度变化的曲线
的物质的量分数随温度变化的曲线②在470℃时,反应
 的平衡常数
的平衡常数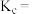
 (用含a的最简分数表示)。
(用含a的最简分数表示)。③实际生产中,温度过高或温度过低均不利于该反应的进行,原因是
(3)下列关于空间站内物质转化和能量变化的说法中,
a.反应B的能量变化是电能(或光能)
 化学能
化学能b.目前科学家致力于开发新型催化剂,此催化剂可将
 的分解转为放热反应,降低生产
的分解转为放热反应,降低生产 的成本
的成本c.反应Ⅰ的
 ,反应II的
,反应II的
d.镍粒子催化剂的颗粒大小不影响反应速率
(4)用
 代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
您最近半年使用:0次
8 . 下列叙述正确的是


| A.由图甲可知, 2SO3(g)⇌2SO2(g)+O2(g) ∆H=(b-a)kJ·mol-1 |
| B.图乙表示反应物断键吸收的能量大于生成物成键放出的能量 |
| C.图丙表示燃料燃烧反应的能量变化 |
| D.图丁表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
您最近半年使用:0次
9 . 一定条件下的密闭容器中发生反应: ,若其他条件不变,下列措施会使该反应速率减小的是
,若其他条件不变,下列措施会使该反应速率减小的是
 ,若其他条件不变,下列措施会使该反应速率减小的是
,若其他条件不变,下列措施会使该反应速率减小的是| A.升高温度 | B.减小压强 | C.增大 浓度 浓度 | D.加入催化剂 |
您最近半年使用:0次
10 . 下列是哈伯法制氨气的流程图,其中为提高反应速率而采取的措施是
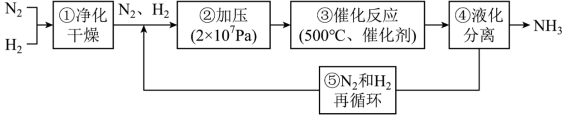

| A.①③④⑤ | B.①②③ | C.①②④ | D.②③④ |
您最近半年使用:0次



