解题方法
1 . 某化学学习小组采用以下方法检验Na2O2中混杂的Na2CO3。下列说法错误的是


| A.Na2O2与水反应过程中有H2O2生成 |
| B.MnO2是催化剂 |
| C.产生白色沉淀,Na2O2样品中含有Na2CO3 |
| D.将Na2O2样品中加入稀盐酸,有气体产生,也可证明含有Na2CO3 |
您最近半年使用:0次
2 . 某实验小组探究 能否催化
能否催化 和
和 反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②
反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②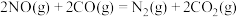
 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是

 能否催化
能否催化 和
和 反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②
反应生成无毒物质。已知:①Ni、Fe的氢氧化物化学性质相似;②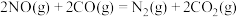
 。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
。现采用如下两个装置完成探究实验(夹持装置略去)。下列有关说法正确的是
| A.从理论上推断,高温有利于反应②自发进行 |
B.固体A成分可能为 、 、 |
| C.反应过程中装置1和2中气体均表现还原性 |
D.若实验证明 能够成功催化,则装置1中的方程式为: 能够成功催化,则装置1中的方程式为: |
您最近半年使用:0次
名校
解题方法
3 . 已知SO2+4I-+4H+=S↓+2I2+2H2O,现进行如下图所示实验。下列说法错误的是


| A.改变c(H+)对反应速率没有影响 |
| B.该反应能够证明SO2既有氧化性,又有还原性 |
| C.整个反应过程中,KI可能起到了催化剂的作用 |
D.该过程中SO2发生的总反应可能为3SO2+2H2O=2SO +S↓+4H+ +S↓+4H+ |
您最近半年使用:0次
2022-07-15更新
|
323次组卷
|
3卷引用:陕西省西安市长安区第一中学2021-2022学年高二下学期期末考试化学试题
陕西省西安市长安区第一中学2021-2022学年高二下学期期末考试化学试题(已下线)2.1.2 影响化学反应速率的因素 活化能 -2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)河南省中原名校2022-2023学年高二上学期第二次联考化学试题
名校
4 . 在化学反应的研究和实际应用中,人们除了选择合适的化学反应以实现所期待的物质转化或能量转化,还要关注化学反应进行的快慢和程度,以提高生产效率,下列关于化学反应速率和程度说法正确的是
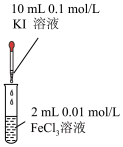 | 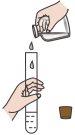 |  |  |
① | ② | ③ | ④ |
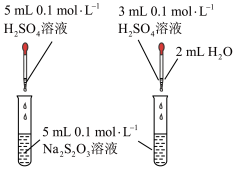
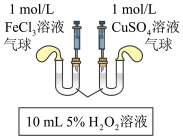
A.取少量图①充分反应后的溶液于试管中,若滴加KSCN溶液后溶液呈红色可以证明可逆反应 存在反应进行的限度 存在反应进行的限度 |
B.若图②是将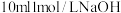 溶液一次性且快速加入到 溶液一次性且快速加入到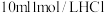 ,结束反应10s,则HCl的化学反应速率为 ,结束反应10s,则HCl的化学反应速率为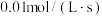 |
C.图③可以探究 浓度对化学反应速率的影响:左试管的速率大于右试管的速率 浓度对化学反应速率的影响:左试管的速率大于右试管的速率 |
D.图④比较 、 、 对反应 对反应 分解制氧气的化学反应速率催化效果 分解制氧气的化学反应速率催化效果 |
您最近半年使用:0次
2022-07-03更新
|
272次组卷
|
4卷引用:江西省上饶市六校2021-2022学年高一下学期期末联考化学试题
解题方法
5 . 能量以多种不同的形式存在,并能相互转化。
I.化学反应伴随能量变化。
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,___________ 代表反应活化能(填“E1”或“E2”)。
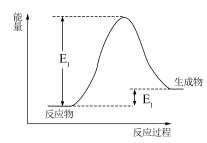
(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是___________ (填序号)。
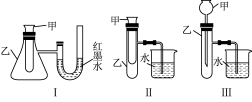
(3)NH4HCO3和CH3COOH反应的离子方程式为___________ 。
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用 、
、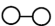 、
、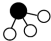 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
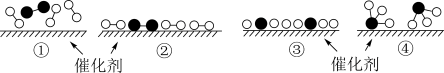
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。
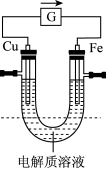
(5)电解质溶液为FeCl3时,图中箭头的方向表示___________ (填“电子”或“电流”)的流向,铁片上的电极反应式为___________ 。
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。
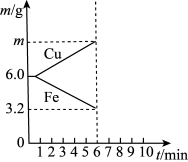
①X可以是___________ (填字母)。
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为___________ g。
I.化学反应伴随能量变化。
(1)NH4HCO3和CH3COOH反应过程的能量变化如图所示,

(2)某实验小组设计了三套实验装置(如图),不能用来证明“NH4HCO3和CH3COOH反应能量变化情况”的是

(3)NH4HCO3和CH3COOH反应的离子方程式为
II.合成氨反应为放热反应,在化工生产中具有重要意义。
(4)N2和H2在催化剂表面合成気的微观历程如图所示,用
 、
、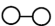 、
、 分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)
分别表示N2、H2、NH3。下列说法不正确的是___________。(填字母)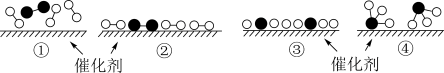
| A.反应过程存在非极性共价键的断裂和形成 |
| B.催化剂仅起到吸附N2和H2的作用,对化学反应速率没有影响 |
| C.②→③过程吸热 |
| D.反应物断键吸收的总能量小于生成物成键释放的总能量 |
III.电池的发明是储能和供能技术的巨大进步,如图所示的原电池装置,插入电解质溶液前Cu和Fe电极质量相等。

(5)电解质溶液为FeCl3时,图中箭头的方向表示
(6)电解质溶液更换为X时,电极质量变化曲线如图所示。

①X可以是
A.稀硫酸 B.CuSO4溶液 C.稀盐酸 D.FeSO4溶液
②6 min时Cu电极的质量a为
您最近半年使用:0次
6 . 下列实验方案不能达到相应目的的是
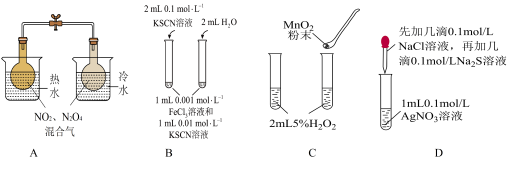

| A.探究温度对化学平衡的影响 | B.研究浓度对化学平衡的影响 |
| C.探究催化剂对反应速率的影响 | D.证明溶解度: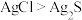 |
您最近半年使用:0次
解题方法
7 . 双氧水在工业、医药等领域应用广泛。某小组采用如下方法制备 并探究
并探究 的分解反应机理。回答下列问题:
的分解反应机理。回答下列问题:
Ⅰ.电解-水解法制备 制备步骤:
制备步骤:
(1)①电解硫酸氢钾饱和溶液,制取 ;
;
②将电解所得 酸化水解制取
酸化水解制取 。电解时阳极反应式为
。电解时阳极反应式为___________ 。

Ⅱ.探究的分解反应机理
①按图1连接装置,检查装置气密性;
②向a中加入60mL15%H2O2,观察现象,通过pH传感器测pH;
③20s时,打开双通阀,向a中加入1滴管 溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。
溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。

回答下列问题:
(2)仪器a的名称是___________ ,已知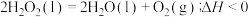 ,据此分析并说明常温常压下
,据此分析并说明常温常压下 能否分解
能否分解___________ ,前20s测得溶液pH为3.47,其原因是___________ (用电离方程式表示)。
(3)步骤③中加入 溶液后的现象为
溶液后的现象为___________ 、溶液颜色由黄色变深,又变回黄色。20~23s pH变化的原因是___________ 。结合图2和图3,23~150s pH变化对应的历程为___________ (用序号表示),150s后pH变化的原因是___________ (用反应式表示)。
(4)加入 溶液后,150s时收集到19.5mL
溶液后,150s时收集到19.5mL ,则用
,则用 的体积变化表示该反应的速率为
的体积变化表示该反应的速率为___________ 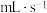 。该实验证明催化剂通过改变反应历程,从而加快反应速率。
。该实验证明催化剂通过改变反应历程,从而加快反应速率。
 并探究
并探究 的分解反应机理。回答下列问题:
的分解反应机理。回答下列问题:Ⅰ.电解-水解法制备
 制备步骤:
制备步骤:(1)①电解硫酸氢钾饱和溶液,制取
 ;
;②将电解所得
 酸化水解制取
酸化水解制取 。电解时阳极反应式为
。电解时阳极反应式为
Ⅱ.探究的分解反应机理
①按图1连接装置,检查装置气密性;
②向a中加入60mL15%H2O2,观察现象,通过pH传感器测pH;
③20s时,打开双通阀,向a中加入1滴管
 溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。
溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。
回答下列问题:
(2)仪器a的名称是
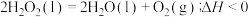 ,据此分析并说明常温常压下
,据此分析并说明常温常压下 能否分解
能否分解(3)步骤③中加入
 溶液后的现象为
溶液后的现象为(4)加入
 溶液后,150s时收集到19.5mL
溶液后,150s时收集到19.5mL ,则用
,则用 的体积变化表示该反应的速率为
的体积变化表示该反应的速率为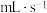 。该实验证明催化剂通过改变反应历程,从而加快反应速率。
。该实验证明催化剂通过改变反应历程,从而加快反应速率。
您最近半年使用:0次
名校
8 . 近年来,将氯化氢转化为氟气的技术成为科学研究的热点。工业上用O2将HCl转化为Cl2,可减少污染。在传统催化剂并加热条件下可实现该转化(反应混合物均为气态),方程式如下: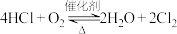
(1)某温度下,将一定量的O2和HCl通入4L的密闭容器中,反应过程中氧气的变化量如图所示,则0~20min平均反应速率v(HCI)为___________ 。

(2)下列选项中,能证明上述反应达到达到平衡状态的是___________。
(3)对该反应达到平衡后,以下分析正确的是___________。
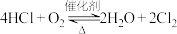
(1)某温度下,将一定量的O2和HCl通入4L的密闭容器中,反应过程中氧气的变化量如图所示,则0~20min平均反应速率v(HCI)为

(2)下列选项中,能证明上述反应达到达到平衡状态的是___________。
| A.单位时间内生成1molO2的同时生成2molCl2 |
| B.v(H2O)=v(Cl2) |
| C.容器中气体的平均相对分子质量不随时间变化而变化 |
| D.容器中气体密度不随时间变化而变化 |
| A.增加n(HCl),对正反应的反应速率影响更大 |
| B.体积不变加入稀有气体,对正反应的反应速率影响更大 |
| C.压强不变加入稀有气体,对逆反应的反应速率影响更大 |
| D.其他条件不变,使用不同催化剂,Cl2(g)的产率不同 |
您最近半年使用:0次
9 . 用下列仪器或装置进行相应实验,可以达到实验目的的是
 | 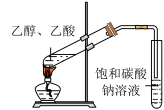 |  | 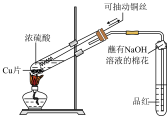 |
A.证明 是 是 分解的催化剂 分解的催化剂 | B.制备并收集乙酸乙酯 | C.收集 气体 气体 | D.检验浓硫酸与铜反应产生的 气体 气体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 下图有关实验或操作能达到实验目的的是


A.①证明 |
| B.②装置蒸发氯化铝溶液制备无水氯化铝 |
C.③装置可判断 反应的热效应 反应的热效应 |
| D.④验证氯化铁对过氧化氢的分解有催化作用 |
您最近半年使用:0次



