解题方法
1 . 化学实验小组同学针对教材中提出的“硫酸铜溶液等对过氧化氢的分解也具有催化作用”进行相关探究。
(1)要证明 溶液可作
溶液可作 分解的催化剂,除需证明
分解的催化剂,除需证明 溶液能改变
溶液能改变 分解的速率外,还需证明
分解的速率外,还需证明 在化学反应前后的
在化学反应前后的________ 不变;
【探究一】:在化学反应前后的质量是否发生改变?
(2)实验小组同学设计了如下实验:将含溶质质量为 的
的 溶液加入一定量的
溶液加入一定量的 溶液中,取充分反应后的全部溶液继续进行实验,流程如图(实验过程中的损耗忽略不计)。
溶液中,取充分反应后的全部溶液继续进行实验,流程如图(实验过程中的损耗忽略不计)。
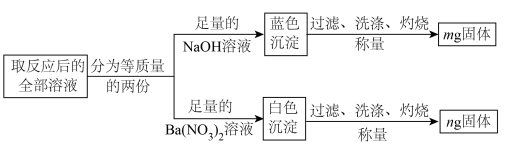
①蓝色沉淀灼烧时发生分解反应,只生成黑色固体和水,该反应的化学方程式________ 。
②流程中生成白色沉淀的化学方程式为________ 。
③若 在化学反应前后质量未改变,则该实验需满足的定量关系为:
在化学反应前后质量未改变,则该实验需满足的定量关系为:
________ (用含m、n的式子表示)。
【探究二】:溶液中起催化作用的是哪种微观粒子?
(3)①【提出猜想】猜想1:起催化作用的是 ;猜想2:起催化作用的是
;猜想2:起催化作用的是________ 。
②【对比实验】设计如图所示实验进行探究。

若观察到________ (填实验现象),则说明猜想1正确。
(1)要证明
 溶液可作
溶液可作 分解的催化剂,除需证明
分解的催化剂,除需证明 溶液能改变
溶液能改变 分解的速率外,还需证明
分解的速率外,还需证明 在化学反应前后的
在化学反应前后的【探究一】:在化学反应前后的质量是否发生改变?
(2)实验小组同学设计了如下实验:将含溶质质量为
 的
的 溶液加入一定量的
溶液加入一定量的 溶液中,取充分反应后的全部溶液继续进行实验,流程如图(实验过程中的损耗忽略不计)。
溶液中,取充分反应后的全部溶液继续进行实验,流程如图(实验过程中的损耗忽略不计)。
①蓝色沉淀灼烧时发生分解反应,只生成黑色固体和水,该反应的化学方程式
②流程中生成白色沉淀的化学方程式为
③若
 在化学反应前后质量未改变,则该实验需满足的定量关系为:
在化学反应前后质量未改变,则该实验需满足的定量关系为:
【探究二】:溶液中起催化作用的是哪种微观粒子?
(3)①【提出猜想】猜想1:起催化作用的是
 ;猜想2:起催化作用的是
;猜想2:起催化作用的是②【对比实验】设计如图所示实验进行探究。

若观察到
您最近一年使用:0次
2 . Ⅰ.降低能耗是氯碱工业发展的重要方向。我国利用氯碱厂生产的H2作燃料,将氢燃料电站应用于氯碱工业,其示意图如图。
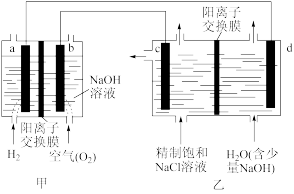
(1)写出b电极的电极反应式_______ 。
(2)写出乙装置发生的总化学方程式_______ 。
(3)若放电一段时间后,消耗空气22.4L(标况),不考虑损耗的情况下,乙池产生的气体_______ mol。
(4)下列说法正确的是_______ 。
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
Ⅱ.二氧化碳催化加氢也可合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH。在密闭容器中投入1mol CO2和2.75mol H2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
CH3OH(g)+H2O(g) ΔH。在密闭容器中投入1mol CO2和2.75mol H2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
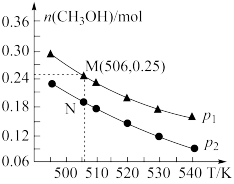
(5)二氧化碳合成甲醇正反应的ΔH_______ 0(填“>”、“<”或“=”),理由是_______ 。
(6)一定条件下,向容积不变的某密闭容器中加入a mol CO2和b mol H2发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是
CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是_______ 。
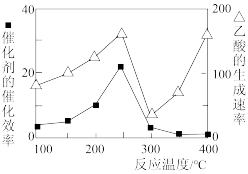
(7)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。当乙酸的生成速率主要取决于温度时,其影响范围是_______ 。

(1)写出b电极的电极反应式
(2)写出乙装置发生的总化学方程式
(3)若放电一段时间后,消耗空气22.4L(标况),不考虑损耗的情况下,乙池产生的气体
(4)下列说法正确的是
A.甲装置可以实现化学能向电能转化
B.甲装置中Na+透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是淡盐水
Ⅱ.二氧化碳催化加氢也可合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH。在密闭容器中投入1mol CO2和2.75mol H2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
CH3OH(g)+H2O(g) ΔH。在密闭容器中投入1mol CO2和2.75mol H2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如图所示。
(5)二氧化碳合成甲醇正反应的ΔH
(6)一定条件下,向容积不变的某密闭容器中加入a mol CO2和b mol H2发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是
CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是(7)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。当乙酸的生成速率主要取决于温度时,其影响范围是

您最近一年使用:0次



