名校
1 . 甲醇 属于基础化工原料,在化学工业中占有重要地位。回答下列问题:
属于基础化工原料,在化学工业中占有重要地位。回答下列问题:
(1)工业上制备甲醇的热化学方程式为
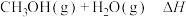 。已知
。已知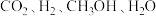 的能量依次为
的能量依次为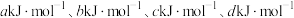 ,则
,则
___________  。将物质的量之比1:3的
。将物质的量之比1:3的 和
和 以相同的流速分别通过两种催化剂(Cat-a和Cat-b),相同时间内测得
以相同的流速分别通过两种催化剂(Cat-a和Cat-b),相同时间内测得 的转化率随温度变化的关系如图1所示:使
的转化率随温度变化的关系如图1所示:使 的转化率最好的催化剂是
的转化率最好的催化剂是___________ (填“Cat-a”或“Cat-b”),与另一催化剂相比,使用该催化剂存在的㢣端是___________ 。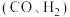 ,反应为
,反应为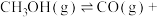
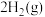 。起始时,向某刚性容器中通入一定量的
。起始时,向某刚性容器中通入一定量的 ,平衡时各物质的物质的量与温度的关系如图2所示。
,平衡时各物质的物质的量与温度的关系如图2所示。___________ (填化学式)。
②A点处体系中 的体积分数为
的体积分数为___________ 。
③ 点处,若容器的压强为
点处,若容器的压强为 ,则
,则 点处
点处 的转化率为
的转化率为___________ ,此温度下该反应的平衡常数
___________  (用平衡压强代替平衡浓度,分压=总压
(用平衡压强代替平衡浓度,分压=总压 物质的量分数)。
物质的量分数)。
(3)甲醇可催化制备丙烯,反应为 ,反应的Arrhenius公式的实验数据如图3中a所示,已知Arrhenius经验公式为
,反应的Arrhenius公式的实验数据如图3中a所示,已知Arrhenius经验公式为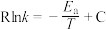 (其中
(其中 为活化能,
为活化能, 为速率常数,只与温度有关,
为速率常数,只与温度有关, 和C为常数)。
和C为常数)。
___________  。
。
②当使用更高效催化剂时,实验数据变成图3中的曲线___________ (填图3“b”或“c”)。
 属于基础化工原料,在化学工业中占有重要地位。回答下列问题:
属于基础化工原料,在化学工业中占有重要地位。回答下列问题:(1)工业上制备甲醇的热化学方程式为

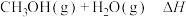 。已知
。已知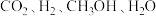 的能量依次为
的能量依次为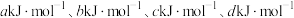 ,则
,则
 。将物质的量之比1:3的
。将物质的量之比1:3的 和
和 以相同的流速分别通过两种催化剂(Cat-a和Cat-b),相同时间内测得
以相同的流速分别通过两种催化剂(Cat-a和Cat-b),相同时间内测得 的转化率随温度变化的关系如图1所示:使
的转化率随温度变化的关系如图1所示:使 的转化率最好的催化剂是
的转化率最好的催化剂是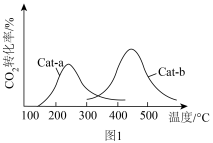
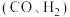 ,反应为
,反应为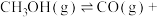
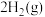 。起始时,向某刚性容器中通入一定量的
。起始时,向某刚性容器中通入一定量的 ,平衡时各物质的物质的量与温度的关系如图2所示。
,平衡时各物质的物质的量与温度的关系如图2所示。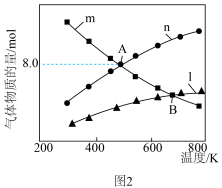
②A点处体系中
 的体积分数为
的体积分数为③
 点处,若容器的压强为
点处,若容器的压强为 ,则
,则 点处
点处 的转化率为
的转化率为
 (用平衡压强代替平衡浓度,分压=总压
(用平衡压强代替平衡浓度,分压=总压 物质的量分数)。
物质的量分数)。(3)甲醇可催化制备丙烯,反应为
 ,反应的Arrhenius公式的实验数据如图3中a所示,已知Arrhenius经验公式为
,反应的Arrhenius公式的实验数据如图3中a所示,已知Arrhenius经验公式为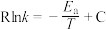 (其中
(其中 为活化能,
为活化能, 为速率常数,只与温度有关,
为速率常数,只与温度有关, 和C为常数)。
和C为常数)。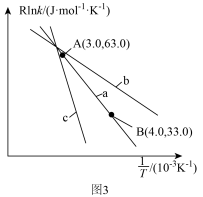

 。
。②当使用更高效催化剂时,实验数据变成图3中的曲线
您最近一年使用:0次
2024-02-23更新
|
249次组卷
|
5卷引用:河南省郑州市第五高级中学2023-2024学年高三2月开学考理综试题-高中化学
2 . 课外实验小组以KI参与的某些反应来对反应过程和化学反应原理进行探究。
(1)KI中的 促进
促进 分解的反应机理如下
分解的反应机理如下
① (慢)
(慢)
② (快)
(快)
则此过程的决速步骤为______ (填序号),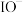 在此过程中的作用是
在此过程中的作用是____________ 。
(2)KI中的 在经酸化的溶液中易被空气氧化:
在经酸化的溶液中易被空气氧化:
实验小组探究外界条件对反应速率的影响,部分实验数据如下表。
①为确保A组实验在39℃下进行,应采用的控温方法为______ 。
②B组实验中V=______ ,C组是探究______ 对反应速率的影响,t的取值范围为______ 。
(3)若将C组实验反应后溶液充分放置一段时间,检验其吸收 的体积,可用
的体积,可用 标准溶液滴定吸收液(
标准溶液滴定吸收液( ),实验时应将
),实验时应将 标准溶液放在
标准溶液放在______ 滴定管中,滴定终点时实验现象为______ ,若消耗0.2mol/L 标准溶液为15.00mL,则吸收氧气在标准状况下的体积为
标准溶液为15.00mL,则吸收氧气在标准状况下的体积为______ 。
(1)KI中的
 促进
促进 分解的反应机理如下
分解的反应机理如下①
 (慢)
(慢)②
 (快)
(快)则此过程的决速步骤为
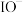 在此过程中的作用是
在此过程中的作用是(2)KI中的
 在经酸化的溶液中易被空气氧化:
在经酸化的溶液中易被空气氧化:
实验小组探究外界条件对反应速率的影响,部分实验数据如下表。
编号 | 温度/℃ |  硫酸体积/mL 硫酸体积/mL |  KI溶液体积/mL KI溶液体积/mL |  体积/mL 体积/mL | 淀粉溶液体积/mL | 出现蓝色的时间/s |
| A | 39 | 10.0 | 5.0 | 5.0 | 1.0 | 5 |
| B | 5 | 10.0 | 5.0 | V | 1.0 | 39 |
| C | 39 | 15.0 | 5.0 | 0.0 | 1.0 | t |
②B组实验中V=
(3)若将C组实验反应后溶液充分放置一段时间,检验其吸收
 的体积,可用
的体积,可用 标准溶液滴定吸收液(
标准溶液滴定吸收液( ),实验时应将
),实验时应将 标准溶液放在
标准溶液放在 标准溶液为15.00mL,则吸收氧气在标准状况下的体积为
标准溶液为15.00mL,则吸收氧气在标准状况下的体积为
您最近一年使用:0次
2022-11-24更新
|
305次组卷
|
4卷引用:河南省商丘市名校2022-2023学年高二下学期第一次联考(开学考试)化学试题
名校
3 . 工业制硫酸中的一步重要反应是SO2的催化氧化。在2L密闭容器中,充入SO2和O2,在催化剂、500℃的条件下发生反应。SO2与SO3的物质的量随时间变化的曲线如图所示,请回答下列问题。

(1)反应开始至2min末,以O2的浓度变化表示该反应的平均反应速率是_______ ;表示SO3的物质的量随时间变化的曲线是_______ (填相应的字母编号)。
(2)由图象可知SO2与O2的反应是可逆反应,证据是_______ 。
(3)下列说法不正确的是_______ 。
a.催化剂可以加快化学反应速率,缩短达到化学平衡所需的时间
b.恒容条件下,通入氮气使压强增大,该反应速率加快
c.通过调控反应条件,可以改变该反应的限度
d.若仅增大容器容积,则该化学反应速率增大
(4)下列情况,能说明该反应一定达到化学平衡状态的是_______ 。
a.单位时间内消耗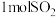 ,同时生成
,同时生成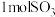
b.SO2的物质的量保持不变
c.混合气体的密度不变
d.SO2的浓度与SO3的浓度相等

(1)反应开始至2min末,以O2的浓度变化表示该反应的平均反应速率是
(2)由图象可知SO2与O2的反应是可逆反应,证据是
(3)下列说法不正确的是
a.催化剂可以加快化学反应速率,缩短达到化学平衡所需的时间
b.恒容条件下,通入氮气使压强增大,该反应速率加快
c.通过调控反应条件,可以改变该反应的限度
d.若仅增大容器容积,则该化学反应速率增大
(4)下列情况,能说明该反应一定达到化学平衡状态的是
a.单位时间内消耗
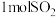 ,同时生成
,同时生成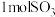
b.SO2的物质的量保持不变
c.混合气体的密度不变
d.SO2的浓度与SO3的浓度相等
您最近一年使用:0次
名校
4 . 为减少大气污染,科学家采取多种措施处理工业废气中排放的氮氧化物(NOx)、SO2等。回答下列问题:
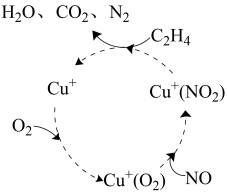
(1)某脱硝反应机理如图所示,Cu+的作用为____ ,C2H4参与的反应方程式为____ 。
(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
①若有3molNO参与反应,则被NO氧化的NH3的物质的量为____ 。
②催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是____ 。
③350℃时NO的百分含量与氨氮比的关系如图所示,若只改变氨气的投放量,当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是____ (用化学方程式表示)。

(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点,ClO2在酸性条件下稳定,是性能优良的脱硫脱硝试剂。
①ClO 也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为
也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为____ 。
②某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。
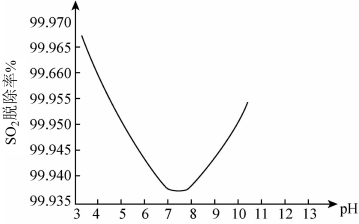
当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是:____ ;在pH约7.8之后,随pH的增大,SO2脱除率又开始升高,其原因是____ 。
(1)某脱硝反应机理如图所示,Cu+的作用为

(2)选择性催化还原技术(SCR)是目前较为成熟的烟气脱硝技术,其反应原理主要为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) △H=-1627kJ·mol-1。
4N2(g)+6H2O(g) △H=-1627kJ·mol-1。①若有3molNO参与反应,则被NO氧化的NH3的物质的量为
②催化还原时应控制反应温度在315~400℃之间,反应温度不宜过高的原因是
③350℃时NO的百分含量与氨氮比的关系如图所示,若只改变氨气的投放量,当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是
(3)烟气脱硫、脱硝一体化技术是大气污染防治研究的热点,ClO2在酸性条件下稳定,是性能优良的脱硫脱硝试剂。
①ClO
 也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为
也是性能优良的脱硫脱硝试剂,ClO2与NaOH溶液反应生成NaClO3和NaClO2,反应的离子方程式为②某研究小组用ClO2进行单独脱除SO2实验时,测得SO2的脱除率随溶液pH变化如图所示。

当3<pH<7时,随pH的增大,SO2脱除率逐渐降低,其原因是:
您最近一年使用:0次
2022-08-29更新
|
242次组卷
|
4卷引用:河南省百所名校2023届高三上学期开学摸底联考化学试题



