名校
解题方法
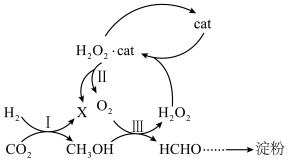
1 . 2021年9月,中国科学院天津工业生物技术研究所成果“无细胞化学酶系统催化 合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
 合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
合成淀粉”在国际学术期刊《自然》上发表,引发化学界的极大关注。其中部分核心反应转化如图所示。下列叙述正确的是
A.反应Ⅰ中消耗2mol ,生成 ,生成 为1mol 为1mol |
B.反应Ⅲ需要额外从环境中补充 |
| C.合成过程可采用高温条件,以加快反应速率 |
D.HCHO转化为淀粉[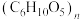 ]的原子利用率可达100% ]的原子利用率可达100% |
您最近一年使用:0次
名校
解题方法
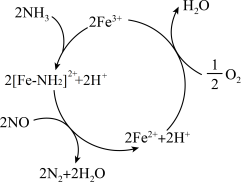
2 . 氮的氧化物是大气污染物之一,一种以 为主的催化剂催化
为主的催化剂催化 脱除烟气中的
脱除烟气中的 反应机理如图所示。下列说法错误的是
反应机理如图所示。下列说法错误的是
 为主的催化剂催化
为主的催化剂催化 脱除烟气中的
脱除烟气中的 反应机理如图所示。下列说法错误的是
反应机理如图所示。下列说法错误的是
A. 为极性分子 为极性分子 |
B.图中反应涉及元 键断裂和形成 键断裂和形成 |
C. 改变了总反应的焓变,提高了反应速率 改变了总反应的焓变,提高了反应速率 |
D.该过程的总反应为: |
您最近一年使用:0次
解题方法
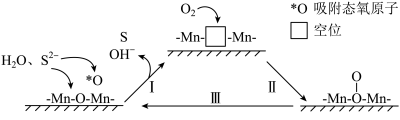
3 . 炼油、石化等工业产生的含硫( 价)废水可通过催化氧化法进行处理。碱性条件下,催化氧化废水的机理如图所示。其中
价)废水可通过催化氧化法进行处理。碱性条件下,催化氧化废水的机理如图所示。其中 为催化剂,附着在催化剂载体聚苯胺的表面。下列说法正确的是
为催化剂,附着在催化剂载体聚苯胺的表面。下列说法正确的是
 价)废水可通过催化氧化法进行处理。碱性条件下,催化氧化废水的机理如图所示。其中
价)废水可通过催化氧化法进行处理。碱性条件下,催化氧化废水的机理如图所示。其中 为催化剂,附着在催化剂载体聚苯胺的表面。下列说法正确的是
为催化剂,附着在催化剂载体聚苯胺的表面。下列说法正确的是
A.转化Ⅰ中 作还原剂,发生还原反应 作还原剂,发生还原反应 |
B. 元素位于第四周期第Ⅶ族 元素位于第四周期第Ⅶ族 |
C.催化氧化过程的总反应为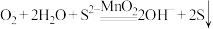 |
D.生成的 进入催化剂空位处可能会导致其催化效率下降 进入催化剂空位处可能会导致其催化效率下降 |
您最近一年使用:0次
2023-10-26更新
|
114次组卷
|
2卷引用:广西壮族自治区桂林市等3地2023-2024学年高三上学期10月月考化学试题
名校
解题方法
4 . 环氧环己烷 作为一种重要的中间体,在有机合成中具有很高的应用价值。在过氧铌酸盐离子催化剂作用下,用环己烯制备环氧环己烷的反应历程及与相对能量关系如下图所示,下列说法错误的是
作为一种重要的中间体,在有机合成中具有很高的应用价值。在过氧铌酸盐离子催化剂作用下,用环己烯制备环氧环己烷的反应历程及与相对能量关系如下图所示,下列说法错误的是

 作为一种重要的中间体,在有机合成中具有很高的应用价值。在过氧铌酸盐离子催化剂作用下,用环己烯制备环氧环己烷的反应历程及与相对能量关系如下图所示,下列说法错误的是
作为一种重要的中间体,在有机合成中具有很高的应用价值。在过氧铌酸盐离子催化剂作用下,用环己烯制备环氧环己烷的反应历程及与相对能量关系如下图所示,下列说法错误的是
| A.过氧铌酸盐离子,CH3OH在反应中均作催化剂 |
B.总反应方程式为:   +H2O +H2O |
| C.步骤I是总反应的决速步骤 |
| D.环己烯制备环氧环己烷反应放出热量 |
您最近一年使用:0次
2023-09-07更新
|
144次组卷
|
4卷引用:2024届广西普通高中学业水平选择性考试第二次调研考试化学试题
名校
解题方法
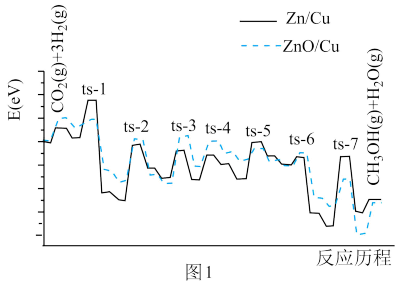
5 . 二氧化碳加氢合成甲醇是化学固碳的一种有效途径,不仅可以有效减少空气中的CO2排放.还可以制备出甲醇清洁能源。在CO2转化为甲醇过程中,伴随有副反应发生,因此常使用催化剂调节控制反应。科学研究者结合实验与计算机模拟,研究了CO2与H2分别在Zn/Cu、ZnO/Cu催化剂表面生成CH3OH和H2O的部分反应历程(如图1所示),其中ts-n表示过渡态。
(1)①图1表示的反应中,若每生成1mol甲醇,反应物与生成物总能量差为58kJ,则反应的热化学方程式为_____ ,从反应原理分析,下列更利于该反应进行的条件是_____ (填标号)。
a.高压、高温 b.高压低温 c.低压、高温 d.低压低温
②已知CO2和H2可发生副反应:CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:
CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:
由此计算E(C=O)=______ kJ•mol-1。
(2)在图1给出的反应历程中,若选择Zn/Cu作为催化剂则正反应最大的活化能发生在______ (用“ts-n”具体数字表示)。图示结果显示,选择ZnO/Cu作为催化剂更优于Zn/Cu,其主要原因是______ 。
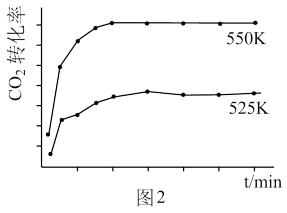
(3)图2为使用Zn/Cu催化剂、分别在525K和550K条件下(其它条件相同),CO2和H2按投料比1:9进行反应生成CH3OH的过程中,CO2的转化率随时间变化图示。______ 。
②工业生产中,对于气相的反应体系,还可用反应体系中各组分的分压来表示化学平衡常数(Kp)。如反应:aA(g)+bB(g) dD(g)+eE(g)达到平衡时,Kp=
dD(g)+eE(g)达到平衡时,Kp=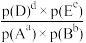 ,组分分压p(A)=P总×
,组分分压p(A)=P总×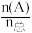 。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=
。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=______ (列出含α、p计算式)。
(1)①图1表示的反应中,若每生成1mol甲醇,反应物与生成物总能量差为58kJ,则反应的热化学方程式为
a.高压、高温 b.高压低温 c.低压、高温 d.低压低温
②已知CO2和H2可发生副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:
CO(g)+H2O(g) ΔH=+41kJ•mol-1部分相关化学键的键能数据如表:| 化学键 | H-H | C-O | H-O | C-H | C≡O |
| E/(kJ•mol-1) | 436 | 326 | 464 | 414 | 1061 |
(2)在图1给出的反应历程中,若选择Zn/Cu作为催化剂则正反应最大的活化能发生在
(3)图2为使用Zn/Cu催化剂、分别在525K和550K条件下(其它条件相同),CO2和H2按投料比1:9进行反应生成CH3OH的过程中,CO2的转化率随时间变化图示。
②工业生产中,对于气相的反应体系,还可用反应体系中各组分的分压来表示化学平衡常数(Kp)。如反应:aA(g)+bB(g)
 dD(g)+eE(g)达到平衡时,Kp=
dD(g)+eE(g)达到平衡时,Kp=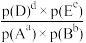 ,组分分压p(A)=P总×
,组分分压p(A)=P总×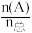 。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=
。现保持550K、pkPa条件,CO2和H2按投料比(物质的量)1:9进行生成CH3OH反应,达到平衡时,CO2的转化率为α,则反应的化学平衡常数Kp=
您最近一年使用:0次
2023-04-08更新
|
437次组卷
|
3卷引用:广西柳州市2023届高三下学期第三次模拟考试理综化学试题
广西柳州市2023届高三下学期第三次模拟考试理综化学试题(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)河北省保定市部分高中2023-2024学年高三上学期1月期末化学试题
名校
解题方法
6 . 在催化剂表面CO2与H2反应的部分历程如图所示,吸附在催化剂表面的物种用“•”标注,Ts表示过渡态。下列说法不正确 的是
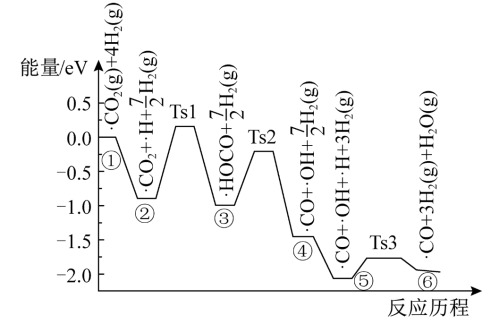

| A.反应•CO2+H2(g)=•CO+H2O(g)的△H<0 |
| B.物质吸附在催化剂表面时通常比其形成的过渡状态稳定 |
| C.②→③是图中①至⑥的历程中的决速步骤 |
| D.③→④的过程中断裂了非极性共价键 |
您最近一年使用:0次
2022-11-04更新
|
227次组卷
|
4卷引用:广西玉林市博白县2023-2024学年高三上学期六校联考化学试卷
名校
解题方法
7 . 有氧条件下,NO在催化剂作用下可被NH3还原为N2,反应机理如图。下列说法错误的是


| A.V5+=O在反应中起到催化剂的作用 |
| B.该转化过程中NO和O2均体现出了氧化性 |
| C.该转化过程中,若O2过量更有利于NO转化为N2 |
D.该转化过程的总反应为4NH3+4NO+O2 4N2+6H2O 4N2+6H2O |
您最近一年使用:0次
2022-04-24更新
|
541次组卷
|
4卷引用:广西玉林市博白县中学2023-2024学年高三上学期开学考试化学试题



