名校
1 . 某反应 的速率方程为
的速率方程为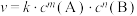 。其中,k为速率常数。已知其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示,下列说法不正确的是
。其中,k为速率常数。已知其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示,下列说法不正确的是
 的速率方程为
的速率方程为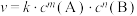 。其中,k为速率常数。已知其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示,下列说法不正确的是
。其中,k为速率常数。已知其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为0.8/k。改变反应物浓度时,反应的瞬时速率如表所示,下列说法不正确的是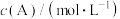 | 0.25 | 0.50 | 1.00 | 0.50 | 1.00 |  |
 | 0.050 | 0.050 | 0.100 | 0.100 | 0.200 |  |
 | 1.6 | 3.2 |  | 3.2 |  | 4.8 |
A.上述表格中的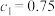 、 、 |
B.该反应的速率常数 |
| C.升温、加入催化剂均可使k增大,反应瞬时速率加快 |
| D.在过量的B存在时,当剩余6.25%的A时,所需的时间是375min |
您最近一年使用:0次
2024-01-24更新
|
469次组卷
|
3卷引用:2024届浙江省瑞安中学高三上学期首考适应性考试 化学试题
2024届浙江省瑞安中学高三上学期首考适应性考试 化学试题重庆市第七中学校2023-2024学年高三下学期2月月考化学试题(已下线)专题06 化学反应速率与化学平衡-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)
名校
2 . 在一定条件下,一定浓度的甲酸溶液在密闭容器中发生分解反应(分解产物均溶于水):
Ⅰ.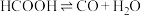 Ⅱ.
Ⅱ.
反应过程中含碳微粒(忽略碳元素的其他存在形式)的占比随时间的变化及反应Ⅰ的反应历程如图所示:
Ⅰ.
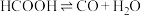 Ⅱ.
Ⅱ.
反应过程中含碳微粒(忽略碳元素的其他存在形式)的占比随时间的变化及反应Ⅰ的反应历程如图所示:
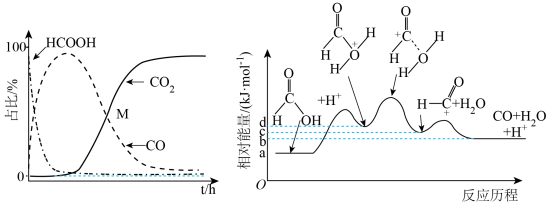
A.反应Ⅰ中 是该反应的催化剂,平衡前适当提高 是该反应的催化剂,平衡前适当提高 浓度有利于加快反应Ⅰ的速率 浓度有利于加快反应Ⅰ的速率 |
B.反应Ⅰ的热化学方程式可表示为: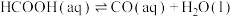 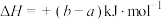 |
C.适当升高温度可降低平衡时CO和 的比例 的比例 |
| D.在反应Ⅰ的反应历程中,存在3种中间产物 |
您最近一年使用:0次
2024-01-12更新
|
342次组卷
|
3卷引用:浙江省宁波市镇海中学2023-2024学年高三上学期首考12月模拟卷化学试题
浙江省宁波市镇海中学2023-2024学年高三上学期首考12月模拟卷化学试题(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)湖南省衡阳市第八中学2024届高三下学期高考模拟预测化学试题
3 . 一定条件下,丙烯与 反应生成
反应生成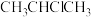 和
和 的反应历程如图所示。下列说法不正确的是
的反应历程如图所示。下列说法不正确的是
 反应生成
反应生成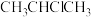 和
和 的反应历程如图所示。下列说法不正确的是
的反应历程如图所示。下列说法不正确的是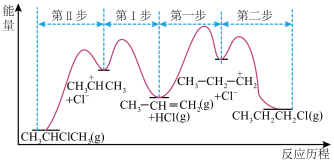
A.合成 的反应中,第一步为反应的决速步 的反应中,第一步为反应的决速步 |
B.其他条件不变,适当升高温度可以提高加成产物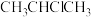 的比例 的比例 |
C.根据该反应推测,丙烯与 加成的主要产物为2-溴丙烷 加成的主要产物为2-溴丙烷 |
D.反应的主要产物为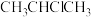 ,是由于活性中间体 ,是由于活性中间体 比 比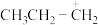 更稳定,所需活化能更低 更稳定,所需活化能更低 |
您最近一年使用:0次
名校
解题方法
4 .  与
与 反应能高选择性地生成甲醇。下图表示
反应能高选择性地生成甲醇。下图表示 分别与
分别与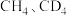 反应体系的能量随反应进程的变化示意图(两者历程相似,图中以
反应体系的能量随反应进程的变化示意图(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
 与
与 反应能高选择性地生成甲醇。下图表示
反应能高选择性地生成甲醇。下图表示 分别与
分别与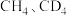 反应体系的能量随反应进程的变化示意图(两者历程相似,图中以
反应体系的能量随反应进程的变化示意图(两者历程相似,图中以 示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是
示例)。已知:直接参与化学键变化的元素被替换为更重的元素时,反应速率会变慢。下列说法正确的是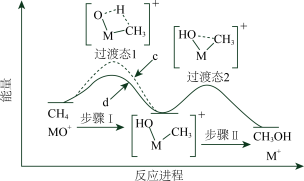
A. 与 与 反应的能量变化应为图中曲线d 反应的能量变化应为图中曲线d |
| B.步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是Ⅱ |
C. 与 与 反应,氘代甲醇的产量: 反应,氘代甲醇的产量: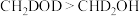 |
D.若 与 与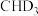 反应,生成的氘代甲醇有2种 反应,生成的氘代甲醇有2种 |
您最近一年使用:0次
2023-12-15更新
|
390次组卷
|
5卷引用:浙江省Z20名校联盟2023-2024学年高三上学期12月月考化学试题
浙江省Z20名校联盟2023-2024学年高三上学期12月月考化学试题(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)(已下线)压轴题04 化学反应机理 历程 能垒图分析(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)河南省郑州市宇华实验学校2023-2024学年高三上学期1月期末化学试题(已下线)选择题11-15
5 . 一定温度下,反应物 转化为产物
转化为产物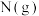 或
或 的关系式如下。已知稳定性
的关系式如下。已知稳定性 ,反应Ⅱ的活化能小于反应Ⅲ的活化能,假设
,反应Ⅱ的活化能小于反应Ⅲ的活化能,假设 的相对能量为0。
的相对能量为0。
Ⅰ:

Ⅱ:

Ⅲ:

Ⅳ:

下列说法正确的是
 转化为产物
转化为产物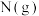 或
或 的关系式如下。已知稳定性
的关系式如下。已知稳定性 ,反应Ⅱ的活化能小于反应Ⅲ的活化能,假设
,反应Ⅱ的活化能小于反应Ⅲ的活化能,假设 的相对能量为0。
的相对能量为0。Ⅰ:


Ⅱ:


Ⅲ:


Ⅳ:


下列说法正确的是
A. |
B.相同条件下,单位体积内活化分子数:Ⅱ Ⅲ Ⅲ |
C.在Ⅰ建立平衡后的密闭容器中再充入 ,新平衡时 ,新平衡时 的转化率下降 的转化率下降 |
D.相同条件下,平衡时正反应速率: |
您最近一年使用:0次
解题方法
6 . 乙醇在浓硫酸做催化剂的条件下发生脱水反应,反应历程和能量变化关系图如下,下列说法正确的是。
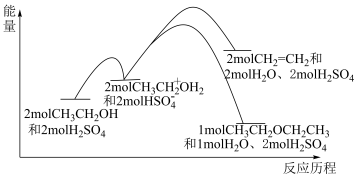
| A.采用较低温度,可获得产率更高的乙醚 |
| B.在上述相同条件下,正丙醇比异丙醇更容易反应 |
| C.为了获得更多的乙烯,温度越高越好 |
| D.选择合适的催化剂,可提高平衡时乙烯的产率 |
您最近一年使用:0次
名校
解题方法
7 . 丙烯是一种重要的化工原料,在催化剂作用下,可以由丙烷直接脱氢或氧化脱氢制备。
反应Ⅰ(直接脱氢):

反应Ⅱ(氧化脱氢):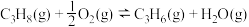

反应Ⅲ(氢气燃烧):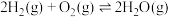
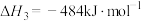
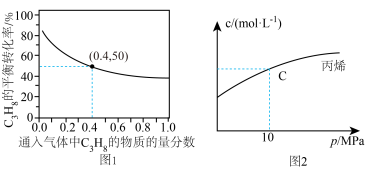
(1)
_____ kJ/mol。
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入 和Ar的混合气体。在温度为
和Ar的混合气体。在温度为 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图1
的物质的量分数的关系如图1
①结合图1,从平衡移动的角度分析,“通入Ar”的作用是_____ 。
②若要将 的平衡转化率提高到60%,则
的平衡转化率提高到60%,则
_____ 。
(3)恒温条件下,测得反应Ⅰ平衡时 的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时
的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时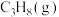 的物质的量浓度随平衡总压变化的曲线
的物质的量浓度随平衡总压变化的曲线_____ 。(在图中C点平衡总压为10Mpa时,丙烷和丙烯的物质的浓度相等)。
(4)①关于反应Ⅲ,下列说法正确的是_____ 。
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高 的转化率
的转化率
②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是_____ 。
(5)研究表明, 可催化氧化
可催化氧化 脱氢制丙烯。在p=0.1MPa,
脱氢制丙烯。在p=0.1MPa, ,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
下列说法不正确的是_____。
反应Ⅰ(直接脱氢):


反应Ⅱ(氧化脱氢):
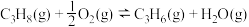

反应Ⅲ(氢气燃烧):
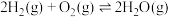
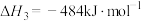
(1)

(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入
 和Ar的混合气体。在温度为
和Ar的混合气体。在温度为 时,
时, 的平衡转化率与通入气体中
的平衡转化率与通入气体中 的物质的量分数的关系如图1
的物质的量分数的关系如图1①结合图1,从平衡移动的角度分析,“通入Ar”的作用是
②若要将
 的平衡转化率提高到60%,则
的平衡转化率提高到60%,则
(3)恒温条件下,测得反应Ⅰ平衡时
 的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时
的物质的量浓度与平衡总压的关系如图2.请在图上画出平衡时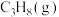 的物质的量浓度随平衡总压变化的曲线
的物质的量浓度随平衡总压变化的曲线(4)①关于反应Ⅲ,下列说法正确的是
A.该反应在任何温度下都能自发进行
B.升高温度,反应Ⅱ的平衡常数增大
C.通入的氧气越多,越有利于丙烷的氧化脱氢
D.将水液化分离出来,既可以加快反应速率,又能提高
 的转化率
的转化率②与直接脱氢反应相比,氧化脱氢制备丙烯的优点是
(5)研究表明,
 可催化氧化
可催化氧化 脱氢制丙烯。在p=0.1MPa,
脱氢制丙烯。在p=0.1MPa, ,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:
,催化剂X的催化下,气体按一定流速通过反应器,丙烷转化率和产物选择性(丙烯的选择性=丙烯的产率÷丙烷的转化率×100%)随温度变化如下表:| t℃ | 丙烷转化率 | 产物的选择性 | ||
 |  | CO | ||
| 400 | 4.06 | 93.12 | 2.20 | 4.68 |
| 500 | 12.32 | 91.23 | 3.16 | 5.61 |
| 600 | 35.22 | 85.44 | 7.73 | 6.83 |
| A.在较高温度下,催化剂X可提高产生丙烯反应的速率 |
B. 催化氧化 催化氧化 脱氢制丙烯的反应是放热反应 脱氢制丙烯的反应是放热反应 |
| C.相同条件下,使用不同的催化剂,丙烷的平衡转化率相同 |
| D.温度升高,催化剂X的活性下降,丙烯的产率降低 |
您最近一年使用:0次
2023-12-05更新
|
218次组卷
|
4卷引用:浙江省稽阳联谊学校2023-2024学年高三上学期联考化学试题
浙江省稽阳联谊学校2023-2024学年高三上学期联考化学试题(已下线)专题10 化学反应原理综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省宁波市2023-2024学年高二上学期九校联考化学试题河南省焦作市博爱县第一中学2023-2024学年高二上学期1月期末化学试题
8 . 氢能源是最具应用前景的能源之一。甲烷-水蒸气催化重整制氢(SMR)是一种制高纯氢的方法之一,其涉及的主要反应如下:
反应Ⅰ:
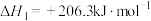
反应Ⅱ: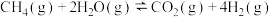

反应Ⅲ:
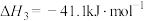
回答下列问题:
(1)反应Ⅱ能自发进行的条件是___________ 。
(2)一定温度下,向某容积为1L的恒容容器中按照水碳比[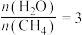 ]充入
]充入 和
和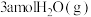 ,tmin后反应达到平衡。达到平衡时,容器中CO为mmol,
,tmin后反应达到平衡。达到平衡时,容器中CO为mmol, 为nmol。
为nmol。
①下列说法不正确 的是___________ 。
A.为防止催化剂中毒和安全事故发生,需对原料气进行脱硫等净化处理
B.提高水碳比[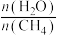 ],有利于提高
],有利于提高 的产率
的产率
C.升高温度有利于反应Ⅰ、Ⅱ的平衡正向移动,温度越高越好
D.以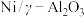 作催化剂,降低反应活化能,提高反应速率和原料利用率
作催化剂,降低反应活化能,提高反应速率和原料利用率
②反应Ⅲ的平衡常数
___________ (用含a,m,n的代数式表示)。
(3)650℃(局部温度过高会造成积碳)、按照一定流速通入原料气,当水碳比[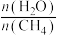 ]一定时,催化剂中无添加吸附剂和添加
]一定时,催化剂中无添加吸附剂和添加 吸附剂(吸收
吸附剂(吸收 ),各气体组分反应的平衡含量与时间的关系如图所示:
),各气体组分反应的平衡含量与时间的关系如图所示:
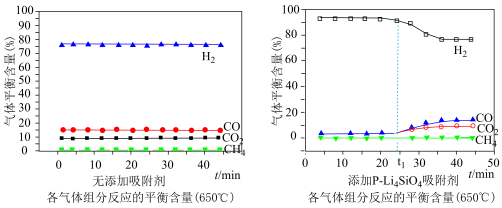
①催化剂中添加 吸附剂与无添加吸附剂比较,
吸附剂与无添加吸附剂比较,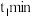 前
前 的平衡含量升高,
的平衡含量升高, 、CO和
、CO和 的平衡含量降低;
的平衡含量降低;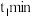 后
后 的平衡含量降低,
的平衡含量降低, 、CO和
、CO和 的平衡含量升高,最后与无添加吸附剂时的含量相同,可能的原因是
的平衡含量升高,最后与无添加吸附剂时的含量相同,可能的原因是___________ 。
②实验时发现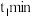 后
后 的平衡含量低于理论平衡值,CO的平衡含量高于理论平衡值,可能的原因是
的平衡含量低于理论平衡值,CO的平衡含量高于理论平衡值,可能的原因是___________ 。(用化学反应方程式表示)
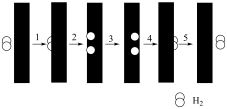
(4)该反应常采用钯膜分离技术(可选择性地让某气体通过而离开体系),其机理如图所示,其中过程2: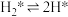 ,其活化能
,其活化能 ;过程3:H*在钯膜内的迁移速率是决速步骤(*表示物质吸附在催化剂表面),下列说法
;过程3:H*在钯膜内的迁移速率是决速步骤(*表示物质吸附在催化剂表面),下列说法不正确 的是___________。
反应Ⅰ:

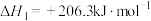
反应Ⅱ:
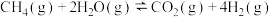

反应Ⅲ:

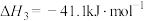
回答下列问题:
(1)反应Ⅱ能自发进行的条件是
(2)一定温度下,向某容积为1L的恒容容器中按照水碳比[
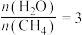 ]充入
]充入 和
和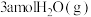 ,tmin后反应达到平衡。达到平衡时,容器中CO为mmol,
,tmin后反应达到平衡。达到平衡时,容器中CO为mmol, 为nmol。
为nmol。①下列说法
A.为防止催化剂中毒和安全事故发生,需对原料气进行脱硫等净化处理
B.提高水碳比[
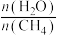 ],有利于提高
],有利于提高 的产率
的产率C.升高温度有利于反应Ⅰ、Ⅱ的平衡正向移动,温度越高越好
D.以
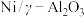 作催化剂,降低反应活化能,提高反应速率和原料利用率
作催化剂,降低反应活化能,提高反应速率和原料利用率②反应Ⅲ的平衡常数

(3)650℃(局部温度过高会造成积碳)、按照一定流速通入原料气,当水碳比[
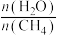 ]一定时,催化剂中无添加吸附剂和添加
]一定时,催化剂中无添加吸附剂和添加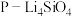 吸附剂(吸收
吸附剂(吸收 ),各气体组分反应的平衡含量与时间的关系如图所示:
),各气体组分反应的平衡含量与时间的关系如图所示:
①催化剂中添加
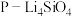 吸附剂与无添加吸附剂比较,
吸附剂与无添加吸附剂比较,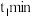 前
前 的平衡含量升高,
的平衡含量升高, 、CO和
、CO和 的平衡含量降低;
的平衡含量降低;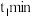 后
后 的平衡含量降低,
的平衡含量降低, 、CO和
、CO和 的平衡含量升高,最后与无添加吸附剂时的含量相同,可能的原因是
的平衡含量升高,最后与无添加吸附剂时的含量相同,可能的原因是②实验时发现
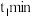 后
后 的平衡含量低于理论平衡值,CO的平衡含量高于理论平衡值,可能的原因是
的平衡含量低于理论平衡值,CO的平衡含量高于理论平衡值,可能的原因是(4)该反应常采用钯膜分离技术(可选择性地让某气体通过而离开体系),其机理如图所示,其中过程2:
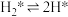 ,其活化能
,其活化能 ;过程3:H*在钯膜内的迁移速率是决速步骤(*表示物质吸附在催化剂表面),下列说法
;过程3:H*在钯膜内的迁移速率是决速步骤(*表示物质吸附在催化剂表面),下列说法
A.钯膜对 分子的透过具有选择性 分子的透过具有选择性 |
B.过程4的 |
| C.采用钯膜分离技术可以提高原料的利用率 |
D.常用 将过程5中的 将过程5中的 吹扫出反应器,增大钯膜两侧的压强差,提高过程1、3速率而促进反应 吹扫出反应器,增大钯膜两侧的压强差,提高过程1、3速率而促进反应 |
您最近一年使用:0次
解题方法
9 . 丙烯是一种重要的化工原料,其主要产品聚丙烯是生产口罩喷溶布的原料。铬基催化剂下丙烷生产丙烯相关主要反应有:
Ⅰ.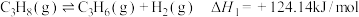
Ⅱ.
Ⅲ.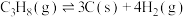
请回答:
(1)已知键能: ,
,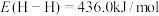 。C=C的键能与C-C的键能相差约
。C=C的键能与C-C的键能相差约___________ kJ/mol。
(2)600℃时,容器压强恒为P,铬基催化剂下两个密闭容器中分别按下表投料发生反应:
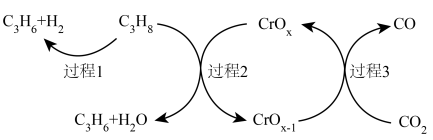
①容器B生成C3H6的反应流程如下:________ 。
A.原料气中通入N2可提高C3H8的平衡转化率
B.升高温度,一定能提高的C3H6平衡产率
C.过程1产生C3H6的量大于过程2和过程3产生的C3H6
D.在铬基催化剂中适当加入CaO可促进过程2平衡正移而提高C3H8的平衡转化率
②若容器A中只发生反应Ⅰ和反应Ⅱ,C3H8的平衡转化率为 ,C3H6的选择性(选择性
,C3H6的选择性(选择性 )为w,计算反应Ⅰ的平衡常数
)为w,计算反应Ⅰ的平衡常数
________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③按照容器A和容器B的气体组分比,将两组气体按相同流速分别通过催化剂固定床反应器,C3H8的转化率和C3H6的选择性随时间变化如图所示:________ ,B组中CO2的作用是________ (用化学方程式和必要的文字说明)。
(3)恒温恒容的密闭容器中通入气体分压比为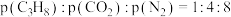 的混合气体,
的混合气体, ,已知某反应条件下只发生反应Ⅳ和反应Ⅴ(
,已知某反应条件下只发生反应Ⅳ和反应Ⅴ( ,
,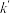 为速率常数,只与温度有关且
为速率常数,只与温度有关且 ):
):
反应Ⅳ: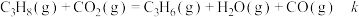
反应Ⅴ:
实验测得丙烯的净生成速率方程为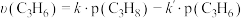 ,请在下图中画出丙烯的物质的量随时间的变化趋势
,请在下图中画出丙烯的物质的量随时间的变化趋势____________ 。
Ⅰ.
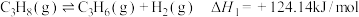
Ⅱ.

Ⅲ.
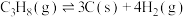
请回答:
(1)已知键能:
 ,
,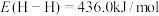 。C=C的键能与C-C的键能相差约
。C=C的键能与C-C的键能相差约(2)600℃时,容器压强恒为P,铬基催化剂下两个密闭容器中分别按下表投料发生反应:
| 容器 | C3H8/mol | CO2/mol | N2/mol |
| A | 1 | 0 | 10 |
| B | 1 | 2 | 8 |
A.原料气中通入N2可提高C3H8的平衡转化率
B.升高温度,一定能提高的C3H6平衡产率
C.过程1产生C3H6的量大于过程2和过程3产生的C3H6
D.在铬基催化剂中适当加入CaO可促进过程2平衡正移而提高C3H8的平衡转化率
②若容器A中只发生反应Ⅰ和反应Ⅱ,C3H8的平衡转化率为
 ,C3H6的选择性(选择性
,C3H6的选择性(选择性 )为w,计算反应Ⅰ的平衡常数
)为w,计算反应Ⅰ的平衡常数
③按照容器A和容器B的气体组分比,将两组气体按相同流速分别通过催化剂固定床反应器,C3H8的转化率和C3H6的选择性随时间变化如图所示:

(3)恒温恒容的密闭容器中通入气体分压比为
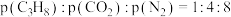 的混合气体,
的混合气体, ,已知某反应条件下只发生反应Ⅳ和反应Ⅴ(
,已知某反应条件下只发生反应Ⅳ和反应Ⅴ( ,
,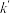 为速率常数,只与温度有关且
为速率常数,只与温度有关且 ):
):反应Ⅳ:
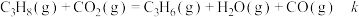
反应Ⅴ:

实验测得丙烯的净生成速率方程为
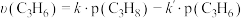 ,请在下图中画出丙烯的物质的量随时间的变化趋势
,请在下图中画出丙烯的物质的量随时间的变化趋势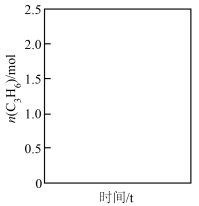
您最近一年使用:0次
10 .  时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示:
时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示:不正确 的是
 时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示:
时,固体酸分子筛催化乙醇脱水,乙醇的分子间脱水和分子内脱水过程与相对能量变化如图所示: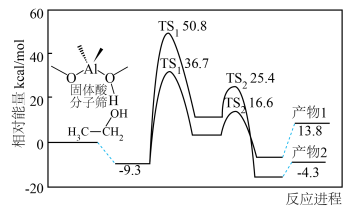
| A.乙醇通过氢键吸附于固体酸分子筛表面并放出热量 |
B.生成产物2的决速步活化能为 |
C.生成产物1的热化学方程式为: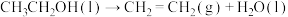 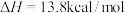 |
| D.升高温度、延长反应时间及选择合适催化剂均可提高产物1的产率 |
您最近一年使用:0次
2023-11-15更新
|
844次组卷
|
5卷引用:浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题
浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题(已下线)专题05 化学反应与能量(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)2024新东方高二上期末考化学03新疆乌鲁木齐市2024届高三第一次质量监测化学试题(已下线)化学(辽宁卷02)-2024年高考押题预测卷



