21-22高三上·甘肃白银·阶段练习
1 . 铍是原子能、火箭、导弹、航空以及冶金工业中不可缺少的宝贵材料。以绿柱石[Be3Al2(SiO3)6]为原料制备两性金属铍的工艺如图:

回答下列问题:
(1)绿柱石写成氧化物的形式为___________ 。
(2)750℃烧结时,Na3FeF6仅与绿柱石中BeO作用生成易溶于水的Na2BeF4,滤渣的主要成分是Fe2O3和___________ 。
(3)“水浸”时“产物压碎磨细”的目的是___________ ,为检验“过滤1”的滤液中是否含有Na+,可选用的方法是___________ (填方法名称)。
(4)“沉氟”的化学方程式为___________ 。
(5)镍坩埚作阴极、石墨作阳极,350~400℃电解NaCl-BeCl2熔融混合物得到金属铍,阳极反应式为___________ ;不能用该电解槽电解熔融氯化铍制金属铍的原因可能是___________ 。

回答下列问题:
(1)绿柱石写成氧化物的形式为
(2)750℃烧结时,Na3FeF6仅与绿柱石中BeO作用生成易溶于水的Na2BeF4,滤渣的主要成分是Fe2O3和
(3)“水浸”时“产物压碎磨细”的目的是
(4)“沉氟”的化学方程式为
(5)镍坩埚作阴极、石墨作阳极,350~400℃电解NaCl-BeCl2熔融混合物得到金属铍,阳极反应式为
您最近一年使用:0次
2 . 钛和钛合金被认为是21世纪的重要金属材料,广泛用于火箭、飞机制造业等。如图是工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备金属钛的工艺流程。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。
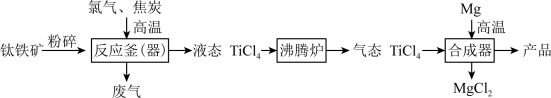
(1)钛酸亚铁(FeTiO3)中钛元素的化合价是___________ 。
(2)钛铁矿在投入反应釜前要先粉碎,其目的是___________ ;反应釜中发生的反应是: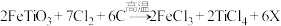 ,X为反应产生的废气,其化学式是
,X为反应产生的废气,其化学式是___________ 。
(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的___________ 不同。
(4)写出合成器中反应的化学方程式___________ 。
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属___________ ,由金属钛的性质可知,除去这种杂质可以用___________ (填试剂名称)。
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是___________ 。
资料:Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是
(2)钛铁矿在投入反应釜前要先粉碎,其目的是
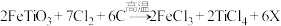 ,X为反应产生的废气,其化学式是
,X为反应产生的废气,其化学式是(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的
(4)写出合成器中反应的化学方程式
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是
您最近一年使用:0次
名校
解题方法
3 . 黄铁矿的主要成分是FeS2,其中含有一定量的铜、钴等金属。某工厂在传统回收工艺的基础上进一步改进焙烧方式,研究出高效利用硫铁矿资源的工艺如下:
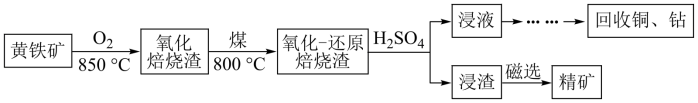
(1)黄铁矿焙烧之前需要粉碎,其目的是:_______
(2)①黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是 ,反应的化学方程式为:
,反应的化学方程式为:_______ ;
②制硫酸工艺中涉及反应2SO2+O2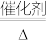 2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是
2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是_______ 。
(3)用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为_______ (填化学式);浸液通过加入萃取剂可实现铜和钴的分离,在萃取前加入NaOH溶液乳化可提高分离效率,不同浓度的溶液对萃取率的影响如图,则NaOH溶液最佳的浓度为_______ 。
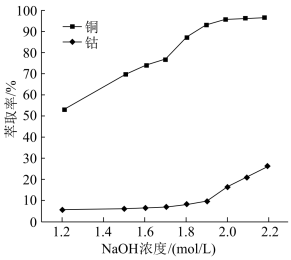
已知黄铁矿氧化焙烧前后主要元素质量分数如表,为测定铜的浸出率,取50 g焙烧后的烧渣,经处理后测得Cu2+物质的量为5×10-3 mol,则铜离子的浸出率为_______ (结果保留三位有效数字)。

(1)黄铁矿焙烧之前需要粉碎,其目的是:
(2)①黄铁矿的氧化焙烧是制硫酸工艺的重要一步,其产物之一是
 ,反应的化学方程式为:
,反应的化学方程式为:②制硫酸工艺中涉及反应2SO2+O2
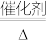 2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是
2SO3 ΔH<0,该反应需将温度控制在400-500℃,温度不宜过低的原因是(3)用硫酸浸取后的浸渣能用磁选法分离,则该氧化物为

已知黄铁矿氧化焙烧前后主要元素质量分数如表,为测定铜的浸出率,取50 g焙烧后的烧渣,经处理后测得Cu2+物质的量为5×10-3 mol,则铜离子的浸出率为
| 项目 | Fe | S | Cu | Co |
| 焙烧前(%) | 40.28 | 42.55 | 0.53 | 0.022 |
| 焙烧后(%) | 53.08 | 0.96 | 0.76 | 0.047 |
您最近一年使用:0次
11-12高二上·广东广州·期中
4 . 某探究小组通过比较酸性KMnO4溶液与H2C2O4溶液反应过程中,溶液紫色消失时间长短的方法,研究浓度、温度对反应速率的影响。
可供选择的实验条件:KMnO4酸性溶液的浓度可选择0.01 mol·L-1、0.1 mol·L-1,H2C2O4溶液的浓度可选择0.1 mol·L-1、0.2 mol·L-1,实验温度可选择298K、323K。每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液的用量均为2mL。
(1)实验设计:请完成以下实验设计表。
(2)实验记录:实验中需要记录的数据是___________________________________ 。
可供选择的实验条件:KMnO4酸性溶液的浓度可选择0.01 mol·L-1、0.1 mol·L-1,H2C2O4溶液的浓度可选择0.1 mol·L-1、0.2 mol·L-1,实验温度可选择298K、323K。每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液的用量均为2mL。
(1)实验设计:请完成以下实验设计表。
| 实验编号 | T/K | KMnO4浓度/mol·L-1 | H2C2O4浓度/mol·L-1 | 实验目的 |
| ① | 298 | 0.01 mol·L-1 | 0.1 mol·L-1 | 为以下实验做对照 |
| ② | ||||
| ③ | 探究浓度对反应速率的影响 |
(2)实验记录:实验中需要记录的数据是
您最近一年使用:0次



